Freie Universit¨at Berlin WS 2006/2007
Fachbereich Physik 8.12.2006
Statistische Physik - Theorie der W¨ arme
(PD Dr. M. Falcke)
Ubungsblatt 9: ¨ Thermodynamische Identit¨aten, Thermische/Kalorische Zustandsgleichung, Kreisprozesse
Aufgabe 1 (4 Punkte)
Beweisen Sie die thermodynamischen Identit¨aten C
pC
V= κ
Tκ
S,
∂T
∂V
S
= − T C
V∂p
∂T
V
, ∂T
∂p
S
= T C
p∂V
∂T
p
. Hierbei bezeichnet κ
Tdie isotherme und κ
Sdie adiabatische Kompressibilit¨at.
Aufgabe 2 (2 Punkte)
Ein in einem Hohlraum eingeschlossenes Photonengas (Hohlraumstrahlung) wird durch die Zustands- gleichung
p = 1
3 u(T ), u = U V
beschrieben. Welche Aussagen lassen sich ¨ uber die Form der thermischen und kalorischen Zustands- gleichung aus der zugeh¨origen Gibbsschen Fundamentalgleichung
T dS = dU + pdV ableiten.
Aufgabe 3 (5 Punkte)
Ein ideales Gas erf¨ ullt bei 300 K ein Volumen von 0,5 m
3bei einem Druck von 202650 Pa. Zun¨achst expandiert das Gas adiabatisch bis zu einem Volumen von 1,2 m
3. Im folgenden Schritt wird es isobar bis zu seinem urspr¨ unglichen Volumen komprimiert. Schließlich wird der Druck isochor so lange erh¨oht, bis das Gas wieder in seinen Ausgangszustand zur¨ uckkehrt. Der Adiabatenkoeffizient sei 5/3.
a. Stellen Sie den Kreisprozess in einem p − V Diagramm dar.
b. Bestimmen Sie die Temperatur am Ende eines jeden Teilschrittes.
c. Berechnen Sie die Arbeit, die w¨ahrend eines Umlaufs verrichtet wird.
d. Wie h¨angt die Temperatur mit der Entropie w¨ahrend der drei Teilschritte zusammen? Stellen Sie den Kreisprozess in einem T − S Diagramm dar.
e. Verifizieren Sie die Gibbs-Duhem-Relation.
Hinweis: Verwenden Sie die Adiabatengleichung pV
γ= const entlang einer Adiabaten.
Abgabetermin: Mittwoch, 20.12.2006 vor Beginn der Vorlesung.
L¨ osungen
Aufgabe 1
Nach den Rechenregeln f¨ ur die Jakobi Determinante ergibt sich C
p= T
∂S
∂T
p
= T ∂(S, p)
∂(T, p) = T ∂(S, p)
∂(S, V )
∂(S, V )
∂(T, V )
∂(T, V )
∂(T, p)
= ∂V
∂p
S
−1C
V∂V
∂p
T
= C
Vκ
Tκ
S,
(1)
woraus die erste Behauptung unmittelbar folgt. Ausgehend vom Differential der freien Energie
dF = − SdT − pdV (2)
erhalten wir die Maxwell Relation ∂S
∂V
T
= − ∂
2F
∂T ∂V = ∂p
∂T
V
. (3)
Weiterin ist ∂T
∂V
S
= ∂(T, S)
∂(V, S) = ∂(T, S)
∂(V, T )
∂(V, T )
∂(V, S) = − ∂S
∂V
T
∂S
∂T
V
−1= − T C
V∂S
∂V
T
, (4)
woraus nun
∂T
∂V
S
= − T C
V∂p
∂T
V
(5) folgt. F¨ur die letzte Identit¨at gehen wir vom Differential der freien Enthalpie aus
dG = − SdT + V dp . (6)
Hier lautet die Maxell-Relation ∂S
∂p
T
= − ∂
2G
∂T ∂G = − ∂V
∂T
p
. (7)
In Analogie zur vorherigen Relation finden wir ∂T
∂p
S
= ∂(T, S)
∂(p, S ) = ∂(T, S)
∂(p, T )
∂(p, T )
∂(p, S) = − ∂S
∂p
T
"
∂S
∂T
p
#
−1= − T C
p∂S
∂p
T
, (8)
womit wir schließlich erhalten:
∂T
∂p
S
= T C
p∂V
∂T
p
. (9)
Aufgabe 2
Thermische p = p(V, T ) und kalorische Zustandsgleichung U = U (V, T ) eines Systems sind nicht un- abh¨angig voneinander vorgebbar. Ihr Zusammenhang erschließt sich ¨uber die gemischten partiellen Ableitungen der Entropie nach ihren nat¨ urlichen Variablen. Zun¨achst setzt man das vollst¨andige Diffe- renzial der innern Energie dU = (∂U/∂T )
VdT +(∂U/∂V )
TdV in die Gibbssche Fundamentalgleichung ein
T dS = dU + pdV = ∂U
∂T
V
dT + ∂U
∂V
T
+ p
dV (10)
=
!T ∂S
∂T
V
dT + T ∂S
∂V
T
dV. (11)
Daraus erh¨alt man durch Vergleich ∂S
∂T
V
= 1 T
∂U
∂T
V
und ∂S
∂V
T
= 1 T
∂U
∂V
T
+ p
(12) und wegen der Vertauschbarkeit der gemischten zweiten Ableitungen ∂
2S/∂T ∂V = ∂
2S/∂V ∂T schließ- lich die gesuchte Relation
∂U
∂V
T
= T ∂p
∂T
V
− p. (13)
Unter Benutzung dieses Zusammenhanges folgt f¨ ur das Photonengas ∂U
∂V
T
= u(T ) = T 1 3
du(T ) dT − 1
3 u(T ) (14)
also die Differentialgleichung
4 dT T = du
u (15)
welche durch
U (T, V ) = b · V T
4, b = const (16)
gel¨ost wird. Die thermische Zustandsgleichung hat demnach die Form p(T, V ) = 1
3 b · T
4. (17)
Aufgabe 3
a. Abbildung 1 zeigt den Kreisprozess im p − V Diagramm. Die einzelnen Schritte sind durchnum- meriert.
V (m
3)
P (Pa)
T=300 K T=167 K
0.5 1.2 202650
47104
PV
γ= const
1
2 3
Abbildung 1: Verlauf des Kreisprozesses in der p − V Ebene. Die Achsen sind nicht maßstabsgetreu skaliert.
b. Aus der Adiabatengleichung pV
γ= c
1folgt nach der Zustandsgleichung des idealen Gases unmittelbar T V
γ−1= c
2, wobei c
1, c
2= const. Daher ist mit p
1= 202650 Pa, T
1= 300 K, V
1= 0, 5 m
3und V
2= 1, 2 m
3:
p
2= p
1V
1γV
2γ= 47104 Pa ⇔ T
2= T
1V
1γ−1V
2γ−1= 167, 36 K . (18)
Nach der isobaren Kompression zum Ursprungsvolumen gilt p
3= p
2und V
3= V
1sowie mittels der Zustandsgleichung des idealen Gases
T
3= T
2p
3V
3p
2V
2= 70 K . (19)
c. Sei W = H
pdV die Arbeit, die w¨ahrend des ganzen Kreisprozesses verrichtet wird. Der Beitrag aus dem ersten Teilschritt ergibt sich zu
W
1=
V2
Z
V1
pdV = c
1 V2Z
V1
V
−γdV = c
11 − γ
h V
21−γ− V
11−γi = c
11 − γ p
2V
2c
1− p
1V
1c
1= 67200, 3 J ,
(20)
wobei wir die Adiabtengleichung verwendet haben. Im zweiten Teilschritt erhalten wir W
2=
V3
Z
V2
pdV = p
2 V3Z
V2
dV = p
2[V
3− V
2] = − 32972, 8 J . (21) Da sich im dritten Schritt das Volumen nicht mehr ¨andert, verschwindet W
3. Daher finden wir abschließend W = W
1+ W
2= 34227, 5 J: das System leistet also Arbeit an der Umgebung.
d. Aus Aufgabe 1, Blatt 5 wissen wir, dass die Entropie eines idealen Gases S = N k
Bln
V N λ
3+ 5
2
(22) betr¨agt, wobei λ := h/ √
2πmk
BT die thermische Wellenl¨ange bezeichnet. Daher erhalten wir auf dem ersten Teilst¨ uck
S = N k
B"
ln (
c
1T
1/γ−1(2πmk
BT )
3/2N h
3) + 5
2
#
= N k
B"
ln
( (2πc
1mk
B)
3/2N h
3) + 5
2
#
= const .
(23)
Im zweiten Schritt folgt wegen pV = N k
BT und p = const S = N k
B"
ln ( k
BT
p
(2πmk
BT )
3/2h
3) + 5
2
#
= N k
Bln n
c
3T
5/2o + 5
2
(24) mit c
3= const. Somit ist
T (S) ∝ exp 2S
5N k
B− 1
. (25)
S
T (K)
1
2 3
300
167 70
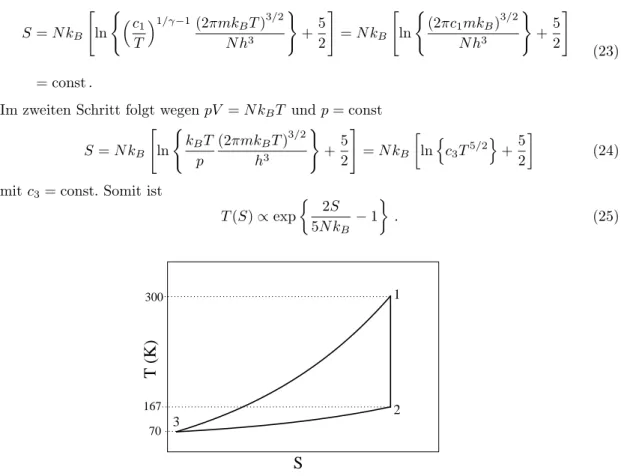
Abbildung 2: Verlauf des Kreisprozesses in der T − S Ebene. Die Achsen sind nicht maßstabsgetreu skaliert.
Da das Volumen im letzten Schritt konstant gehalten wird, resultiert die einzige Temperatu- rabh¨angigkeit der Entropie aus der thermischen Wellenl¨ange, also
S = N k
Bln n
c
4T
3/2o + 5
2
⇔ T (S) ∝ exp 2S
3N k
B− 5 3
(26)
mit c
4= const. Abbildung 2 illustriert den Zusammenhang zwischen T und S.
e. Die Gibbs-Duhem-Relation besagt, dass F + pV − µN = 0 ist. Die freie Energie eines idealen Gases berechnet sich zu
F = U − T S = 3
2 N k
BT − T N k
Bln
V N λ
3+ 5
2
(27)
= − N k
BT
ln V
N λ
3+ 1
. (28)
Daraus erhalten wir umgehend µ =
∂F
∂N
T,V