Philipps-Universität Marburg
Fachbereich Chemie
Seminar: Übungen im Experimentalvortrag, SS 2006 Leitung: Prof. Dr. B. Neumüller, Dr. P. Reiß,
Prof. Dr. M. Bröring, Prof. Dr. Koert
Aminosäuren
und
Proteine
Experimentalvortrag vom 06.07.2006
Anke Schleipen, Hinweis:
Dieses Protokoll stammt von der Seite www.chids.de (Chemie in der Schule).
Dort können unterschiedliche Materialien für den Schulunterricht heruntergeladen werden, unter anderem hunderte von Experimentalvorträgen so wie der vorliegende:
http://online-media.uni-marburg.de/chemie/chids/veranstaltungen/uebungen_experimentalvortrag.html
INHALTSVERZEICHNIS
1. Aminosäuren ... Seite 2 1.1 Definition Aminosäure... Seite 2 1.2 Häufigkeit und Vorkommen von Aminosäuren ... Seite 2
Versuch 1: Nachweis der Aminogruppe... Seite 3 1.3 Die proteinogenen Aminosäuren ... Seite 6 1.4 Nicht-poteinogene Aminosäuren ... Seite 9 1.5 Optische Aktivität von Aminosäuren / D- L-Stereoisomere... Seite 9 1.6 Aminosäuren sind Zwitterionen ... Seite 10
Versuch 2: Löslichkeit von Tyrosin ... Seite 12
Versuch 3: Nachweis von -Aminosäuren in Aufbau-
präparaten mit Ninhydrin ... Seite 13 2. Von der Aminosäure zum Protein – Proteinbiosynthese ... Seite 16
3. Proteine ... Seite 17 3.1 Peptidbindung ... Seite 17 3.2 Definition Proteine ... Seite 17 3.3 Vorkommen und Funktionen von Proteinen ... Seite 18 3.4 Strukturgebung ... Seite 19
Demo 1: Schleimlösende Wirkung von Acetylcystein ... Seite 23
Versuch 4: Xanthoprotein-Reaktion ... Seite 25
Versuch 5: Biuret-Reaktion ... Seite 27
Demo 2: Auswaschen von Blutfleck ... Seite 28 3.5 Isolierung, Reinigung und Analyse von Proteinen ... Seite 29
Demo 3: Proteinfingerabdruck ... Seite 32 3.6 Löslichkeitsverhalten von Proteinen ... Seite 34
Versuch 6: Tyndall-Effekt einer Eiklar-Lösung ... Seite 34
4. Literaturangabe ... Seite 36
1. Aminosäuren
1.1 Definition:
Aminosäuren sind Carbonsäuren, die eine Aminogruppe enthalten. Das bedeutet, das Aminosäuren bifunktionell sind, da sie sowohl eine Aminogruppe als auch eine Carboxygruppe (Säuregruppe) enthalten.
Die meisten Aminosäuren sind -Aminosäuren, d. h. am C
2-Atom hängt die Aminogruppe.
H2N OH
O
R H
1.2 Häufigkeit und Vorkommen von Aminosäuren
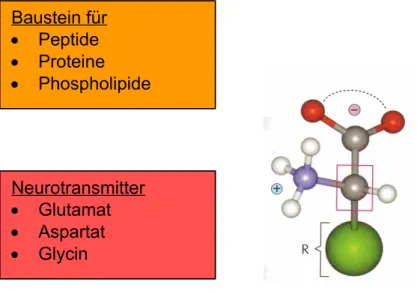
Wie bereits oben im Schaubild zu erkennen ist, erfüllen Aminosäuren in unserem Körper die unterschiedlichsten Funktionen.
Den Schülern am meisten bekannt ist ihre Funktion als Bausteine von Proteinen und Peptiden, worauf ich später noch einmal detaillierter eingehen werde.
Auch können Aminosäuren als Neurotransmitter fungieren. Dabei können sowohl proteinogene Aminosäuren, als auch biogene Amine Neurotransmitterfunktion haben.
Baustein für
Peptide
Proteine
Phospholipide
Neurotransmitter
Glutamat
Aspartat
Glycin
Vorstufe für
biogene Amine
Glucose
Nucleotide
Häm, Keratin
Transportmolekül für
NH
2-Gruppen
Abb. 1: Aminosäure allgemein (eigener Entwurf)
Abb. 2: Funktionen (eigener Entwurf + nach RÖHM)
Besonders wichtig ist Glutamat, das als erregender Transmitter im ZNS aktiv ist. Mehr als die Hälfte aller Synapsen im Gehirn sind glutaminerg.
Glycin hingegen ist ein inhibitorischer Neurotransmitter, dessen Wirkungen im Rückenmark und im Gehirn lokalisiert ist.
Auch sind Aminosäuren Vorstufen für biogene Amine. Diese enstehen durch eine weitere Umwandlung von proteinogenen Aminen. Beispielsweise entsteht durch Decarboxylierung von Glutamat der Neurotransmitter -Aminobutyrat (GABA). Dieses hat eine inhibitorische Neurotransmitterfunktion im ZNS.
Aber auch Noradrenalin, Adrenalin, Serotonin, das sich vom Tryptophan ableitet, und Histamin gehören zu den biogenen Aminen. Diese haben u.a. Funktionen als Mediatoren und Hormone.
Aminosäuren sind die Vorstufen für eine Vielzahl von Molekülgruppen – nicht nur für biogene Amine. Sie sind beispielsweise die Vorstufe für die Glucose in der Gluconeogenese, für Purin- und Pyrimidinbasen, für Häm und für andere Moleküle.
Desweiteren können Aminosäuren als Intermediate und NH
2-Transportmoleküle beim Harnstoffzyklus fungieren.
Versuch 1: Nachweis der Aminogruppe
Die Aminogruppe soll in Gly mit der VAN SLYKE-Methode nachgewiesen werden. Der dabei entstehende Distickstoff soll qualitativ durch das Verlöschen einer brennenden Kerze unnd durch Einleiten in Bariumhydroxid-Lösung (keine Trübung) nachgewiesen werden.
Geräte: Magnetrührer mit Rührfisch, Dreihalskolben (250 mL, 3 x NS 29), Absaugstück NS 29, Tropftrichter mit Druckausgleich (100 mL, NS 29), zwei Glasstopfen NS 29, zwei Waschflaschen, Messzylinder (200 mL), Stativmaterial, Schlauchschellen, PVC-Schlauch, Federn, Abzug, Kerze, Feuerzeug, Winkelrohr, Becherglas (100 mL), Keck- Klemmen
Chemikalien: Natriumnitrit-Lösung (c = 2 mol/L),
salzsaure Gly-Lösung (c = 2 mol/L) (bis sich Gly vollständig gelöst hat)
Natronlauge (c = 2 mol/L)
Versuchsaufbau:
Mithilfe von Schlauchschellen müssen die Verbindungen zwischen Glas und PVC-Schlauch gesichert werden. Desweiteren müssen die Schliffverbindungen gefettet werden. Ein Stopfen darf nicht gesichert werden, da er als Druckausgleich dient.
Durchführung: 100 mL Natriumnitritlösung werden in den Tropftrichter, 100 mL salzsaure Gly-Lösung werden in den Dreihalskolben gefüllt. Die zweite Waschflasche wird bis zur Hälfte mit Natronauge gefüllt (Blasenzähler, Umsetzung nitroser Gase).
Unter ständigem Rühren wird der Hahn des Trichters vorsichtig geöffnet und die NaNO
2-Lösung langsam in den Kolben getropft.
Nach ca. 30 Min. hat sich genügend Distickstoff im Messzylinder angesammelt und es kann mit dem Distickstoffnachweis gestartet werden.
Beim Einleiten des entstehenden Gases in eine Bariumhydroxid-Lösung ist keine Reaktion erkennbar.
Desweiteren wird eine brennende Kerze in den Messzylinder gehalten.
Beobachtung: Nach Zugabe weniger Tropfen NaNO
2-Lösung ist im Rundkolben eine rege Gasentwicklung sichtbar. Auch erwärmt sich der Kolben.
Abb. 2: Versuchsaufbau (eigener Entwurf)
Desweiteren sind nitrose Gase (Braunfärbung) in der ersten Waschflasche erkennbar.
Beim Distickstoffnachweis kommt es beim Einleiten des entstehenden Gases zu keiner erkennbaren Nachweisreaktion. Sobald man die brennende Kerze in den Kolben hält, erlischt diese schon am Anfang des Messzylinders.
Auswertung: Die Flamme erlischt, da Distickstoff entstanden ist. Da beim Einleiten in die Bariumhydroxid-Lösung keine Reaktion erkennbar ist, kann es sich bei dem entwickelnden Gas nicht um CO
2handeln, sondern muss N
2sein.
Gesamtreaktion:
H2N
OH
O
+ HNO2 HO
OH
O
+ N2 + H2O
Glycin Salpetrige Säure Glucolsäure
Bildung des Elektrophils:
NO2 HNO2 O N
OH2
N O N O
H+ H+
Durch Protonierung des Nitrits entsteht formal salpetrige Säure. Durch weitere Protonierung und anschließende Wasserabspaltung wird ein Nitrosylkation (2 mesomere Grenzformeln) gebildet.
Diazotierung:
R NH2 + N O R NH2
N O
R N
N OH2
~2 H H2O
- H2O
R N N R N N
Diazonium-Ion
Das lone-pair der NH
2-Gruppe greift nukleophil am postiv polarisierten Stickstoff des Nitrosylkations an. Durch eine Tautomerisierung und anschließende Wasserabspaltung wird das Diazoniumion gebildet.
Freisetzung von Stickstoff:
R N N + H2O R OH + N2 + H+
Durch eine S
NI-Reaktion wird Distickstoff als Abgangsgruppe freigesetzt. Distickstoff ist eine sehr gute Abgangsgruppe, da sie sehr stabil ist und zudem die Entropie erhöht.
1.3 Die proteinogenen Aminosäuren
Insgesamt sind inzwischen mehr als 500 verschiedene Aminosäuren bekannt. Aber laut Literatur kommen in unserem Körper nur 20 proteinogene Aminosäuren vor. Proteinogen bedeutet, dass diese Aminosäuren in den Proteinen vorkommen. Nur für die folgenden 20 Aminosäuren codiert die DNA.
Ausgehend von ihrer Seitenkette lassen sich die Aminosäuren zu folgenden Gruppen zusammenfassen:
Hydrophobe Aminosäuren: Gly, Ala, Val, Leu, Ile Aromatische Aminosäuren: Phe, Tyr, Trp
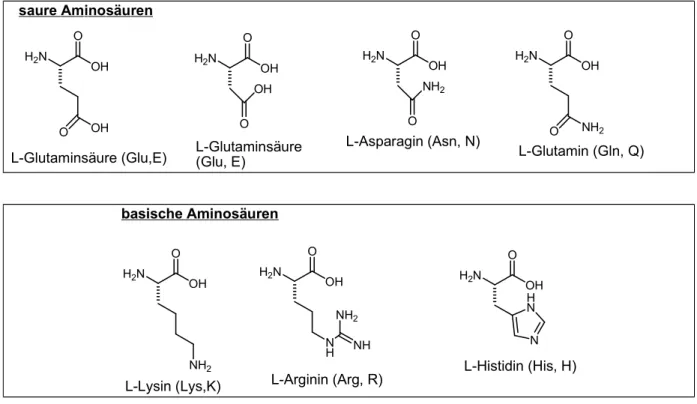
Polare Aminosäuren: Ser, Thr, Cys, Met Saure Aminosäuren: Asp, Glu, Asn, Gln Basische Amnosäuren: Lys, Arg, His
Aus der Tabelle geht ebenfalls hervor, dass die Aminosäuren nicht nur mit ihrem Namen,
sondern mit einem Drei- oder Ein-Buchstaben-Coden bezeichnet werden.
H2N
OH O
Glycin (Gly,G)
H2N
OH O
L-Leucin (Leu,L) H2N
OH O
H2N
OH O
H2N
OH O
L-Valin (Val,V)
L-Alanin (Ala,A)
L-Isoleucin (Ile, I) Hydrophobe Aminosäuren
H2N
OH O
L-Phenylalanin (Phe,F)
HN
OH O H2N
OH O
OH L-Tyrosin (Tyr, Y)
L-Prolin (Pro, P) sek.
Aminofunktion
H2N
OH O
NH
L-Tryptophan (Trp, T) aromatische Aminosäuren
H2N
OH O
OH L-Serin (Ser,S)
H2N
OH O
SH L-Cystein (Cys,C)
H2N
OH O
OH
H2N
OH O
L-Threonin (Thr, T) SMe
L-Methionin (Met, M) polare Aminosäuren
H2N
OH O
O OH
L-Glutaminsäure (Glu,E)
H2N
OH O
H2N
OH O
H2N
OH O
OH O
L-Glutaminsäure (Glu, E)
NH2 O
L-Asparagin (Asn, N) O NH2 L-Glutamin (Gln, Q) saure Aminosäuren
H2N
OH O
NH2 L-Lysin (Lys,K)
H2N
OH O
NH
H2N
OH O
NH2 NH L-Arginin (Arg, R)
N HN
L-Histidin (His, H) basische Aminosäuren
Von den 20 proteinogenen Aminosäuren sind 8 essentiell. Der Körper kann diese nicht synthetisieren; deshalb müssen diese Aminosäuren mit der Nahrung aufgenommen werden.
Die essentiellen Aminosäuen sind: Valin, Leucin, Isoleucin, Phenylalanin, Threonin, Lysin, Tryptophan, Cystein, Methionin.
MERKSPRUCH: Phenomenale Isolde trüpt metunter Leutnant Valentins lysterne Thräume.
Abb. 4: Aminosäuren (eigener Entwurf)
1.4 Nicht-proteinogene Aminosäuren
Wie bereits bei 1.2 erwähnt, kommen Aminosäuren nicht nur in Proteinen vor. Diese nicht- proteinogenen Aminosäuren werden durch weitere Reaktionen aus proteinogenen Aminosäuren synthetisiert.
Im Körper haben sie die unterschiedlichsten Funktionen. Hierbei nur 2 für den Schulalltag interessante Beispiele:
- 3,4-Dihydroxyphenylalanin: entsteht durch Hydroxylierung von Tyrosin;
ist Vorstufe von Melanin (Pigment in Haut und Haaren)
OH O OH
O NH3 OH
O O
NH3
+ OH-
Tyrosin 3,4-Dihydroxyphenylalanin
- -Aminobutyrat: entsteht durch Abspaltung der -Carboxylgruppe von Aspartat; inhibitorischer Neurotransmitter (GABA)
H3N
O NH3 O
O O O
O
- CO2
Glutamat -Aminobutyrat
1.5 Optische Aktivität von Aminosäuren / D- und L-Stereoisomere
Wie man aus der Strukturformel der Aminosäuren erkennen kann, besitzen Aminosäuren am C
2ein Chiralitätszentrum, da alle Aminosäuren am C
2vier unterschiedliche Substituenten besitzen. Ausnahme hierbei ist nur Glycin, wo der Rest R ein Wasserstoffatom ist.
Daher handelt es sonst bei allen übrigen Aminosäuren beim C
2um ein Asymmetrie- bzw.
Chiralitätszentrum. Daher sind die Aminosäuren chiral und können Spiegelisomere /Enantio- mere bilden.
Daher sind Aminosäuren optisch aktiv. Sie können linear polarisiertes Licht drehen. Hierbei
muss man aber beachten, dass die Richtung des Drehwertes in keinem Zusammenhang zur L-
und D-Nomenklatur steht.
1.6 Aminosäuren sind Zwitterionen
Die unter 1.1 angegebene Strukturformel ist nicht ganz korrekt.
Wie bereits erwähnt sind Aminosäure bifunktionell. Aufgrund ihrer Carboxyl- und Aminogruppe sind sie amphoter, d.h. sie können sowohl sauer als auch basisch reagieren. Die Aminogruppe (pK
a=2-5) ist deutlich basischer als die Carboxylatgruppe (pK
a=10-11). Daher ist die COOH-Gruppe in der Lage, durch einen intramolekularen Protonenübergang ihr Proton abzugeben und somit die NH
2-Gruppe zu protonieren. Somit liegen Aminosäuren als zwitterionische Ammoniumcarboxylate vor.
H H
2N
R
O O
H
H H
3N
R
O O
Die stark polare Natur der Zwitterionen macht es möglich, dass Aminosäuren besonders stabile Kristallgitter ausbilden können. Dies erklärt auch, warum sich die meisten Aminosäuren im Wasser sehr schlecht lösen und auch generell einen sehr hohen Schmelzpunkt haben.
In wässriger Lösung bilden sich unterschiedliche Säure-Base-Gleichgewichte unter Beteiligung der funktionellen Gruppe. Das bedeutet, dass bei Veränderung des pH-Wertes das bei pH 7 vorliegende Zwitterion deprotoniert oder protoniert wird. Dadurch liegt es nicht mehr in Zwitterionenform vor, sondern in einer Monoionenform – entweder Monokation oder Monoanion. Diese Struktur ist nicht in der Lage eine stabile Kristallstruktur auszubilden; sie löst sich im wässsrigen.
Bsp.: Glycin
H
3N R COOH H
H
3N
COO H
R H
2N
H R
COO
Monokation:
überwiegt bei pH< 1
Zwitterion:
überwiegt bei pH = 6
Monoanion:
überwiegt bei pH > 13
+ OH- + OH-
+ H+ + H+
Beim sogenannten Isoelektrischen Punkt (IEP) ist – laut Definition - die Konzentration der Monoanionen gleich der Konzentration der Monokationen. Kurz: Alle Aminosäuren liegen in Zwitterionen-Form vor.
Da beim Isoelektrischen Feld alle Ladungen neutralisiert sind, ist keine Wanderung der Aminosäuren in einem von außen angelegten elektrischen Feld sichtbar.
Der Isoelektrische Punkt kann berechnet werden. Er ist der Mittelwert der beiden pK
a-Werte der Aminosäure.
IEP = (pK
COOH+ pK
NH2)/2
Die Berechnung des IEP ist komplizierter, wenn auch die Seitenkette der Aminosäure basische oder saure Funktion haben.
Hierbei werden die pK
afunktionellen Gruppen berücksichtigt, die für die Ausbildung der Zwitterionen-Form relevant ist.
Versuch 2: Löslichkeit von Tyrosin
Geräte: Demoreagenzglas, Reagenzglashalter, Pipetten, Pipettenhütchen
Chemikalien: Tyrosin, ention. Wasser, Natronlauge (c(NaOH) = 1 mol/L), Salzsäure (c(HCl) = 1 mol/L)
Durchführung: Man suspendiert in dem Reagenzglas ca. 0,15 g Tyrosin in ca. 40 mL Wasser. Anschließend gibt man unter Rühren tropfenweise Natronlauge hinzu, bis die Lösung völlig klar ist. Dann versetzt man die Lösung mit einigen Tropfen Phenolphthalein und anschließend abermals tropfenweise mit Salzsäure, bis die Lösung wieder trübe erscheint.
Dann werden noch ein bis zwei Tropfen Salzsäure hinzugegeben.
Beobachtung: Zu Beginn ist die Lösung trübe. Nach Natronlaugen-Zugabe wird sie
klar. Gibt man bis ca. zum Äquivalenzpunkt Salzsäure hinzu, wird die
Lösung wieder trüb. Werden dann noch weitere Tropfen Salzsäure
hinzugegeben, wird die Lösung wieder klar.
Auswertung: Im Neutralen liegt Tyrosin in Zwitterionen-Form vor und ist somit kaum wasserlöslich. Durch Zugabe von Natronlauge wird die NH
3+- Gruppe (ab pH 9 auch die OH-Gruppe) deprotoniert und es entsteht ein wasserlösliches Anion.
Durch Zugabe von Salzsäure findet eine Protonierung statt, wobei Tyrosin am IEP als Zwitterion ausfällt. Bei weiterer Salzsäurezugabe wird die COO
--Gruppe protoniert. Das entstehende Kation geht in Lösung.
OH H3N
HO O
OH / H2O H
OH H3N
O O
OH / H2O H
OH H2N
O O
OH / H2O H
O H2N
O O
Monokation ladungsneutralisiertes
Zwitterion Monoanion Dianion
2,2
9,1
10,1
pKa = 2,2 pKa = 9,1 pKa = 10,1
Da – wie schon erwähnt – Aminosäuren in unserem Körper Baustein für viele Makromoleküle sind, werden Aminosäuren auch oft sogenannten leistungssteigernden Nahrungsergänzungsmitteln und Aufbaupräparaten beigegeben. Die Konsumenten solcher Produkte hoffen, dass sie somit die Proteinsynthese und dadurch den Muskelaufbau beschleunigen bzw. den Muskelabbau verlangsamen können.
Ob nun wirklich Aminosäuren in den Power-Riegeln oder Pulver sind, kann mit folgendem
Versuch überprüft werden:
Versuch 3: Nachweis von -Aminosäuren in Aufbaupräparaten mit Ninhydrin
Geräte: zwei Reagenzgläaser, Reagenzglasständer, Reagenzglasklammer, Wasserbad
Chemikalien: wässrige Lösung von Gly und Aufbaupräparat, Ninhydrin-Reagenz Durchführung: Man füllt jeweils 5 mL der wässrigen Lösungen in ein Reagenzglas,
versetzt diese mit 10 Tropfen Ninhydrin-Reagenz und erwärmt diese im Wasserbad.
Beobachtung: Bei der Gly-Lösung zeigt sich nach einiger Zeit eine tiefe, blauviolette Farbe, bei der Aufbaupräparate-Lösung eine leicht violette bis rosa Farbe.
Auswertung: -Aminosäuren gehen mit Ninhydrin-Lösung Farbreaktionen ein, wobei fast alle Aminosäuren eine blau- bis rotviolette Farbe zeigen.
Die dezentere Farbe bei den Aufbaupräparaten kommt durch die
geringere Aminosäure-Konzentration zustande.
O O O
+
H3N
O O R
N O
O O O
O O O
O
O OH OH + H2O
- H2O
Indan-1,2,3-trion
O O O
+
H2NCOOH H
R
O
O OH NH
H R HO O
Halbaminol
O
O OH NH
H R
HO O - H2O
- CO2 O
O H N
H R
O
OH N
H R
Keto-Enol-Tautomerie
O
OH N
H R
O
OH
NH2
+
R H O
Aminoketon Aldehyd Ruhemanns Purpur
+
-O
OH NH2
O O
O
+
O
O N
O
O
O
O N
O
O
O N
O
O O
Ruhemanns Purpur
+
-2. Von der Aminosäure zum Protein – Proteinbiosynthese
Wie bereits erwähnt werden Proteine aus Aminosäuren gebildet. Dies geschieht im Organismus während der Proteinbiosynthese.
Die Proteinbiosynthese unterteilt sich in Transkription und Translation.
Die Transkription findet im Zellkern statt. Dabei wird die in der Basenfolge der DNA enthaltene Information auf die mRNA übertragen. Die mRNA gelangt durch eine Kernpore ins Cytoplasma.
Im Cytoplasma findet die Translation statt. An eine tRNA wird eine spezifische Aminosäure gebunden. Die beiden Untereinheiten eines Ribosoms binden an die mRNA und setzen sich zum funktionsfähigen Ribosom zusammen. Die tRNA setzt sich jeweils komplementär an die mRNA. Die von der tRNA mitgebrachten Aminosäuren werden am Ribosom enzymatisch zu einer Polypeptidkette verknüpft.
Zum Schluss (beim Stoppcodon) löst sich das fertige Polypeptid von dem Ribosom und bildet seine endgültige Struktur aus.
Abb. 5: Proteinbiosynthese (Quelle: Internet www2.chemie.uni-erlangen.de)
3. Proteine
3.1 Peptidbindung
Peptidbindungen verknüpfen Aminosäuren untereinander zu Peptiden. Dies geschieht durch eine Kondensationsreaktion.
H2N R H
COOH H2N R H
+
COOH- H
2O
H2N O
NH O
OH R
R
Wichtiges zur Struktur der Peptidbindung:
- Peptidbindung weist bei Raumtemperatur keine freie Drehbarkeit auf - planar aufgrund der Delokalisierung des freien Elektronenpaares
HN O
NH O R
R H
N N
H O
R
R O
- fast immer: NH-Wasserstoffatom trans zum Carbonylsauerstoff
- Rotaton um CN-Bindung ist wegen partiellen Doppelbindungscharakters langsam (aufgrund Bindungslänge zwischen C und N)
- die den Amidfunktionen benachbarten Bindungen sind frei rotierbar
Polypeptide sind relativ starr, aber beweglich genug, um verschiedene Konformationen einzugehen.
3.2
Definition Proteine
Proteine sind Makromoleküle, die aus durch Peptidbindungen verknüpfte Aminosäuren aufgebaut sind. Dabei spricht man erst von Proteinen, wenn mehr als 100 Aminosäuren miteinander verknüpft sind. (1 – 9 Aminosäuren: Oligopeptide; 10 – 99 Aminosäuren:
Polypeptide).
Protein kommt vom griech Wort (proteuo), was bedeutet „ich nehme den ersten
Platz ein“. Dies beschreibt sehr gut die Bedeutung von Proteinen in Organismen, wie auch im
folgenden erläutert wird.
3.3
Vorkommen und Funktion von Proteinen
Jeder Organismus enthält Tausende verschiedene Proteine mit unterschiedlichen Aufgaben.
Hier nur ein kurzer Überblick über die am weitesten verbreiteten Proteinfunktionen:
Strukturbildung und –erhaltung
Die Strukturproteine sind für Form und Stabilität der Zellen und Gewebe verantwortlich. Als wichtige Beispiele sind Collagen und Histone zu nennen. Histone organisieren die Anordnung der DNA im Chromatin, indem die Grundbausteine des Chromatins, die Nucleosomen, aus einem oktameren Komplex von Histonen bestehen, um den die DANN gewunden ist.
Transport
Ionenkanäle/Carrier bestehen aus integralen Membranproteinen. Sie vermitteln den Transport von Ionen und anderen niedermolekularen Verbindungen durch biologische Membranen.
Es gibt aber auch spezielle Transportproteine, wie z.B. das Hämoglobin, das für den Transport von Sauerstoff und Kohlendioxid zwischen den Lungen und den Geweben verantwortlich ist.
Schutz und Abwehr
Das aus Proteinen bestehende Immunglobulin G ist ein wichtiger Bestandteil unseres Immunsystems, das den Organismus vor Krankheitserregern und körperfremde Substanzen schützt.
Steuerung und Regelung
Auch Hormone und Hormonrezeptoren bestehen aus Proteinen. Sie haben somit in biochemischen Signalketten eine große Bedeutung.
Katalyse
Die zahlenmäßig größte Gruppe von Proteinen mit über 2000 Vertretern bilden die
Enzyme.
Bewegung
Muskelfasern bestehen – vereinfacht – aus Actin und Myosin, was wiederum Proteine sind. Das Zusammenspiel von Actin und Myosin ist für die Muskelkontraktion, aber auch für andere Bewegungsabläufe verantwortlich.
Speicherung
In Pflanzen gibt es sogenannte Speicherproteine, die auch für die menschliche Ernährung wichtig sind. Aber auch im tierischen Organismus gibt es Speicherproteine;
diese Muskelproteine stellen im Notfall eine mobilisierbare Nährstoffreserve dar.
3.4
Strukturgebung
Wie schon erwähnt, wird bei der Proteinbiosynthese nur eine Polypeptidkette ohne spezifische Struktur synthetisiert. Aber damit die Proteine ihre unterschiedliche Funktion wahrnehmen können, müssen sie eine bestimmte Form bekommen. Denn auch wenn Autos aus Blech bestehen, ein Blechstück erfüllt noch lange nicht die Funktion eines Autos.
Änalog der Autoherstellung müssen auch noch Proteine ihre spezifische Struktur bekommen, um letzendlich ihre Funktion zu haben.
Diese Strukturgebung erfolgt in mehreren Abschnitten:
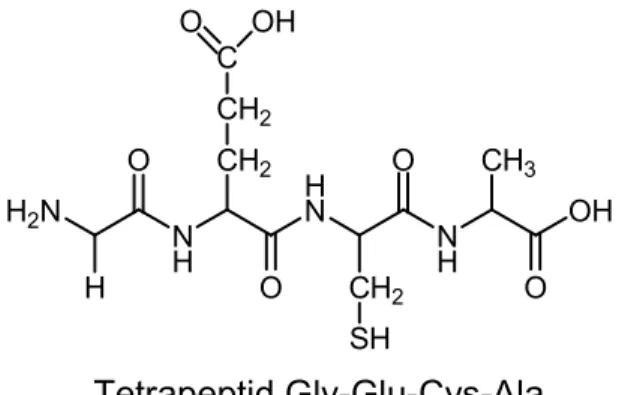
Primärstruktur
Die Primärstruktur stellt nur die Abfolge der Aminosäuresequenz, aber nicht die Struktur der Polypeptidkette dar.
H2N
NH O
H
CH2 CH2 C O OH
HN O
NH
OH O
O CH2
SH
CH3
Tetrapeptid Gly-Glu-Cys-Ala
Abb. 6: Primärstruktur (eigener Entwurf)
Bei der Schreibweise muss beachtet werden, dass das N-terminale Ende links und das C-terminale Ende rechts steht.
Sekundärstruktur
Die Sekundärstruktur gibt mögliche Faltungsmuster wider.
Die Sekundärstruktur kommt teilweise durch Disulfidbrücken, hauptsächlich jedoch aufgrund der Starrheit der Amidbindung und der Maximierung der Wasserstoffbrücken zwischen den Peptidbindungen des Polypeptids zustande.
Hierbei muss zwischen intra- und intermolekularen Wasserstoffbrücken unterschieden werden.
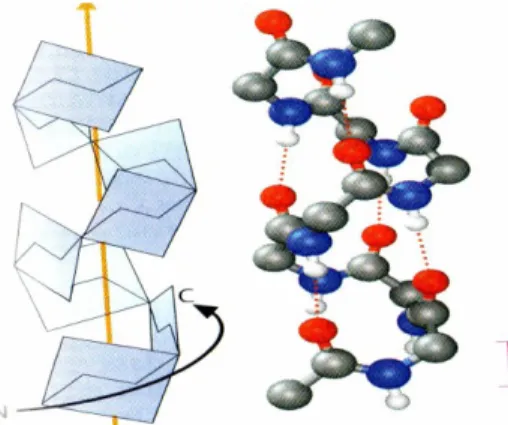
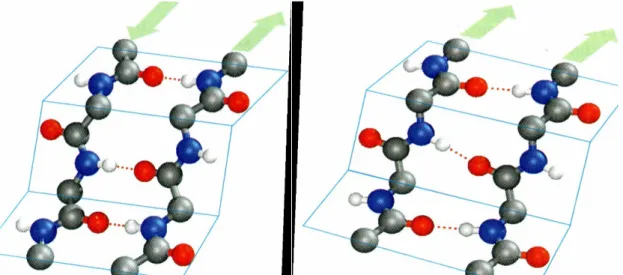
Durch intramolekulare Wasserstoffbrückenbindungen bildet sich die meist rechtsgängige -Helix. Diese hat eine Ganghöhe von 0,54 nm und 3,6 Aminosäuren pro Windung. Wie auch der Grafik zu entnehmen ist, sind die Wasserstoffbrücken nahezu linear und parallel zur Drehachse des sich bildenden Hohlzylinders angeordnet.
Beispielsweise hat das Protein Keratin die Sekundärstruktur -Helix.
Durch intermolekulare Wasserstoffbrücken kommt die -Faltblattstruktur zustande.
Dabei sind zwei Polypeptidketten so angeordnet, dass jeweils die Aminogruppe einer Peptidbindung gegenüber der Carbonylgruppe einer anderen liegt, so dass sich zwischen beiden Gruppen Wasserstoffbrücken ausbilden können.
Abb. 7: -Helix ( nach KOOLMAN / RÖHM, Taschenatlas der Biochemie)
Tertiärstruktur
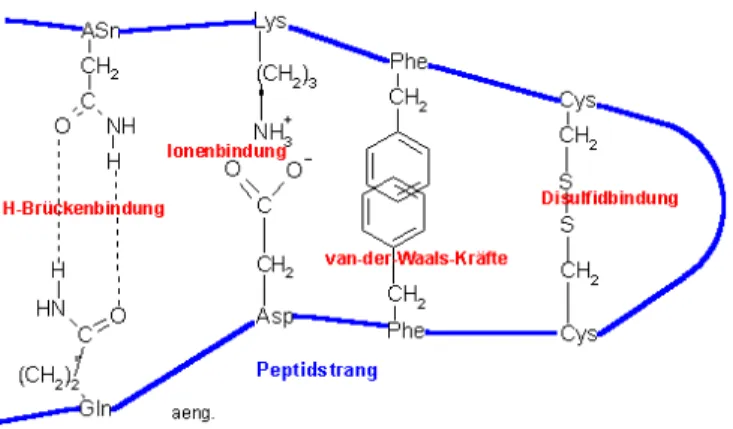
Unter der Tertiärstruktur versteht man die spezifische räumliche Anordnung der helicalen bzw. der zickzackgefalteten Peptidkette, bedingt durch Bindungen oder Wechselwirkungen zwischen den Seitenketten.
Hierbei gibt es mehrere Bindungen bzw. Wechselwirkungen:
- Wasserstoffbrückenbindungen: zwischen polaren Aminosäuren
(Serin, Threonin, Asparagin, Glutamin) - Ionenbindungen: zwischen sauren und basischen Aminosäuren
(Aspartat, Glutamat, Histidin, Lysin, Arginin) - Van-der-Waals: zwischen unpolaren, aliphatischen Aminosäuren
(Glycin, Alanin, Valin, Leucin, Isoleucin) - -stacking : zwischen aromatischen Aminosäuren
(Phenylalanin, Tyrosin, Tryptophan) - Disulfidbrücken: zwischen Cystein
Abb. 8: Faltblattstruktur (antiparallel und parallel) (nach KOOLMAN / RÖHM; Taschenatlas der Biochemie)
Quartärstruktur
Die Quartärstruktur ist die Endform eines Proteinkomplexes. Mehrere tertiär strukturierte Polypeptidketten lagern sich zusammen.
Bsp.: Hämoglobin
PRINZIP: FORM FOLLOWS FUNCTION!!!
Mit dem Wissen über den Aufbau und Struktur der Proteine lassen sich die im folgenden erläuterten Versuche gut verstehen.
Hierbei habe ich zwei klassische Proteinnachweise – nämlich „Xanthoprotein-Reaktion“ und
„Biuret-Reaktion“ - gewählt, da diese auch in der Schule beim Themenkomplex „Proteine“
Abb. 9: Tertiärstruktur (Quelle: Internet)
Abb. 10: Hämoglobin (Quelle: Internet www.nurseminerva.co.uk)
In einem weiteren Versuch soll auch die Wirkweise von ACC
200 Kapseln gezeigt werden.
Fast jeder hat dieses oder ein auf dessen Wirkbasis beruhendes Medikament bei Erkältungen zu sich genommen. Daher ist es bestimmt auch für Schüler interessant, die Wirkweise in vereinfachter Form nachzuvollziehen und am Modell „Eiklar“ zu testen.
Versuch / Demo 1: Schleimlösende Wirkung von Acetylcystein
Geräte: 2 Vollpipetten (10 mL), 3 Messpipette (25 mL), Messzylinder (100 mL), Peleusball,, Erlenmeyerkolben (250 mL), Stoppuhr, 3 Bechergläser (50 mL), 2 Erlenmeyerkolben (100 mL), 2 Trichter, Glaswolle, Faltenfilter, Magnetrührer mit Rührfische, Stativmaterial Chemikalien: Puffer pH=6,8, ACC
200 Kapseln, Eiweiß
Herstellung des Puffers:
Zur Herstellung des Puffers mischt man 500 mL Kaliumdihydrogenphsphat-Lösung ((KH
2PO
4)=9,078 g/L) mit 426 mL Natriumhydrogenphosphat-Lösung ((Na
2HPO
4 12 H
2O)=23,896 g/L)
Durchführung: Der Inhalt von vier ACC
200 Kapseln wird zu 100 mL Puffer gegeben Und ca. 1 Minuten gerührt; wenn nötig, werden ungelöste Hilfsstoffe abfiltriert.
In zwei Bechergläser werden je 15 mL Eiweiß mit 15 mL Puffer bzw.
15 mL Acetylcystein-Lösung versetzt und für 30 Minuten gerührt.
Um gröbere Partikel aus den Mischungen zu entfernen, filtriert man durch einen lockeren Glaswollebausch.
Anschließend kässt man jede Lösung durch eine Messpipette fließen und stoppt dabei die Zeit, die die Lösungen benötigen, um von der 0 mL-Marke bis zur 20 mL-Marke der Messpipette zu fließen.
Beobachtung. Die mit Acetylcystein vesetzte Lösung fließt schneller. Sie ist auch
klarer.
Auswertung: Das Acetylcystein spaltet reduktiv die Disulfidbrücken der im Eiweiß enthaltenen Glykoproteine.
Durch Spaltung der Brücken wird die Viskosität der Proteinlösung herabgesetzt. Daher fließt es schneller aus der Messpipette.
OH
N-Acetylcystein
OH O
NH CO CH3 HO S
O
NH H3C CO
S S H2
2
H2 C C
HS H2 C H2
C
+
+
Peptidstrang SH S
O HS
HN CO CH3
Versuch 4: Die Xanthoprotein-Reaktion
Geräte: Becherglas (500 mL), Reagenzgläser, Reagenzglasständer, Reagenzglasklammer, Pipette, Pipettenhütchen
Chemikalien: Hühnereiweiß, isotonische Kochsalzlösung (0,9%ig), konzentrierte Salpetersäure
Durchführung: Zuerst wird eine Eiweißlösung hergestellt, indem ein Hühnereiweiß in ca. 250 mL isotonischer Kochsalzlösung dispergiert wird.
Ein Reagenzglas wird bis zur Hälfte mit der Eiweißlösung gefüllt;
anschließend werden eineige Tropfen konzentrierte Salpetersäure hinzugegeben.
Beobachtung: Zuerst bildet sich ein weißlicher flockiger Niederschlag, der sich relativ schnell gelb wird.
Auswertung: Die Aminosäuren Phenylalanin und Tyrosin besitzen Phenylreste. Diese aromatischen Systeme können durch konzentrierte Salpetersäure nitriert werde. Die entstandenen Nitroderivate sind intensiv gelb.
3 HNO
3NO
2++ 2 NO
3-+ H
3O
+R
+ NO
2+H
R
H O2N
R
NO2 - H+
Bei der Xanthoprotein-Reaktion handelt es sich um eine Nitrierungs- Reaktion eines monosubstituierten Aromaten (elektrophile aromatische Substitution).
Als Elektrophil fungiert das Nitronium-Ion NO
2+.
Der Erstsubstituent (Peptidkette) dirigiert in para-Stellung.
Durch die Wechselwirkungen der -Elektonen des Aromaten mit dem Nitronium-Ion entsteht ein -Komplex.
Nach der Bildung des -Komplexes bildet sich im geschwindigkeits- bestimmenden Schritt der -Komplex aus.
Anschließend kommt es durch Deprotonierung zur Rearomatisierung.
Versuch 5: Die Biuret-Reaktion
Geräte: Reagenzglas, Reagenzglasständer, Pipetten, Pipettenhütchen Chemikalien: Eiweiß, isotonische Kochsalzlösung (0,9%ig),
Natronlauge (c(NaOH) = 1 mol/L), Kupfersulfat-Lösung (c(CuSO
4) = 1 mol/l)
Durchführung: Zuerst wird eine Eiweißlösung hergestellt, indem ein Hühnereiweiß in ca. 250 mL isotonischer Kochsalzlösung dispergiert wird.
In das Reagenzglas wird ca. 2 mL Eiweiß-Lösung gegeben und auf ca. 5 ml mit ention. Wasser aufgefüllt. Anschließend werden 5 Tropfen Natronlauge hinzugegeben, das Reagenzglas geschüttelt und zum Schluss vorsichtig 5 Tropfen Kupfersulfat-Lösung hinzugegeben.
Beobachtung: Es bildet sich ein blauer Niederschlag, der nach kurzer Zeit nach violett umschlägt.
Auswertung: Durch Zugabe von Natronlauge wird die NH-Gruppe in der Peptidbindung deprotoniert. Mit den Cu
2+-Ionen bildet sich ein verzerrt oktaedrischer, violetter Komplex. Das Cu
2+-Ion wird von insgesamt 4 Peptidbindungen komplexiert. Daher tritt dies Biuret-Reaktion frühestens bei Tripeptiden auf.
HN
NH O
R O
R O
2 + [Cu(H2O)6]2++ 2 OH Cu
N
HN R O
O
R
O
NH
N O R
R
O
R H2O
H2O
+ 8 H2O
Auch bei dem folgenden Demonstrationsversuch wird auf eine Problematik der Alltagswelt der Schüler eingegangen. Was soll man machen, wenn bei einer Rauferei mit den Nachbarskindern die Nase geblutet hat und das Lieblings-T-Shirt beschmutzt hat? Wie kriegt man den Fleck raus, ohne dass die Mutter es bemerkt und lästige Fragen stellt?
Demo 2: Auswaschen eines Blutflecks
Geräte: 2 Kristallisierschalen, Pipetten, Pipettenhütchen
Chemikalien: heißes Wasser, kaltes Wasser, Schweineblut, 2 Stofffetzen
Durchführung: Man gibt je 3 Tropfen Schweineblut auf die Stofffetzen. Diese werden jeweils in eine Kristallisierschale gegeben. In die eine Kristallisierschale wird kaltes, in die andere heißes Wasser gegossen.
Beobachtung: Beim mit heißem Wasser übergossenen Stofffetzen ist der Blutfleck weiterhin sichtbar. Im kalten Wasser lässt sich der Blutfleck rauswaschen.
Auswertung: Durch das heiße Wasser werden die Blutproteine denaturiert. Sie
verklumpen und setzen sich in die Textilfasern fest. Daher kann der
Blutfleck nur schwer ausgewaschen werden.
3.5
Isolierung, Reinigung und Analyse von Proteinen
Proteine werden in Forschung, Medizin und Biotechnologie für eine Vielzahl von Verwendungen benötigt. Dabei müssen sie gereinigt und oft analysiert vorliegen. Da einige Proteine – wie z.B. die globulären Proteine – sehr labil sind, wird oft in einem den Proteinen angemessenen Temperaturbereich gearbeitet.
Im folgenden werden die gängigsten Verfahren erläutert:
Salzfällung
Die Löslichkeit von Proteinen ist stark von der Salzkonzentration (Ionenstärke) des des Mediums abhängig. Wie auch in einem späteren Versuch gezeigt wird, sind Proteine in reinem Wasser schlecht löslich. Mit zunehmender Salzkonzentration erhöht sich die Proteinlöslichkeit, da die gut hydratisierten Salzionen an der Proteinoberfläche gebunden werden und dadurch die Aggregation der Moleküle verhindern. Diesen Vorgang nennt man „Einsalzen“. Bei einer sehr hohen Salzkonzentration uns somit hoher Ionenstärke kann das Salz den Proteinen auch die Hydrathülle entziehen, wodurch es zur Aggregation und Ausfällen der Proteinmoleküle kommt. Diesen Vorgang nennt man analog „Aussalzen“.
Durch dieses Verhalten kann man Proteingemische nach dem unterschiedlichen Löslichkeitsverhalten der einzelnen Proteine fraktioniert auftrennen.
Bei Salzfällungen wird oft das Salz Ammoniumsulfat (NH
4)
2SO
4verwendet.
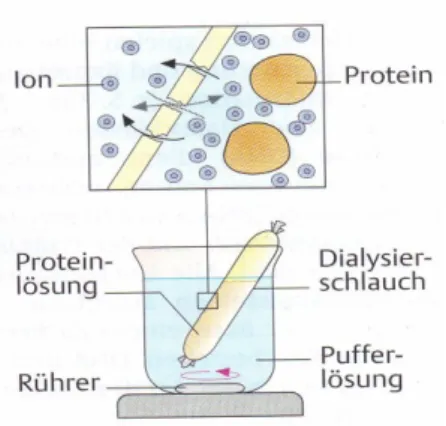
Dialyse
Die Dialyse ist ein klassisches Reinigungsverfahren. Diese wird zur Entfernung niedermolekularer Bestandteile verwendet.
Dazu gibt man die zu reinigende proteinhaltige Lösung in einen Dialysierschlauch (semipermeable Membran). Die Proteine (Makromoleküle) können im Gegensatz zu den niedermolekularen Substanzen (z.B. bestimmte Salze) nicht die semipermeable Membran passieren. Nach einiger Zeit ist dann die Konzentration der niedermolekularen Substanzen im Außenmedium gleich dem Innenmedium im Dialysierschlauch.
Daher hat erst nach mehrfachem Wechseln des Außenmediums das Innenmedium die
gewünschte Reinheit.
Gelfiltration
Mithilfe der Gelpermeationschromatographie – kurz: Gelfiltration – werden Proteine nach Größe und Form aufgetrennt. Dazu wird eine Chromatographiesäule verwendet, die mit kugelförmigen Gelpartikeln (Durchmesser: 10 – 500 m) aus polymerem Material gefüllt ist. Die Partikel sind zusätzlich mit Kanälen von definiertem Durchmesser durchzogen.
Zur Proteintrennung wird das Proteingemisch am oberen Ende der Säule aufgetragen und eluiert. Die großen Proteine können nicht in die Kanälchen der Partikel gelangen und bewegen sich so schnell durch die Säule. Die mittelgroßen bis kleinen Proteine müssen den Umweg über die Kanälchen gehen und benötigen somit mehr Zeit für das Passieren der Säule. Am Säulenende können die Proteine abgefangen werden. Da die Proteine aufgrund ihrer Größe eine unterschiedliche Durchlaufzeit haben – die größten am schnellsten, die kleinsten am langsamsten – kann das Proteingemisch getrennt werden.
Abb. 11: Dialyse ( nach KOOLMAN / RÖHM; Taschenatlas der Biochemie)
Abb. 12: Gelfiltration (nach KOOLMAN / RÖHM; Taschenatlas der Biochemie)
SDS-Gelelektrophorese
Die SDS-Gelelektrophorese ist die gebräuchlichste und am weitesten verbreitete Methode zur Reinigung und Analyse von Proteinen. Eine genauere Versuchsanleitung folgt bei Demo/Versuch Proteinfingerabdruck.
Bei einer allgemeinen Elektrophorese werden Moleküle in einem elektrischen Feld aufgetrennt. Dabei ist die Wanderungsgeschwindigkeit abhängig von der Größe, der Form und der elektrischen Ladung der Moleküle.
Bei der SDS-Gelelektrophorese werden die zu untersuchenden Proteine so vorbehandelt, das nur noch ihre Masse für die Wanderungsgeschwindigkeit von Bedeutung ist.
Durch Zugabe von Natrium-Laurylsulfat (C
12-H
25-OSO
3Na ; engl.: sodium dodecyl sulfate SDS) werden die oligomeren Proteine in ihre Untereinheiten zerlegt und denaturiert. An die entfalteten Peptidketten binden SDS-Moleküle und verleihen ihnen eine stark negative Ladung. Damit die Proteine vollständig entfaltet werden, werden Thiole zur reduktiven Spaltung der Disulfidbrücken hinzugegeben.
Die anschließende Elektrophorese verläuft wie jede andere auch. Die Proben werden in die jeweilige Probentasche im Polyacrylamid-Gel aufgetragen. Anschließend wird die Apparatur verschlossen und eine Spannung angelegt. Die Moleküle wandern in Richtung Anode (-Pol).
Nach der vollständigen Auftrennng werden die getrennten Proteine durch Färbung sichtbar gemacht und mit einer bereits angelegten Tabelle von bekannten Proteinen verglichen.
Die SDS-Gelelektrophorese hat auch einen guten Alltagsbezug.
Mit dieser Methode kann beispielsweise genau bestimmt werden, aus welcher Fleischsorte die Wurst besteht. Dies hat einen
Bezug zur aktuellen
Gammelfleischdebatte.
Abb. 13: SDS-Gelelektrophorese (nach KOOLMAN / RÖHM; Taschenatlas der Biochemie)
Demo 3: Proteinfingerabdruck
Geräte: Thermoblock, Stoppuhr, Elektrophoreseapparatur, Gel-Gießstand, Gilsonpipetten, Hamiltonpipette, Schutzhandschuhe
Chemikalien: SDS (Sodiumdodecylsulfat), -Mercaptoethanol, Bromphenolblau, dest. Wasser, Isopropanol, Coomassie-Färbelösung, Coomassie- Entfärbelösung
Durchführung: Herstellung der verschiedenen Proteinproben:
Es werden verschiedene Fisch- und Fleischarten bereitgestellt.
Zu jeder Fleischprobe (im Eppendorf-Gefäß) werden 500 L Laemmli Sample Buffer + ME gegeben. Anschließend werden die Eppendorf- Gefäße 10 Minuten bei 95°C im Thermoblock inkubiert.
Anschließend werden die Proben 1 Minute in der Zentrifuge bei 6000 rpm zentrifugiert.
Der Überstand mit dem denaturierten Proteingemisch wird für die Gel- Elektrophorese weiterverwendet. Bei Bedarf können die Proben auch eingefroren werden.
Probenauftrag:
Die Probenauftragshilfe wird auf die Apparatur aufgesteckt.
Die aufbereiteten Proben werden vorsichtig in die Geltaschen aufgetragen.
Hierbei empfiehlt es sich, vorher die optimale Menge (Bsp. 5 L oder 10 L) zu ermitteln. Desweiteren muss die Reihenfolge der Probenauftragung protokolliert werden.
Abb. 14: Elektrophoresekammer (Quelle: Internet www1.hs-bremerhaven.de)
Nach dem Probenauftrag werden die Probenauftragshilfen entfernt. Der Deckel wird auf den Pufferbehälter aufgesetzt und an das Spannungsgerät angeschlossen. Die Elektrophorese wird 45 – 60 Minuten bei 200 V durchgeführt.
Man schaltet die Elektrophorese ab, wenn die blaue Bromphenolblau- Bande am unteren Gelrand angelangt ist.
Coomassie-Färbelösung:
Man nimmt die Bestandteile der Apparatur in umgekehrter Reihenfolge wieder auseinander, bis man die Gelkassette mit dem SDS-Gel vor sich liegen hat. Das von der Apparatur gelöste Gel wird in ca. 100 mL Coomassie-Lösung gegeben und in der Mikrowelle bei 80°C für ca. 20 Minuten unter ständigem Schwenken gefärbt.
Coomassie-Entfärbelösung:
Die Färbelösung wird abgegossen und das Gel mit ca. 100 mL Entfärber erneut in der Mikrowelle erwärmt. Man erkennt nach ca. 45 Minuten das Bandenmuster, wenn man das Gel auf einen Leuchttisch legt.
Auswertung des fertigen Gels:
Abb. 15: fertiges Gel (eigene Herstellung)
3.6
Löslichkeitsverhalten von Proteine
Ein weiterer interessanter Aspekt ist das Löslichkeitsverhalten von Proteinen. Proteine behalten im neutralen, wässrigen Milieu ihre Struktur. Dass sie – die hochmolekularen Proteine – sich nicht wieder in die niedermolekularen Aminosäuren zerlegen, kann man mithilfe des unten genannten Versuches zeigen.
Versuch 6: Tyndall-Effekt einer Eiklar-Lösung
Geräte: Glaswolle, Glastrichter, Magnetrührer mit Rührfisch, Becherglas (500 mL), zwei Demo-Reagenzgläser, Reagenzglasständer, Taschenlampe
Chemikalien: Eiklar, isotonische Kochsalzlösung (0,9 %), Leitungswasser
Durchführung: Ein Hühnereiweiß wird in 200 mL isotonischer Kochsalzlösung suspendiert. Und anschließend wird die Lösung durch Glaswolle filtriert.
In ein Reagenzglas wird die Eiklar-Lösung gefüllt; in das andere nur Wasser.
In einem abgedunkelten Raum hält man zuerst den Lichtstrahl der Taschenlampe an das Reagenzglas mit der Eiklarlösung, dann an das Reagenzglas mit dem Wasser.
Beobachtung: Bei der Eiklar-Lösung kann man den Lichtstrahl durch die Lösung
hindurchverfolgen. Das Wasser ist optisch leer; das heißt, dass der
Lichtstrahl, der durch das Reagenzglas mit dem Wasser fällt, von der
Seite nicht zu erkennen ist.
Deutung: Die Proteine verlieren nicht ihre Struktur im wässriger Lösung, sondern sie liegen kolloidal in der Lösung vor, weshalb man den Lichtstahl genau verfolgen kann.
Der in der Abb. dargestellte Effekt ist der Tyndall-Effekt. In der Abb.
werden die kolloidal in der Lösung vorliegenden Proteine durch die schwarzen Punkte dargestellt.
Die kolloidal vorliegenden Teilchen müssen einen Durchmesser zwischen 1 und 100 nm haben (dies entspricht der Wellenlänge des Lichts), damit der Lichtstrahl an ihnen gestreut wird.
Abb. 16: Tyndall-Effekt (eigener Entwurf)