Protokoll zum
Experimentalvortrag
über
„Regenerative Kraftstoffe“ (OC)
von
Jan Grosse Austing Zwischenhausen 5 ½ 35037 Marburg jan.austing@web.de Matr.-Nr.: 1517260
zum Vortrag vom 28.06.2007 (SS 07)
- 0 - Hinweis:
Dieses Protokoll stammt von der Seite www.chids.de (Chemie in der Schule).
Dort können unterschiedliche Materialien für den Schulunterricht heruntergeladen werden, unter anderem hunderte von Experimentalvorträgen so wie der vorliegende:
http://www.chids.de/veranstaltungen/uebungen_experimentalvortrag.html
Inhaltsverzeichnis
0. EINLEITUNG 1
1. REGENERATIVE KRAFTSTOFFE 2
1.0. Biodiesel 2
1.0.0 Einleitung 2
1.0.1 Versuche 3
1.0.1.0 Versuch 1: Herstellung von Biodiesel 3
1.0.1.1 Demo 1: Vergleich der Viskositäten 8
1.0.1.2 Demo 2: Verbrennung von Diesel bzw. Biodiesel 9
1.1. Bioethanol 11
1.1.0 Einleitung 11
1.1.1 Versuche 13
1.1.1.0 Versuch 2: Wasserentzug durch Molekularsieb 13
1.1.1.1 Versuch 3: Explosion eines E85-Luftgemisches 16
1.2. BtL-Kraftstoffe 19
1.2.0 Einleitung 19
1.2.1 Versuche 19
1.2.1.0 Versuch 4: Holzvergasung 19
1.2.1.1 Versuch 5: Fischer-Tropsch-Synthese
,23
1.3. weitere, nicht im Vortrag behandelte regenerative Kraftstoffe 35
1.3.0 Wasserstoff 35
1.3.1 Biogas 36
2. SCHULRELEVANZ 36
3. FAZIT 37
3.0 Regenerative Kraftstoffe 37
3.1 Schulrelevanz 41
4. Literaturangaben 43
- 1 -
0. Einleitung
Das Thema „Regenerative Kraftstoffe“ stellt als Unterpunkt des Themenkomplexes
„Regenerative Energien“ ein hochaktuelles und interessantes Gebiet dar, welches sowohl in der Politik als auch in der Alltagswelt der Schüler mittlerweile eine gewisse Relevanz erlangt hat. Der Klimawandel mit der Erderwärmung sowie die steigende CO
2-Konzentration in der Atmosphäre werfen Fragen nach den Ursachen auf, und neben natürlichen Emittenten von Treibhausgasen wie u.a. Vulkanen und Mineralquellen (Hauptanteil des in der Atmosphäre vorhandenen Kohlendioxid
1) werden auch die anthropogenen Einflüsse auf die Kohlendioxid- Konzentration der Atmosphäre diskutiert.
Durch die steigende CO
2-Konzentration wird der Treibhauseffekt der Erde begünstigt, welcher von einigen Klimaforschern für die Erwärmung der Erde als Ursache verantwortlich gemacht wird (andere Forscher führen die Erderwärmung auf natürliche Schwankungen des Erdklimas zurück). Da man allerdings nicht warten möchte, bis der Grund für die Erderwärmung vollständig geklärt ist, werden große Bemühungen angestrengt, um die vom Menschen verursachten CO
2-Emissionen zu senken (man denke an das Kyoto-Protokoll, in dem viele Staaten sich verpflichtet haben, ihren Kohlendioxid-Ausstoß stark zu verringern, und man denke an die in Deutschland gewährten Subventionen für Regenerativen Energien allgemein, sei es die Förderung von Windrädern und Solaranlagen, sei es die steuerliche Vergünstigung von Biodiesel). Da das vom Menschen emittierte Kohlendioxid hauptsächlich auf die Verbrennung von fossilen Stoffen zurückzuführen ist, kommen für die Verringerung der Kohlendioxid-Emissionen im wesentlichen 3 mögliche, miteinander kombinierbare Wege zum Erreichen des Ziels in Betracht: Zunächst wäre da die Effizienz-Steigerung bei der Verbrennung von fossilen Energieträgern (z.B. durch effizientere Motoren in Automobilen oder in auf fossilen Brennstoffen basierenden Kraftwerken). Eine weitere Möglichkeit stellt die Umstellung auf andere Energiequellen als fossile Brennstoffe zur Stromproduktion dar (z.B. die forcierte Nutzung von Atomkraftwerken für die Stromproduktion oder die Verwendung von Wasser-, Wind- oder Solarenergie zur Stromerzeugung, wobei gerade die letzten beiden den Nachteil haben, dass die Speicherung des in Spitzenzeiten erzeugten Stroms gewisse Schwierigkeiten mit sich bringt). Die dritte Möglichkeit besteht darin, fossile Kraftstoffe die zur Erzeugung von mechanischer (Verkehr) bzw. thermischer (Heizung,
1
siehe: http://atlas.umwelt.hessen.de/servlet/Frame/atlas/luft/ek/alle_kohlendioxid/ek_alle_ko_txt.htm (besucht
am 30.08.2007)
Industrie) Energie genutzt werden, durch regenerative Brennstoffe zu ersetzen, welche bei der Verbrennung nur soviel Kohlendioxid freisetzen, wie zuvor aus der Atmosphäre assimiliert wurde.
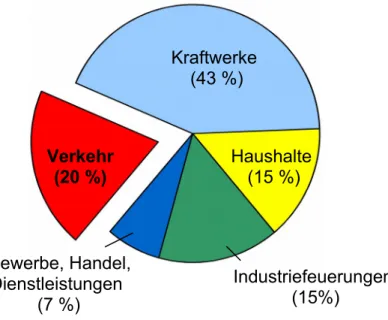
Da in Deutschland im Jahre 2003 in Deutschland der Verkehr einen Anteil von ca. 20 % am gesamten vom Menschen verursachten CO
2-Ausstoß
2hatte, ist die Suche nach alternativen Kraftstoffen für den Verkehrssektor verständlich und sinnvoll.
Diagramm 1: anthropogene CO
2-Emissionen in 2003
2Mein Experimentalvortragsthema beschäftigt sich mit einigen der heute verfügbaren regenerativen Kraftstoffe für die Nutzung in Verbrennungsmotoren.
1. Regenerative Kraftstoffe
1.0. Biodiesel 1.0.0 Einleitung
Biodiesel ist mit 4,7 % Marktanteil
3in 2006 (Marktanteil Biokraftstoffe 2006 gesamt: 5,4 %) der am stärksten verwendete Biokraftstoff in Deutschland. Die Ausgangssubstanz für die Biodiesel-Produktion ist Pflanzenöl, in Deutschland wird zum größten Teil aus Rapssamen gewonnenes Rapsöl verwendet. Das hochviskose Rapsöl ist allerdings für den normalen
2
Daten aus: http://www.umweltbundesamt.de/uba-info-
presse/hintergrund/Trendtabellen_Emissionen_DE_1990_2004_CO2.pdf
3
siehe: http://bambus.tutech.net/energy/Content/download/Lamp_Quoten%20Treibstoffe_rev.pdf (besucht am 30.08.07)
Verkehr (20 %)
Kraftwerke (43 %)
Haushalte (15 %)
Industriefeuerungen (15%)
Gewerbe, Handel, Dienstleistungen
(7 %)
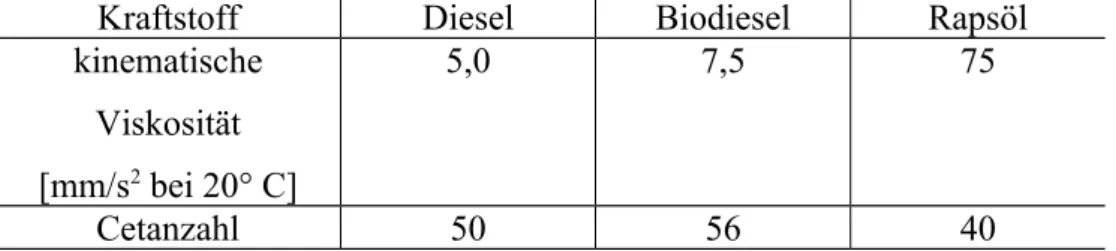
Dieselmotor noch zu zähflüssig (siehe Demo 1 und Tabelle 1) und besitzt einen zu hohen Zündpunkt und eine zu geringe Zündwilligkeit (siehe Tabelle 2). Bei Diesel spricht man von der Cetanzahl zur Charakterisierung der Zündwilligkeit (hohe Cetanzahl = hohe Zündwilligkeit), Referenz sind die Zündwilligkeit von reinem Cetan (C
16H
34) mit der Cetanzahl 100 bzw. α-Methyl-Naphthalin mit der Cetanzahl 0. Die Cetanzahl zur Beschreibung der Zündwilligkeit von Diesel-Kraftstoffen kann mit der Oktanzahl zur Kennzeichnung von Otto-Kraftstoffen verglichen werden, allerdings ist beim Otto-Motor eine Selbstzündung unerwünscht (diese führt zum „Klopfen“ des Motors, daher wird die Oktanzahl auch als Maß für die „Klopffestigkeit“ bezeichnet), im Diesel-Motor ist hingegen die Selbstzündung notwendig.
Kraftstoff Diesel Biodiesel Rapsöl
kinematische Viskosität [mm/s
2bei 20° C]
5,0 7,5 75
Cetanzahl 50 56 40
Tabelle 1: Eigenschaften von Diesel-Kraftstoffen
4Da das Rapsöl aufgrund der hohen Viskostität und der geringen Cetanzahl in seiner ursprünglichen Form nicht in normalen Dieselmotoren zum Einsatz kommen kann, wird das Rapsöl zu Biodiesel verarbeitet (siehe Versuch 1).
1.0.1 Versuche
1.0.1.0 Versuch 1: Herstellung von Biodiesel
5In meinem ersten Versuch wird die Umesterung von Rapsöl zu Biodiesel durchgeführt, nach dem gleichen Prinzip findet auch die industrielle Herstellung statt.
Chemikalien
4
aus: ftp://fnr-server.de/pdf/literatur/pdf_174bd_biokraftstoffe%20august%202005.pdf (besucht am 30.08.07)
5
aus: Chemkon Nr. 3, Jg. 2000, S. 143/144
· Natriumhydroxid NaOH (C; R 35, S 26-36/37/39-45)
· Methanol H
3COH
· (T, F; R 11-23/24/25-39/23/24/25, S 7-16-36/37-45)
· Rapsöl (-) Geräte
· Demoreagenzglas
· Magnetrührer/Rührfisch
· Becherglas (400 mL) als Wasserbad
· Thermometer
· Glasrohr (40 cm)
· Stativmaterial
·
Versuchsaufbau
200 300 400 mL
100
100 80
20 40 60 0
AUS ANLaboBib© U/min
Glasrohr
Thermometer
Demo-Reagenzglas mit Reaktionsgemisch
Wasserbad
Magnetrührer
Durchführung/Beobachtung
Zunächst wird eine Natriummethanolat-Lösung hergestellt, indem man 0,3 g Natriumhydroxid in 100 mL Methanol löst.
Das Becherglas wird zur Hälfte mit Wasser gefüllt und auf 75 ° C erhitzt. In das
Demoreagenzglas werden nun 8 mL der Methanolat-Lösung, 4 mL Rapsöl und der Rührfisch
eingefüllt. Unter Rühren wird die trübe, milchige Emulsion erhitzt, nach ca. 5 Minuten wird das Reaktionsgemisch schlagartig klar.
Für weitere Versuche kann das Reaktionsgemisch ohne Abkühlen nun in ein zu ¾ mit Wasser gefülltes Reagenzglas gegeben werden, nach der Phasenbildung kann die obere Phase (Rapsölmethylester) abpipettiert und für weitere Untersuchungen verwendet werden.
Auswertung/Hintergründe
Durch eine Umesterungsreaktion erhält man aus Rapsöl Biodiesel.
Dabei werden die Triglyceride, aus welchen das Rapsöl hauptsächlich besteht, mit Methanol in die entsprechenden Methylester umgewandelt. Die dabei entstehenden Rapsölmethylester (kurz: RME) nennt man Biodiesel, sie weisen die gewünschten Treibstoffeigenschaften für die Verwendung in Dieselmotoren auf.
Rapsöl besteht zum größten Teil aus Triglyceriden,
die hauptsächlich veresterten Fettsäuren sind Ölsäure (C
18:1; 50-65 %, s.o.),
Linolsäure (C
18:2; 15-30 %) und
Linolensäure (C
18:3; 5-13 %):
Die Umesterung der Triglyceride kann durch folgende Reaktionsgleichung beschrieben werden (R
1, R
2und R
3sind Fettsäurereste der oben genannten Fettsäuren):
Ölsäuretriglycerid
CH3 O
CH3
O CH3
O O
O O
O O
H CH3
Linolsäure
O O
H CH3
Linolensäure
Der Katalysator Methanolat wird dabei aus Natronlauge und Methanol dargestellt:
Mechanistisch kann man die Umesterung wie folgt verstehen:
+ 3 H
3C OH
CH
3Kat.: O
O R
2O
C H
3OH
OH
OH
O R
1O
C H
3+ + +
Triglycerid Methanol Glycerin Rapsölmethylester (RME) R
3O R
2O R
1O O
O O
O R
3O
C H
3NaOH + H
3C OH Na
++ H
3C O
-+ H
2O
O
O O
R
1R
3R
2O
O
O
+
CH
3O
R
3O
O O
R
1O
R
2O
O
O CH
3R
3O O
CH
3+
O
O O
R
1R
2O O
O
O O
R
1R
2O O
+ O CH
3H H O
O O
R
1R
2O O +
O H
O O
R
1R
2O O
+ 2 H
3C OH ; Kat: O CH
3R
2O
O CH
3OH
OH OH
R
1O O CH
3+ +
CH
3O
Die Trübung des Reaktionsgemisches ist durch die Unlöslichkeit von Rapsöl in Methanol sowohl bei Raumtemperatur als auch bei 75 ° C bedingt. Die Entstehung einer klaren Lösung nach ca. 5 Minuten Reaktionszeit ist dadurch zu begründen, dass die entstanden
Rapsölmethylester sowie das Glycerin im Gegensatz zu den Triglyceriden in der Hitze in Methanol löslich sind. Gibt man den Reagenzglasinhalt nun in ein mit Wasser gefülltes Reagenzglas, so löst sich das überschüssige Methanol sowie das Glycerin in der wässrigen Phase, darüber befindet sich die Methylester-Phase.
Industriell wird Biodiesel nach dem gleichen chemischen Prinzip hergestellt, allerdings wird, um eine bessere Ausbeute zu erlangen (im obigen Versuch sind ca. 25 % des Rapsöls nicht umgeestert worden), das bei der Reaktion anfallende Glycerin kontinuierlich entfernt.
Dadurch wird die (Gleichgewichts-)Reaktion zugunsten der Rapsölmethylester auf die Produktseite verschoben. Man nennt das Verfahren CD-Verfahren („continuously deglycerolizing“).
1.0.1.1 Demo 1: Vergleich der Viskositäten
6Chemikalien
· Rapsöl
6
basierend auf: RAABits Grundwerk Chemie Sekundarstufe II, Stuttgart: Raabe 2002, Kap. II/H 2, pp.1-20, M3
(-)
· Diesel
(Xn, N; R 40-51/53-65-66, S 2-29-36/37-61-62)
· Biodiesel (-)
Geräte
· 3 Reagenzgläser mit Gummistopfen
· 3 Glasmurmeln, in Reagenzgläser frei beweglich passend
· Gestell zum fixieren der 3 Gläser zum gleichzeitigen Umdrehen der Gläser Versuchsaufbau
RG mit Diesel RG mit Biodiesel RG mit Rapsöl
Glasmurmeln Holzstab
Durchführung/ Beobachtung
In jedes Reagenzglas wird eine Murmel gegeben, der Rest wird jeweils mit Diesel, Biodiesel bzw. Rapsöl aufgefüllt, so dass der Gummistopfen noch das Glas verschließen kann.
Anschließend werden die Reagenzgläser z.B. an einer Holzstange mit Draht derart befestigt, dass ein gleichzeitiges Umdrehen der Gläser möglich wird. Zur Demonstration der unterschiedlichen Viskositäten wird der Holzstab rasch gedreht, so dass alle Murmeln nach unten sinken können. Dabei sinkt die Murmel im Glas mit Diesel am schnellsten, im Glas mit Biodiesel etwas langsamer, im Glas mit Rapsöl hingegen dauert es sehr lange.
Auswertung/ Hintergründe
Die Demonstration zeigt anhand der unterschiedlichen Sinkgeschwindigkeiten sehr eindrucksvoll, dass die Flüssigkeiten unterschiedliche Viskositäten haben. Die Befunde decken sich qualitativ mit den in der Literatur gefundenen Werten.
Eine Begründung der unterschiedlichen Sinkgeschwindigkeit durch die Betrachtung der jeweiligen Dichte der Flüssigkeiten kann das Ergebnis nicht erklären (ρ
Diesel= 0,84 g/mL, ρ
Biodiesel= 0,88 g/mL, ρ
Rapsöl= 0, 92 g/mL
7).
Das Viskositätsproblem des Rapsöls wird ebenfalls durch die Umesterung behoben.
1.0.1.2 Demo 2: Verbrennung von Diesel bzw. Biodiesel
Chemikalien
· Biodiesel (-)
· Diesel
(Xn, N; R 40-51/53-65-66, S 2-29-36/37-61-62)
Geräte
· 2 kleine Döschen (z.B. von „Pulmoll“)
· Kerzendocht
· Nagel
Versuchsaufbau
7
alle Dichten aus: ftp://fnr-server.de/pdf/literatur/pdf_174bd_biokraftstoffe%20august%202005.pdf (besucht am
30.08.07)
Döschen mit Diesel bzw. Biodiesel Deckel
Loch Docht
Durchführung/ Beobachtung
Zunächst wird mit dem Nagel jeweils ein Loch in jeden Deckel gedrückt. Durch dieses Loch fädelt man jeweils ein Stück Docht, die Dochte sollten beide gleich weit ca. 2 mm aus dem Deckel ragen. Die Dose wird nun mit Diesel bzw. Biodiesel halb voll befüllt und der Deckel mitsamt Docht aufgesetzt. Zur Demonstration zündet man nun beide „Kerzen“ an, bei der Diesel-Kerze ist eine wesentlich stärker rußende Flamme erkennbar als bei der Biodiesel- Kerze.
Auswertung/ Hintergründe
Diese Demonstration zeigt, was sich auch bei der Verbrennung der beiden Kraftstoffe im Diesel-Motor feststellen lässt. In der Tat erzeugt Biodiesel beim Gebrauch im Kraftfahrzeug wesentlich weniger Ruß-Emissionen als normaler Diesel. Eine mögliche Erklärung hierfür ist, dass im Biodiesel, einem Ester, schon Sauerstoff molekular gebunden ist und somit eine vollständigere Verbrennung (Ruß-Bildung bedeutet unvollständige Verbrennung) ermöglicht wird.
Auch andere Abgas-Emissionen sind beim Einsatz von Biodiesel reduziert, z.B. wird aufgrund der Tatsache, dass Biodiesel von Natur aus nahezu schwefelfrei ist, kein Schwefeldioxid emittiert. Auf die Tatsache, dass Biodiesel aufgrund seiner regenerativen Herkunft nur soviel Kohlendioxid freisetzt wie vorher von den Rapspflanzen aufgenommen wurde und der daraus resultierende Glaube, dass Biodiesel die CO
2-Emissionen um 100 % gegenüber Diesel senke und somit eine Wohltat für bzw. eher gegen den Treibhauseffekt sei, möchte ich im Fazit näher eingehen.
1.1. Bioethanol
1.1.0 Einleitung
Zwar betrug der Bioethanol-Marktanteil in Deutschland in 2006 nur 0,5 %, allerdings fand ich diesen Biokraftstoff einerseits aufgrund seiner relativ einfachen Verfügbarkeit und andererseits aufgrund der intensiven Verwendung desselben in Brasilien und auch den USA interessant.
Sollten zudem Pilotprojekte zur Erzeugung von Ethanol aus Lignozellulose
8erfolgreich abgeschlossen werden, so wäre ein Verfahren zugänglich, welches mit weniger wertvollen Rohstoffen wie Holz oder Stroh höhere Ethanol-Erträge als mit heutigen Techniken ermöglichen würde. Zudem könnte die heute schon teilweise vorhandene Konkurrenz zwischen Nahrungsmittel- und Energiepflanzen-Produktion und die damit meist verbundenen Verteuerungen der Lebensmittel verringert werden.
Schaut man sich die Erträge von Ethanol pro Hektar Anbaufläche diverser Nutzpflanzen an, so wird deutlich, dass sich der Einsatz von Ethanol als Kraftstoff insbesondere in Brasilien eher lohnt als anderswo (siehe Diagramm 2).
Diagramm 2: Erträge von Ethanol [L/ha]
9Für meinen Vortrag habe ich mich deshalb auch näher an der Bioethanol-Produktion in Brasilien orientiert. Brasilien hatte 2006 einen Marktanteil von 34 % an der Welt-Ethanol- Produktion und war somit zweit-größter Produzent
8. 40 % des brasilianischen Kraftstoffbedarfs werden durch Ethanol gedeckt, 50 % der brasilianischen PKW fahren mit E85, einem Gemisch aus 85 Vol-% Ethanol mit 15 Vol-% Super-Benzin
10.
Der Bioethanol wird durch Vergärung von zuckerhaltigem Material mit Hefe erhalten, letzteres kann durch enzymatische Spaltung von stärkehaltigen Substanzen gewonnen werden:
8
siehe Spiegel Special „Neue Energien“, Nr.1/2007, S.61
9
aus: http://www.fh-aachen.de/uploads/media/061124_Bioethanol_Vortrag_sp.pps.zip (besucht am 31.08.07)
10
aus: http://www.fh-aachen.de/uploads/media/061124_Bioethanol_Vortrag_sp.pps.zip (besucht am 31.08.07)
6 10 5 2 6 12 6
Enzym
n Glukose aq
Stärke s
C H O n H O n C H O
Spaltung der Stärke
6 12 6aq Hefe
2
2 g2
2 5 aqGlukose Kohlendioxid Ethanol
C H O CO C H OH
Vergärung der Glukose
Die Vergärung findet im Allgemeinen nur bis zu einer Volumen-Konzentration bis ca. 20 Vol-% Ethanol statt, dann sind die Hefe-Zellen aufgrund des Alkohols gehemmt und können keine weitere Glukose in Ethanol umwandeln.
Um nun möglichst hochprozentigen Alkohol zu erhalten, wird die Gärmischung destilliert (mehrfach oder fraktioniert), auf diesem Wege kann man bis zu ca. 96 Vol-%igen Alkohol erhalten. Eine weitere Absolutierung des Alkohols auf destillativem Wege ist dann nicht mehr möglich, da ein Gemisch von 96 Vol-% Ethanol und 4 Vol-% Wasser azeotrop siedet. Das bedeutet, dass ein solches Gemisch bei der Siedetemperatur dieses Gemisches gleichstark verdampft, also genauso viel Ethanol wie Wasser in die Gasphase übergeht. Dadurch ist eine weitere Auftrennung des Gemisches auf diesem Wege ausgeschlossen.
Für die Verwendung als Kraftstoff im Gemisch mit Benzin wird allerdings sehr reiner Alkohol mit einem Gehalt von 99,5-99,8 Vol-% Ethanol benötigt. Mögliche Wege zur Absolutierung sind das Schleppmittelverfahren (destillative Auftrennung nach Zugabe eines dritten Stoffes, z.B. Toluol), das Membranverfahren (Gemisch wird an einer Membran vorbeigeleitet, welche nur für Wasser durchlässig ist, somit wird eine Aufkonzentrierung erreicht) und das Molekularsiebverfahren. Letzteres ist Motivation für Versuch 2 (s.u.).
1.1.1 Versuche
1.1.1.0 Versuch 2: Wasserentzug durch Molekularsieb
Chemikalien
· Ethanol
(F; R 11, S 7-16)
(ca. 94 Vol-%, z.B. durch fraktionierte Destillation von Zuckerrohrschnaps)
· Molekularsieb 3 A
(-) Geräte
· kleine Chromatographie-Säule
· kleiner Trichter
· Aräometer oder genaue Waage (mind. 3 Nachkommastellen), kleine Bechergläser und Vollpipetten
· Bechergläser
· Stativmaterial Versuchsaufbau
NS24
30
10 50 mL
20
Trichter
Chromatographiesäule mit Molekularsieb
Becherglas
Durchführung/ Beobachtung
Um einem zuvor destillativ aufkonzentriertem Ethanol/Wasser-Gemisch weiter Wasser zu entziehen, lässt man ca. 10 mL des Gemisches durch die mit dem Molekularsieb gefüllte Säule laufen. Eventuell ist es für eine bessere Adsorption des Wassers sinnvoll, das Molekularsieb vorher im Trockenofen zu trocknen.
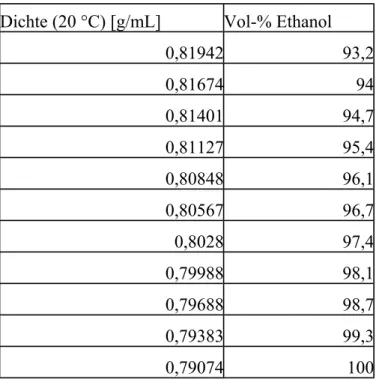
Die Konzentration des unten aufgefangenen Produktes kann dann über die Dichte unter Zuhilfenahme einer Dichte/Konzentrations-Tabelle (siehe Tabelle 2) bestimmt werden. Zu Vergleichszwecken kann man auch die Dichte des oben eingefüllten Gemisches bestimmen.
Dabei wird die Dichte entweder mit einem Aräometer direkt ermittelt, oder, falls nicht
verfügbar, indem mit einer Vollpipette (z.B. 5 mL) ein exaktes Volumen abgemessen wird, dessen Gewicht mithilfe einer genauen Waage dann festgestellt wird. Die Dichte ergibt sich dann als Quotient aus dem Gewicht pro Volumen.
Auswertung/ Hintergründe
Dichte (20 °C) [g/mL] Vol-% Ethanol
0,81942 93,2
0,81674 94
0,81401 94,7
0,81127 95,4
0,80848 96,1
0,80567 96,7
0,8028 97,4
0,79988 98,1
0,79688 98,7
0,79383 99,3
0,79074 100
Tabelle 2: Konzentrationsbestimmung über die Dichte
11Ergibt die Dichte-Bestimmung vor dem Passieren des Molekularsiebes einen Wert von ca.
0,815 g/mL ( ca. 94 Vol-% Ethanol), so kann bei dem Gemisch, dass die Säule durchlaufen hat, eine Dichte von ca. 0,801 ( ca. 97 Vol-% Ethanol) ermittelt werden. Zwar gelingt es mit dieser primitiven Säule nicht, den Alkohol zu absolutieren, aber die Idee dieses Verfahrens wird erkenntlich.
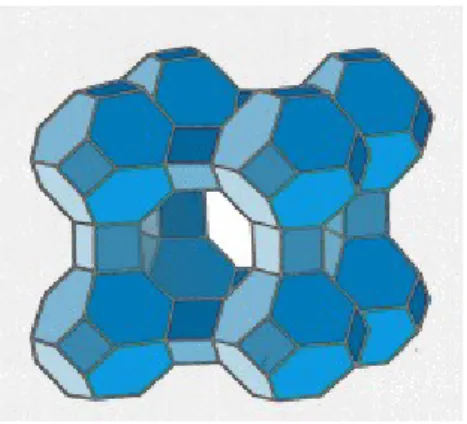
Das Molekularsieb 3 A ist ein Zeolith A, Zeolithe sind Alumosilikate mit großer innerer Oberfläche und „Käfigen“ (siehe Abbildung 1).
11
Auszug aus: http://www.hamm-chemie.de/j11/j11db/ethanol_wasser.pdf (besucht am 31.08.07)
Abbildung 1: Zeolith A
12Zeolithe bestehen aus gitterartigen Alumosilikat-Anionen, die negative Ladung wird durch Kationen stabilisiert, die in den Käfigen sitzen. Diese Kationen können ausgetauscht werden, diese Eigenschaft macht man sich bei Wasserenthärtern zu Nutze (z.B. Austausch Natrium gegen Calcium). Die negative Ladung des Alumosilicat-Gitters rührt von dem tetraedrisch gebundenen Aluminium her. Je mehr Aluminium ein Zeolith enthält (und entsprechend je weniger Silicium), desto dichter ist die negative Ladung im Gitter und dadurch umso polarer die innere Oberfläche. Das Molekularsieb 3 A (3 A steht für 3 Å = 3·10
-10m und gibt die Größe der Käfigöffnung an) besitzt zum einen eine relativ polare innere Oberfläche, so dass die Adsorption von neutralen polaren Molekülen (wie Wasser es ist) gut funktioniert, zum anderen ist die Käfigöffnung für Wasser groß genug, für Ethanol allerdings nicht.
13Technisch bedient man sich des gleichen Prinzips, allerdings unter optimierten Bedingungen und modifizierten technischen Details. Gefahren werden zwei Kolonnen, wobei abwechselnd die eine mit dem dampfförmigen, komprimierten Ethanol-Wasser-Gemisch beschickt und die andere regeneriert wird. Nach ca. 5-10 min. Betrieb ist die Beladung des Molekularsiebes mit Wasser so hoch, dass eine weitere Aufnahme von Wasser nicht mehr möglich ist. Zur Regeneration wird die Kolonne mit bereits absolutiertem Ethanol unter abgesenktem Partialdruck beschickt, dabei löst sich das adsorbierte Wasser. Das wasserhaltige Ethanol wird dann wieder in den Destillationsprozess überführt.
141.1.1.1 Versuch 3: Explosion eines E85-Luftgemisches
12
aus: http://www.arnold-chemie.de/grafik/zeolith-a.gif (besucht am 01.09.07)
13
allgemeine Informationen aus: http://www.arnold-chemie.de/grundlagen.html (besucht am 01.09.07)
14
technische Funktionsweise aus: https://www.fh-
muenster.de/fb4/downloads/personen/wetter/fhmuenstermachbarkeitsstudieabsolutierung.pdf (besucht am
31.08.07)
Um die Funktionsweise eines Otto-Motors bzw. genauer den Arbeitstakt eines Zylinders zu simulieren, eignet sich der folgende Versuch. Zudem wird durch die Explosion veranschaulicht, dass auch ein Gemisch aus 85 Vol-% Ethanol und 15 Vol-% Benzin als Treibstoff genutzt werden kann.
Chemikalien
· Super-Benzin
(F+, T, N; R 12-20/21/22/48-38-45-51/53-65-67, S 2-16-23-24-29-36/37-45-53-61-62)
· Ethanol
(F; R 11, S 7-16) Geräte
· Papp-Rohr mit Deckeln (z.B. Posterrolle)
· Watte
· Piezozünder (z.B. von Conrad Elektronic) oder Schaschlik-Spieß zur Zündung
· Isolierband
Versuchsaufbau
Piezozünder
2 Kabel Deckel Posterrolle
Watte (mit E85 getränkt)
Durchführung/ Beobachtung
Zuerst muss die Posterrolle präpariert werden. Ist ein Piezozünder vorhanden, werden die beiden Kontakte am Zünder mit zwei Kabeln verbunden. Die anderen beiden Kabelenden werden jeweils so durch ein kleines Loch an einem Ende der Rolle gesteckt, dass der Funke überspringen kann (testen!), anschließend die Kabel außen mit Isolierband fixieren. Ist kein Piezozünder vorhanden, so wird ein kleines Loch ( ca.5 mm) an einem Ende der Rolle in ebendiese mithilfe eines Messers gestochen. Zur Zündung hält man dann den brennenden Schaschlik-Spieß an das Loch (die Verwendung eines Feuerzeugs anstelle des Schaschlik- Spießes wird nicht empfohlen, die austretende Stichflamme kann schnell die Hand verbrennen!). Für einen festeren Sitz der Deckel (und somit lauteren Knall) können die Deckel an den in der Rolle sitzenden Seiten noch mit 2-3 Lagen Isolierband umwickelt werden, vom Festkleben o.ä. des Deckels sollte abgesehen werden, da sonst die Explosion andere Wege als das Herausdrücken des Deckels suchen könnte.
Ein explosionsfähiges E85-Luft-Gemisch wird hergestellt, indem man ca. 2 mL eines E85- Gemisches auf ein kleines Stück Watte gibt, die Watte in die Rolle überführt und mit geschlossenem Deckel das Gemisch zum Verdampfen gebracht wird, indem man die Watte mehrfach durch Drehen der Rolle in dieser hin- und herbewegt. Zum Zünden des Gemisches wird die Rolle senkrecht auf den Boden gestellt, so dass die Kabel bzw. das Loch sich unten befinden. Die Rolle wird mit einer Hand festgehalten, mit der anderen wird die Zündung vorgenommen, bei der Explosion fliegt der obere Deckel mit einem Knall und einer aus der Rolle austretenden Stichflamme aus der Rolle.
Sollte die Zündung nicht erfolgreich verlaufen, kommen im Prinzip zwei Gründe in Frage.
Zum einen kann es sein, dass der Wattebausch auf den Kontakten liegt und ein Überspringen
des Zündfunkens verhindert, zum anderen kann das in der Rolle befindliche Gemisch noch nicht genug verdampft sein, so dass noch kein explosionsfähiges Gemisch vorliegt.
Auswertung/ Hintergründe
Durch den Zündfunken wird das explosionsfähige Gemisch zur Explosion gebracht, die schlagartig entstehenden Verbrennungsgase treiben den Deckel aus der Rolle.
Reaktionsgleichungen:
Benzin (Hautbestandteil Alkane, n ≈ 5-11)
2 2
3 1
2 21
2n n
C H
n O
~n CO n H O
Ethanol
2 5
3
22
23
2C H OH O
~CO H O
Anstelle eines E85-Gemisches können auch andere leicht verdampfbare, entzündliche Stoffe verwendet werden, z.B. Pentan. Zur Berechnung der erforderlichen Flüssigkeitsmenge werden zunächst folgende Angaben benötigt: Volumen der Rolle (bestimmbar als Volumen eines Zylinders, V = π·r
2·h, wobei h die Länge der Rolle und r der Radius der Rolle ist), die Explosionsgrenzen des Stoffes (meist ein angegebener Bereich in Vol-% der verdampften Flüssigkeit in Luft), die Molmasse der Flüssigkeit sowie die Dichte der Flüssigkeit.
Zunächst wählt man sich einen Vol-%-Wert in der Mitte der Explosions-Grenzen aus und
ermittelt die erforderliche Menge verdampfter Flüssigkeit, die dem vorliegenden Volumen der
Rolle entspricht (Dreisatz, Bsp.: 5 Vol-% Pentan entsprechen 5 mL verdampften Pentans in
einem Rollenvolumen von 100 mL, für ein Rollenvolumen von 3 L werden also 150 mL
gasförmiges Pentan benötigt). Über das Normvolumen idealer Gase (1 mol eines idealen
Gases nimmt bei Normbedingungen 22,414 L Volumen ein) kann die der verdampften
Flüssigkeit entsprechende Stoffmenge angenähert ermittelt werden. Über die Stoffmenge
kann nun mithilfe der Molmasse der Flüssigkeit und der Beziehung m = n·M die Masse der
benötigten Flüssigkeit errechnet werden, welche entweder abgewogen oder unter
Verwendung der Dichte der Flüssigkeit in das Volumen der benötigten Flüssigkeit
umgerechnet wird (V = m/ρ). Diese Flüssigkeitsmenge wird dann auf den Wattebausch
aufgetragen und in der Rolle zum Verdampfen gebracht.
1.2. BtL-Kraftstoffe 1.2.0 Einleitung
Die Abkürzung „BtL“ kommt vom dem Begriff „biomass to liquid“ und ist als Begriff für flüssige Kraftstoffe entstanden, die aus Biomasse synthetisiert werden. Zurzeit sind am interessantesten die Verfahren, bei denen zunächst Holz oder andere organische Substanzen, auch Abfälle, durch Pyrolyse in Pyrolysegas und kokshaltige Rückstände zersetzt werden (siehe Versuch 4). Die Rückstände werden im nächsten Schritt weiter unterstöchiometrisch oxidiert, man erhält zusammen mit dem vorher erzeugten Gas das Synthese-Rohgas.
Im Fischer-Tropsch-Verfahren werden anschließend aus dem Synthese-Rohgas, welches zum großen Teil aus Kohlenmonoxid und Wasserstoff besteht, kettenförmige Alkane synthetisiert (siehe Versuch 5). Dieses Alkangemisch kann als Kraftstoff für Dieselmotoren verwendet werden.
1.2.1 Versuche
1.2.1.0 Versuch 4: Holzvergasung
15Dieser Versuch simuliert in einfacher Weise den ersten Schritt auf dem Weg zum BtL-Diesel, die Pyrolyse von Holz.
Chemikalien
· Holzspäne (z.B. Sägemehl) (-)
Geräte
· Reagenzglas mit durchbohrtem Stopfen
15
Idee aus: http://www.idee-nrw.de/pdfs/ureihechem.pdf (besucht am 01.09.2007)
· rechtwinkliges Ableitungsrohr
· Bunsenbrenner Versuchsaufbau
RG mit Sägemehl Ableitungsrohr
Brenner
Durchführung/ Beobachtung
Das Reagenzglas wird zu 1/3 mit Sägespänen befüllt, der Stopfen mit Ableitungsrohr aufgesetzt und anschließend wird das Reagenzglas am unteren Ende durch Fächern mit dem Brenner gleichmäßig erhitzt. Nach kurzer Zeit nimmt der zuvor gelblich-weiße Reagenzglasinhalt eine braune und dann eine schwarze Farbe an, gleichzeitig kondensieren an der oberen Reagenzglaswand Wasser und andere gelblich-braune Produkte, aus dem Ableitungsrohr tritt weißlicher Qualm aus. Letzterer kann mit Hilfe eines Feuerzeugs entzündet werden, eine von allein weiter brennende Flamme am Ende des Ableitungsrohrs wird beobachtet.
Auswertung/ Hintergründe
Holz besteht im Wesentlichen aus vier Bestandteilen: Cellulose (≈ 35 %), Hemicellulose (≈
20 %), Lignin (≈ 20 %) und Wasser (≈ 25 %). Cellulose und Hemicellulose sind
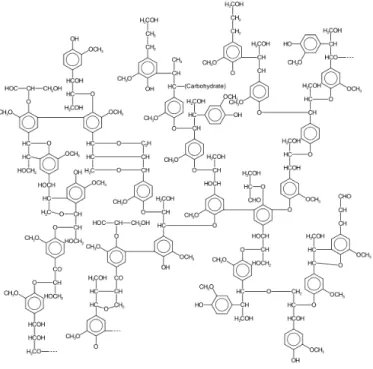
Polysaccharide, Lignin ist ein unregelmäßiges Phenol-Polymer (siehe Abbildungen 2,3 und
4).
Abbildung 2: Cellulose
16Abbildung 3: Hemicellulose
1716
aus: http://www.doitpoms.ac.uk/tlplib/wood/figures/cellulose.png (besucht am 01.09.07)
17
aus: http://www.membres.lycos.fr/nico911/images/hemicell.gif (besucht am 20.06.07)
Abbildung 4: Lignin
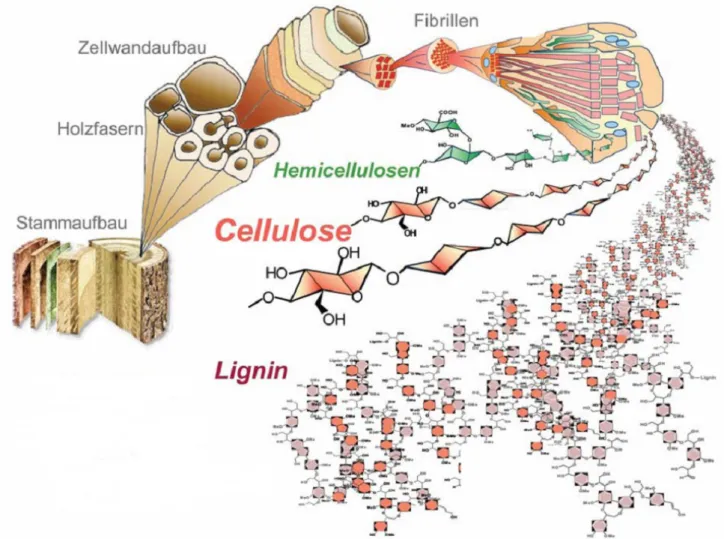
18Schematisch kann man sich den Aufbau des Holzes wie in Abbildung 5 vorstellen:
18
aus: http://upload.wikimedia.org/wikipedia/commons/e/ee/Lignin_structure.svg (besucht am 01.09.07)
Abbildung 5: struktureller Aufbau von Holz
19Bei dem Versuch findet zunächst die Zersetzung des Holzes in gasförmige Bestandteile (Holzgas), flüssige (Holzgeist) und feste (Holzkohle/Holzteer) statt. In abstrakter Reaktionsgleichung kann man sich den Vorgang wie folgt vorstellen:
2
2 4
2
8 4 8
k m n s s g g
k m n s s g g g
C H O k n C n CO m H
m m m
C H O k n C n CO H CH
Die Tatsache, dass das aus dem Ableitungsrohr entweichende Holzgas brennbar ist, kann durch die bei der Pyrolyse entstehenden Gase Kohlenmonoxid, Wasserstoff und Methan erklärt werden.
19
aus: ftp://fnr-server.de/pdf/literatur/pdf_253studie_zur_direktverfluessigung_final_komprimiert.pdf (besucht
am 01.09.07)
Bei der einfachen Pyrolyse (wie in diesem Versuch) ist die Gaszusammensetzung eine andere, als wenn nach der Pyrolyse auch noch die Koks- und Teer-Rückstände unvollständig oxidiert werden (siehe Tabelle 3).
Holzgas-Zusammensetzung Gas-Zusammensetzung nach zusätzlicher unterstöchiometrischer Oxidation von Holkohle/-teer (Synthese-Rohgas)
CO 34 % 20 %
H2 2 % 20 %
C2H4 2 % -
CH4 13 % 2 %
N2 - 45 %
CO2 49 % 13 %
Tabelle 3: Gaszusammensetzungen
20Der in der Tabelle auftretende Stickstoff ist im Synthese-Rohgas vorhanden, da die weitere unvollständige Oxidation mit Luft geschieht. Man kann gut erkennen, dass das Synthese- Rohgas einen höheren Wasserstoff-Anteil und einen geringeren Kohlendioxid-Anteil aufweist, was für die Fischer-Tropsch-Synthese wichtig ist.
1.2.1.1 Versuch 5: Fischer-Tropsch-Synthese
21,22Der nachfolgende Versuch soll die eigentliche Synthese des Fischer-Tropsch-Diesels demonstrieren. Es ist mir nicht gelungen, unter Laborbedingungen flüssige Endprodukte zu synthetisieren, jedoch wird das Prinzip der Synthese durch den Versuch etwas verdeutlicht.
Chemikalien
Für Katalysatorherstellung
20
Werte aus: http://www.bhkws.de/bhkw_anwendung_holzgas.htm und http://www.holzgas.com/kraftwaerme.htm (besucht am 01.09.07)
21
Katalysatorherstellung und Prinzip aus: Chemie in der Schule, Heft 5 (1958), S. 101; Heft 6 (1959), S. 94; Heft 7 (1960), S. 211 (Autoren: W. Jöricke, E. Schulze)
22
weitere Anregungen aus: http://www.schuelerforum-nordbayern.de/schuelerforum%20vortraege/Energie
%20und%20Umwelt/7%2005%20Kraftstoffe%20aus%20nachwachsenden%20Rohstoffen.pdf (besucht am
01.09.07)
· Cobaltnitrat Co(NO
3)
2· 6 H
2O (Xn; R 22-40-43, S 36/37)
· Natriumcarbonat Na
2CO
3(Xi; R 36, S 22-26)
· Magesiumoxid MgO (-; S 22)
· konz. Ameisensäure HCOOH (C; R 10-35, S 23-26-45)
· techn. Wasserglaslösung (Xi; R 36/38, S 26)
· Eisendrehspäne (-)
Für Synthesegasherstellung
· konz. Ameisensäure HCOOH (C; R 10-35, S 23-26-45)
· konz. Schwefelsäure H
2SO
4(C; R 35, S 26-30-45)
· konz. Salzsäure HCl
(C; R 34-37, S 26-36/37/39-45)
· Zink-Granalien Zn (-)
Geräte
Für Katalysatorherstellung
· Becherglas (600 mL), Becherglas (1,5 L)
· Glasstab
· 2 Magnetrührer mit Fisch
· große Porzellannutsche
· Exsikkator
· Filterpapier
· ein paar größere Reagenzgläser
· auf RG passender, durchbohrter Stopfen, dazu passendes Ableitungsrohr
· auf Ableitungsrohr passendes Stück PVC-Schlauch (ca. 20 cm)
· Bunsenbrenner
· fest verschließbares Vorratsgefäß für Katalysator Für Synthesegasherstellung
· 2 Reagenzgläser mit durchbohrtem Stopfen und Ableitungsrohr
· 2 Stücke PVC-Schlauch (ca. 20 cm)
· 2 Einwegspritzen mit Kanüle
· Bunsenbrenner oder Wasserbad Für den eigentlichen Versuch
· 2 Kolbenprober (100 mL) mit Drei-Wege-Hahn
· Glührohr mit 2 fest sitzenden, durchbohrten Stopfen
· Glaswolle
· Digitalthermometer mit Temperaturfühler
· Glaswolle
· kleine Glasrohrstücke, PVC-Schlauch
· Bunsenbrenner
· Stativmaterial, diverse Schlauchschellen Für die Produktanalyse (Gaschromatographie)
· Low-Cost-Gaschromatograph (bestehend aus: Aquarienpumpe, GC-Säule,
Glühbirnen-Detektoreinheit inkl. Detektorelektronik, PC mit Auswertungssoftware;
alles vom AG Kappenberg)
· für selbst gemachte GC-Säule:
- Schlauch, Länge: 80 cm;
innen= 4 mm (laut GC-Hersteller am besten aus PA, nach meiner Erfahrung funktioniert ebenso gut ein im Baumarkt erhältlicher Aquarienpumpenschlauch aus Silikon),
- Silicagel (80-130 msh)
- 2 Kabelbinder
· 5 mL-Einwegspritze mit Kanüle
· zu Vergleichszwecken: Methan aus der Druckdose Versuchsaufbau
mL100
0 20 40 60 80
mL100 020
40
60
80
Kolbenprober
3-Wege-Hahn
Katalysator auf Eisenspänen
Glaswolle
Brenner
Durchführung/ Beobachtung Katalysatorherstellung
Die hier nun beschriebene Darstellung für den Cobalt-Katalysator entspricht dem halben Ansatz der in Quelle
20angegebenen Menge, wobei diese Menge, sollte der Versuch nach meiner unten beschriebenen Vorschrift durchgeführt werden, noch wesentlich reduziert werden kann (1/10 des Original-Ansatzes reicht vollkommen aus).
Zunächst werden 100g Cobaltnitrat in 400 mL ention. Wasser gelöst, parallel werden 60 g Na
2CO
3in 1 L ention. Wasser gelöst. Beide Lösungen werden zum Sieden gebracht, anschließend wird die Soda-Lösung schnell in die Cobaltnitrat-Lösung gegossen. Nach kurzem Umrühren wird der Niederschlag sofort auf einer großen Nutsche abgesaugt. Der Niederschlag von Cobaltcarbonat wird dann in 750 mL siedendes Wasser eingebracht, verrührt und nochmals abgesaugt, anschließend wird der Niederschlag einige Tage an der Luft oder im Exsikkator getrocknet.
Im nächsten Schritt trägt man unter Rühren in 250 mL konz. Ameisensäure zuerst 30 g
Magnesiumoxid ein, dann das Kobaltcarbonat. Nun lässt man das Gemisch ein bis zwei Tage
im bedeckten Gefäß stehen, ohne den Niederschlag aufzuwirbeln. Danach gießt man die
überstehende Lösung ab, ohne den Niederschlag aufzuwirbeln, und gibt den Niederschlag auf
Filterpapier, worauf er oberflächlich an einem staubfreien Ort über Nacht trocknen gelassen
wird.
Der Niederschlag wird nun mit verdünnter Wasserglaslösung (25 g technische Wasserglaslösung wird mit ention. Wasser auf ein Volumen von 50 mL aufgefüllt) übergossen, nach einiger Zeit presst man auf Filterpapier ab und lässt möglichst vollständig trocknen, am besten im Exsikkator über Calciumchlorid und Ätznatron (Natriumhydroxid mit Calciumhydroxid).
Um nun das fein verteilte Cobalt-Pulver zu erhalten, füllt man ein großes Reagenzglas ca. 1/3 voll mit dem getrockneten Pulver, welches man zwischen Eisendrehspänen verteilt. Man setzt einen durchbohrten Stopfen auf, durch den ein PVC-Schlauch führt. Letzteren führt man in die Luftzufuhr eines Brenners und entzündet diesen. Mit einem anderen Brenner wird nun das Reagenzglas langsam und gleichmäßig erhitzt, wobei sich das Pulver durch Zersetzung des Cobaltformiats zu Cobalt, Kohlenmonoxid, Kohlendioxid und Wasser schwarz färbt und beim Indikatorbrenner eine blaue Flamme aufgrund des Kohlenmonoxids zu erkennen ist. Unter Schütteln erhitzt man so lange, bis ein gleichmäßig schwarzes Pulver vorliegt, allerdings sollte man nicht zu stark erhitzen, um ein Zusammensintern des Pulvers zu vermeiden.
Allerdings muss auch eine vollständige Umsetzung erreicht worden sein, das Vorhandensein von kleinen rosa-farbenen Klumpen ist ein Zeichen dafür, dass das Ende noch nicht erreicht ist. Man lässt vollständig erkalten und gibt den Reagenzglasinhalt in ein fest verschließbares Vorratsgefäß, man muss Luftkontakt des Pulvers möglichst vermeiden, da es zur Selbstentzündung neigt. Diesen Vorgang wiederholt man, bis alles Cobaltformiat zersetzt wurde.
Synthesegasherstellung
Stehen Wasserstoff und Kohlenmonoxid nicht in Bomben zur Verfügung, so können diese (nachdem die eigentliche Syntheseapparatur aufgebaut wurde!!) selbst hergestellt werden.
Für die Wasserstoff-Herstellung werden in ein Reagenzglas 2-3 Zink-Granalien gefüllt und ein fest sitzender, einfach durchbohrter Stopfen mit darin befindlichem Ableitungsrohr aufgesetzt. Durch den Stopfen wird eine Kanüle gestochen, auf diese wird eine mit konz.
Salzsäure gefüllte Einwegspritze aufgesetzt. Tropfenweise wird nun Säure zugetropft, nachdem die Luft im Reagenzglas verdrängt wurde, wird das Gas über den Drei-Wege-Hahn in den Kolbenprober gefüllt.
Kohlenmonoxid stellt man her, indem ein Gasentwickler nach oben beschriebenem Prinzip
hergestellt wird, jedoch wird das Reagenzglas zu ca. einem Drittel mit konz. Schwefelsäure
gefüllt, die Spritze mit konz. Ameisensäure. Nachdem die Schwefelsäure erwärmt wurde (ca.
70°C, entweder im Wasserbad oder vorsichtig mit dem Brenner), lässt man langsam Ameisensäure zutropfen und verfährt mit dem Auffangen des Gases wie oben.
Fischer-Tropsch-Synthese
Gemäß der Skizze zum Versuchsaufbau verbindet man zwei Kolbenprober mit Drei-Wege- Hahn mit PVC-Schlauch und Schellen mit dem Glührohr. Dieses wurde zuvor mit dem Kontakt (Cobaltpulver zwischen Eisendrehspänen) so gefüllt, dass der Kontakt in der Mitte des Rohres zum Liegen kommt und möglichst den gesamten Querschnitt des Rohres ausfüllt.
Um zu verhindern, dass der Kontakt beim Synthesevorgang in die Prober gelangt, werden an den Enden des Glührohres Glaswollebäusche eingesteckt. In die Enden des Glührohres werden einfach durchbohrte Gummistopfen gesteckt, welche dicht abschließen müssen. In der Bohrung steckt jeweils ein kleines Stück Glasrohr, um die PVC-Schläuche mit Schraubschellen anschließen zu können. Zur Temperaturkontrolle wird durch einen der am Ende des Glührohres befindlichen Stopfens der Fühler eines Thermometers gestochen (für dichten Sitz des Fühlers empfiehlt es sich, mit einem erhitzen Stück Draht ein feines Loch in den Stopfen zu schmelzen, durch welches man den Fühler schiebt). Das Ende des Fühlers sollte sich sinnvollerweise in der Mitte der Katalysatormischung befinden. Nachdem die Dichtigkeit der Apparatur getestet wurde, füllt man den ersten Kolbenprober voll mit Wasserstoff und spült damit die Apparatur, indem man das Gas durch die Apparatur hin- und herleitet. Man lässt das Gas aus dem Drei-Wege-Hahn des anderen Probers entweichen, befüllt den ersten Prober erneut voll mit Wasserstoff, und drückt dann wiederum soviel Gas durch den Drei-Wege-Hahn des anderen Kolbenprobers aus der Apparatur, bis in dem Wasserstoffkolbenprober noch ca. 50 mL Wasserstoff verbleiben. Nun wird der andere Kolbenprober mit Kohlenmonoxid voll gefüllt, worauf man direkt über den an diesem Prober befindlichen Hahn wiederum soviel Gas ausströmen lässt, bis ein Volumen von ca. 20 mL in diesem verbleibt. Die Hähne werden nun so gedreht, dass beide Kolbenprober mit der Apparatur verbunden sind, und man vermischt die Gase durch hin- und herschieben der Prober. Nach dem Mischen drückt man das gesamte Gas in einen der Prober und bestimmt das Gesamtvolumen, dieses sollte ca. 70 mL betragen, auf Druckfreiheit in der Apparatur ist zu achten.
Die Synthese beginnt man, indem man mit einem Bunsenbrenner den im Glührohr
befindlichen Katalysator erhitzt. Ist eine Temperatur von ca. 250 °C erreicht, leitet man das
Gas über den Kontakt hin und her. Nach anfänglicher geringer Volumenzunahme (auf ein
Volumen von ca. 80 mL, eine größere Volumenzunahme deutet auf einen nicht vollständig umgesetzten Katalysator hin bzw. auf Feuchtigkeitsrückstände in diesem hin und hat sehr wahrscheinlich ein Scheitern des Versuchs zur Folge) durch die Erwärmung des Gases nimmt im weiteren Verlauf das Volumen nach und nach ab, nach ca. 5-10 min ist nur noch ein Volumen von ca. 25 mL vorhanden, dies ist ein Anzeichen dafür, dass die Reaktion abgelaufen ist. Zur Untersuchung des Gases mit einem Gaschromatographen wird mit einer sauberen Einwegspritze eine Probe aus einem der Drei-Wege-Hähne entnommen.
Analyse mittels GC
Für die Analyse von Methan (erwartetes Hauptprodukt) neben Wasserstoff benötigt man eine andere als die mitgelieferte GC-Säule, in dieser werden Wasserstoff und Methan nicht getrennt, ihre Peaks liegen übereinander, wodurch man nicht erkennen kann, ob man das Edukt Wasserstoff oder das Produkt Methan identifiziert hat. Diese kann man sich jedoch einfach, unkompliziert und billig selbst herstellen. Dazu nimmt man ein 80 cm langes Stück Silikonschlauch mit einem Innendurchmesser von 4 mm und befüllt diesen mit dem Silicagel so, dass zum Schluss an den Enden jeweils ca. 5 mm frei bleiben, der Rest aber durchgängig mit dem Trägermaterial gefüllt ist. In die Enden stopft man jeweils ein kleines Stück Glaswolle, es sollte immer noch an beiden Enden etwas unbefüllter Schlauch vorhanden sein.
Um der Säule etwas Halt zu geben, wickelt man ca. 3 Windungen auf und fixiert diese mit 2 Kabelbindern.
Nachdem man die GC-Apparatur gemäß der Beschreibung aufgebaut hat, entfernt man die ursprüngliche GC-Säule durch Abdrehen der Anschlussmutter und baut die neue Säule entsprechend ein. Zur Analyse des Produktgases stellt man die Aquarienpumpe, die Detektorelektronik und den PC an und spritzt zügig 1 mL des erzeugten Gases in das Septum ein. Zu Vergleichszwecken kann man auch noch Methan aus der Druckgasdose sowie den reinen selbst hergestellten Wasserstoff untersuchen. Nach meinen Erfahrungen befindet sich der Methan-Peak direkt hinter dem (größeren) Wasserstoff-Peak (siehe Auswertung).
Auswertung/ Hintergründe
Katalysatorherstellung
Die Herstellung eines fein verteilten Cobalt-Pulvers geschieht durch thermische Zersetzung von Cobaltformiat, welches zuvor aus Cobaltcarbonat und dieses wiederum aus Cobaltnitrat hergestellt wurde.
3
2
aq 2 3
aq 3
s2
aq2
3
aqCo NO Na CO CoCO Na
NO
3s
2
l 2s"
2 3"
aqCoCO HCOOH Co HCOO H CO
2 1 2 2 2 0 2 2 4 2 1 2
2 2
2
s g g l
s
Co H C OO
Co C O
C O
H O
Synthesegas-Herstellung
Die Herstellung von Wasserstoff und Kohlenmonoxid geschieht gemäß folgenden Reaktionsgleichungen.
s2
aq 2
g 2
aqZn HCl H ZnCl
2
2
2 4l l g 3 4 aq
H SO H C OOH
C O
H O
HSO
Fischer-Tropsch-Synthese
Die Fischer-Tropsch-Synthese ist eigentlich eine Reaktion, bei der C-C-Bindungen gebildet
werden und so kettenförmige Kohlenwasserstoffe aufgebaut werden. Das Verfahren, aus
Synthesegas flüssige Kohlenwasserstoffe zu synthetisieren, ist schon länger bekannt. 1925
hatten die beiden Chemiker Hans Tropsch und Franz Fischer ihre Forschungen soweit
vorangetrieben, dass sie unter geeigneten Bedingungen (hoher Druck, ca. 200-300 °C
Temperatur) mit bestimmten Katalysatoren flüssige Kohlenwasserstoffe herstellen konnten.
Foto 1: Franz Fischer (l.) und Hans Tropsch
23Dieses Verfahren wurde dann auch vom Nazi-Regime während des 2. Weltkrieges eingesetzt, um die Kriegsmaschinerie mit Treibstoff zu versorgen, Öllieferungen aus dem Ausland waren eingestellt. Ebenso wird und wurde das Verfahren in Südafrika während der Apartheid eingesetzt, da Ölembargos dies notwendig machten und andererseits Kohle in Südafrika ausreichend vorhanden war/ist (die Firma Sasol betreibt noch heute einige Fischer-Tropsch- Synthese-Anlagen). Kohle war für die Erzeugung des Synthesegases notwendig, im Gegensatz zu heutigen Bestrebungen, das Synthesegas aus regenerativen Quellen zu gewinnen, wurde damals das Synthesegas durch Kohlevergasumg von Kohle mit Wasserdampf und Sauerstoff bei höheren Temperaturen gewonnen.
Die Fischer-Tropsch-Sythese kann man allgemein mit folgender Reaktionsgleichung beschreiben (kettenförmiges Wachstum):
2 2 0 2/ 3 1 1 2
. /
2 2 2 / / 2
2 1
Co bzw Feg g n n s l g l g
n C O
n H
C H
n H O
Die Fischer-Tropsch-Synthese kann man schematisch wie folgt darstellen
24:
23
aus:
http://www.mpg.de/bilderBerichteDokumente/multimedial/bilderWissenschaft/2005/12/Haenel0501/Web_Zoom .jpeg (besucht am 6.09.2007)
24
nach: http://www.tu-braunschweig.de/Medien-DB/anchem/merk_kontakte1991-3_29-52.pdf (besucht am 06.09.2007)
C O + H
2C O
. .
Co-Oberfläche
H H . .
H .
H . C
. . . O
.
O H
2H
2CH
3.
CO CH
2. .
CH . . .
CH
2C H
3.
H
2CO
CH
2. .
CH
2. . O
H
2. CH
2(CH
2)
nC
H
3H
2CH
3(CH
2)
nC
H
3Dabei werden zunächst der Wasserstoff und das Kohlenmonoxid assoziativ an die Cobalt- Oberfläche adsorbiert, anschließend werden die C-O-Bindung und die H-H-Bindung gespalten. Mit dem adsorbierten Wasserstoff wird dann der Kohlenstoff und der Sauerstoff jeweils hydriert, dass entstehende Wasser verlässt die Katalysatoroberfläche. Im weiteren Verlauf werden nun C-C-Bindungen zwischen den an der Oberfläche gebundenen CH
x- Gruppen geknüpft, die Kette wächst. Nach einer bestimmten Anzahl von Wachstumsschritten wird die Kohlenwasserstoffkette dann desorbiert.
Unter den von mir erreichten Bedingungen war dies jedoch nicht möglich, somit stellt meine Reaktion nur einen Vorläufer der Fischer-Tropsch-Synthese dar, die das Prinzip verdeutlichen soll.
Das unter den oben beschriebenen Bedingungen erwartete Haupt-Reaktionsprodukt ist Methan:
2 2 0 4 1 1 2
2 4 2 /
3
Cog g g l g
C O
H
C H
H O
4 mol Gas
2 mol Gas (bzw. 1
mol Gas, wenn das
Wasser kondensiert)
Die Reaktionsgleichung erklärt auch anschaulich die Volumenabnahme während der Synthese, man erkennt, dass für große Ausbeuten ein großer Druck hilfreich ist (Prinzip des kleinsten Zwanges).
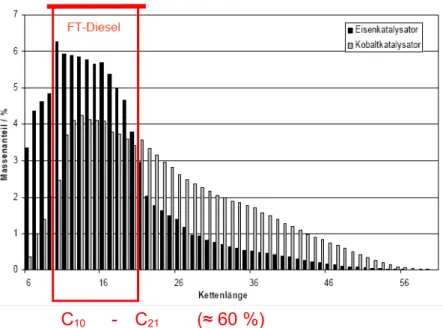
Bei einer typischen technischen Fischer-Tropsch-Synthese erhält man andere Reaktionsprodukte als nur Methan. Eine typische Produktverteilung gibt nachfolgende Grafik wieder (schwarz: Fe-Katalysator, grau: Cobalt-Katalysator).
Diagramm 3: Produktverteilung Fischer-Tropsch-Synthese
25Gaschromatographie
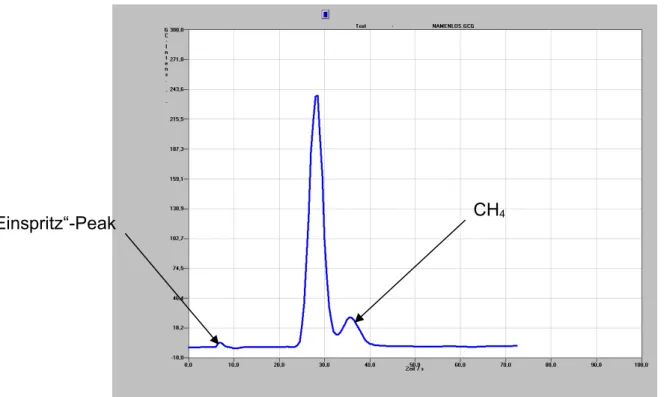
Die Auswertung des Produktgases mittels Gaschromatographie liefert folgendes Ergebnis:
25
aus: http://www.renet.at/gfx/download/biomasse/4_Hofbauer1_EZ-P4-Polygeneration_2005.pdf (besucht am 6.09.2007)
C
10-
C
21(≈ 60 %)
H
2Diagramm 4: Ergebnis GC-Analyse
Durch vorherige Vergleichsmessungen von reinem Methan und reinem Wasserstoff konnten die Peaks den jeweiligen Stoffen zugeordnet werden.
Die grobe Funktionsweise eines Chromatographen ist folgende: Man hat eine stationäre und eine mobile Phase (hier: Luft als mobile Phase, das Silicagel als stationäre Phase). Durch unterschiedlich starke Adsorption der zu trennenden Stoffe an der stationären Phase passieren die Stoffe unterschiedlich schnell mithilfe der mobilen Phase die Chromatographie-Säule. Am Ende der Säule werden die Stoffe detektiert, bei diesem Gaschromatographen funktioniert das derart, dass durch eine Glühbirne, deren Glaskolben entfernt wurde, ein konstanter Strom geleitet wird und der Spannungsabfall, verursacht durch die verschiedenen Wärmeleitfähigkeiten der vorbeiströmenden Gase, gemessen wird.
1.3. weitere, nicht im Vortrag behandelte regenerative Kraftstoffe
Natürlich kann so ein kurzer Experimentalvortrag nicht alle Konzepte ansprechen, die die Erzeugung von regenerativen Kraftstoffen verfolgen. In kurzer Darstellung sollen nun noch zwei weitere Kraftstoffe vorgestellt werden, die der Vortrag nicht berücksichtigte.
„Einspritz“-Peak CH
41.3.0 Wasserstoff
Wasserstoff als Energieträger (nicht Energiequelle!) und somit als Kraftstoff ist eine mögliche Option, die vielleicht bald große Bedeutung haben wird. Seine Gewinnung kann auf unterschiedlichen Wegen erfolgen, eine Möglichkeit wäre die Elektrolyse von Wasser mit regenerativ hergestelltem Strom. Aus ökonomischen Gründen müsste dieser Strom aber im Überfluss zur Verfügung stehen, dies ist im Moment (zumindest in Deutschland) noch nicht der Fall. Aus Wasserkraft gewonnener überschüssiger Strom könnte dafür genutzt werden (wie er z.B. in großem Maße in Norwegen gewonnen wird). Der Weg der Wasserstoff- Gewinnung über die Elektrolyse bringt aber auch Energieverluste mit sich. Andere, noch nicht ausreichend ausgereifte Verfahren haben das Ziel, den Wasserstoff direkt aus Biomasse zu gewinnen, ohne den mit Verlust behafteten Umweg über die Elektrolyse zu gehen. Die direkte Gewinnung von Wasserstoff aus Biomasse kann derart erfolgen, dass Biomasse mit Wasser zunächst vergast wird zu Synthesegas, und der darin enthaltene Wasserstoff abgetrennt wird.
Der gewonnene Wasserstoff kann dann als Kraftstoff entweder in Brennstoffzellen elektrischen Strom erzeugen, der dann Elektromotoren antreibt, oder in Verbrennungsmotoren die Stelle von Benzin bzw. Diesel einnehmen. Nachteilig bei letzterem Konzept ist, dass, nicht wie bei der Brennstoffzelle, durch die höheren Temperaturen Stickoxide entstehen, wodurch die Emissionen beim mit Wasserstoff betriebenen Fahrzeug sich nicht auf Wasser(- dampf) beschränken. Daher und auch aus Effizienzgründen scheint das Brennstoffzellenkonzept vielversprechender zu sein.
Allerdings ist die Verwendung von Wasserstoff als Kraftstoff auch mit diversen Problemen
behaftet. Zum einen ist es aus Volumengründen zweckmäßig, Wasserstoff in flüssiger Form
zu verwenden. Um diesen jedoch zu gewinnen und auch diesen Aggregatzustand zu erhalten
sind große Drücke und enorme Abkühlung vonnöten, was wiederum mit einem
Energieaufwand verbunden ist. Zudem muss eine sichere Lagerung und Transport des
Wasserstoffs ermöglicht werden. Des Weiteren ist für den Einsatz von Wasserstoff in
Kraftfahrzeugen keine Infrastruktur (Tankstellen, Versorgungswege, Produktionsanlagen)
vorhanden, wodurch das Vorantreiben der Technologie (neben der Tatsache, dass Wasserstoff
einerseits noch nicht wirtschaftlich und erst recht nicht regenerativ gewonnen wird/werden
kann) gehemmt wird, und ebenso wird der Aufbau einer entsprechenden Infrastruktur nicht
forciert, so lange nicht genügend Bedarf durch Fahrzeuge herrscht, ein kleiner Teufelskreis.
1.3.1 Biogas
Biogasanlagen sind momentan in vielen ländlichen Gebieten groß im Kommen, besteht doch die Möglichkeit, aus Abfällen über die Produktion von Strom Geld zu machen. Biogas wird aus landwirtschaftlichen Abfällen (Gülle, Gras, Grünabfälle jeglicher Art, Stroh) und/oder zu diesem Zweck angebautem Biomaterial (Maissilage etc.) durch (anaerobe) Vergärung erhalten, es besteht zum größten Teil aus Methan. Dieses Biogas wird in den schon heute betriebenen Biogasanlagen zum Antrieb von Motoren verwendet, die wiederum Generatoren antreiben und somit Strom produzieren (sogenannte Blockheizkraftwerke).
Anstelle der Erzeugung von Strom aus dem Biogas könnte dieses aber auch direkt in Verbrennungsmotoren zum Einsatz kommen. Biogas könnte dann, analog der Nutzung von Erdgas, als regenerativer Kraftstoff genutzt werden. Allerdings ist zuvor eine Aufarbeitung des erzeugten Biogases auf Erdgasqualität notwendig (Abtrennung von Kohlendioxid, Stickstoff etc.)
2. Schulrelevanz
Ausgehend vom hessischen Lehrplan für Chemie an Gymnasien (G8)
26werden in diesem Vortrag folgende Stichpunkte angesprochen:
• 7G.1: Trennverfahren zur Trennung von Stoffgemischen aus Alltag, Industrie und Umwelt kennen lernen
• 9G.3: Erdöl und Erdgas als Energieträger und Rohstoffe
Vorgänge im Verbrennungsmotor (u.a. Modellversuch zum Otto-Motor, Explosion von Benzin-Luft-Gemischen)
• 10G: Alkanole
fakultativ: Alkohole als Treibstoffzusatz
26
http://www.kultusministerium.hessen.de/irj/servlet/prt/portal/prtroot/slimp.CMReader/HKM_15/HKM_Internet
/med/08a/08a50e9f-ba45-b901-be59-2697ccf4e69f,22222222-2222-2222-2222-222222222222,true.pdf (besucht
am 07.09.2007)
• 11G.1: Mechanismus der Esterbildung und -verseifung, mehrwertige Alkohole (Glycerin)
• 11G.2: Fette
• 12G.2: Wahlthema Angewandte Chemie (u.a. „Vom Raps zum Biodiesel“)
3. Fazit
3.0 Regenerative Kraftstoffe
Auf die alltägliche Gegenwärtigkeit der Debatte über den Klimawandel mit möglichen Lösungen für dieses Problem wie z.B. den Einsatz regenerativer Energien wurde schon in der Einleitung eingegangen, hier möchte ich nun einige kritische Bemerkungen zum Thema Regenerative Kraftstoffe machen.
Die grundsätzliche Idee, den menschlichen Hunger nach Energie auch durch Energieträger zu stillen, die regenerativ gewonnen werden können, indem man die von der Sonne abgestrahlte Energie nutzt (sei es fürs Pflanzenwachstum, sei es für Photovoltaikzellen, sei es durch Verwertung der Windenergie usw.), ist durchaus positiv zu bewerten. Schwinden irgendwann die fossilen Rohstoffe vollständig, sind wir auf diese Art der Energiegewinnung sowieso angewiesen, im Moment kommen sie vor allem verstärkt zum Einsatz, um dem steigenden CO
2-Ausstoß etwas entgegenzusetzen. So lobenswert der Grundsatz und die ursprüngliche Idee auch sind, so angreifbar ist auch die Umsetzung in die Praxis. Einst von grünen Visionären geträumt und von anderen belächelt, haben regenerative Energien heute einen festen Bestandteil in unserer Gesellschaft, sogar eine konservative Kanzlerin hat sich die Bekämpfung des Klimawandels zum Ziel gesetzt. Jedoch ist deren Nutzen für die Umwelt manchmal nicht mehr zu entdecken.
Ganz allgemein ist es häufig noch so, dass die Verfahren zur Nutzung regenerativer Energien nicht so weit ausgereift sind, dass sie rentabel sind. Aber eingesetzt werden sie trotzdem, dank staatlicher Subventionen, die die Kosten-Nutzen-Rechnung verschönern. Zum Beispiel ist es so, dass kleine Windkraftanlagen während ihrer gesamten Laufzeit weniger Energie erzeugen, als zu ihrer Herstellung nötig war
27. Diese Missstände werden einerseits durch weitere Forschung und größere Anlagen sicherlich bald behoben, aber im Moment werden sie durch
27
![Diagramm 2: Erträge von Ethanol [L/ha] 9](https://thumb-eu.123doks.com/thumbv2/1library_info/3938822.1532899/13.892.244.623.587.784/diagramm-erträge-von-ethanol-l-ha.webp)