Hinweis
Bei dieser Datei handelt es sich um ein Protokoll, das einen Vortrag im Rahmen des Chemielehramtsstudiums an der Uni Marburg referiert. Zur besseren
Durchsuchbarkeit wurde zudem eine Texterkennung durchgeführt und hinter das eingescannte Bild gelegt, so dass Copy & Paste möglich ist – aber Vorsicht, die Texterkennung wurde nicht korrigiert und ist gerade bei schlecht leserlichen Dateien mit Fehlern behaftet.
Alle mehr als 700 Protokolle (Anfang 2007) können auf der Seite
http://www.chids.de/veranstaltungen/uebungen_experimentalvortrag.html eingesehen und heruntergeladen werden.
Zudem stehen auf der Seite www.chids.de weitere Versuche, Lernzirkel und Staatsexamensarbeiten bereit.
Dr. Ph. Reiß, im Juli 2007
Philipps-Universität Marburg Fachbereich Chemie
Ausarbeitung zu den
Übungen im- Experimental-vortrag Für L3-Studierende
Thema:
Kunststoffe
im WS 1999/2000
vorqeleqt von:
Yvonne Wallacher
An der Eiche 2
35274 Kirchhain
Kunststoffe
Yvonne WallacherInhaltsverzeichnis
1. Einleitung
1.1. Definition 3
1.2. Historisches 4
2. Darstellungsmethodenvon Kunststoffen . 6
2
.1.Polyaddition 8
Versuch 1: Darstellunqeines Polyurethans 9
2.2
.Polymerisation 12
Versuch 2: Oarsteüunq.eines PolyamidsPedon)_ _ 13 Demonstration 1: Veranschaulichung makromolekularer
Strukturen 16
2.3. Polykondensation 18
Versuch 3: Darstellung eines Phenoplasten 19
2.4. Weiterverarbeitung 23
3. Eigenschaften und Verhalten von Kunststoffen 24
3.1. Thermoplaste 24
3.2. Duroplaste 25
3.3. Elastomere 25
Damonstration 2: Kristallinität von Kunststoffen 26 Demonstration 3: Verstrecken des Polyamid-Rohfadens 28
4. Umwelt- und Recyclingaspekte
4.1. Der Weg des Mülls 30
4.2
.Verwertung 31
Versuch 4: Recycling von TetraPak 33
Versuch 5: Pyrolyse von Styropor 34
5. Literaturverzeichnis 3& -
2
Kunststoffe Yvonne Wallacher
1. Einleitung
3
Sehr passen für unsere Zeit ist der Ausspruch von Guilio Natta (Nobelpreisträgers für Chemie 1963) :
" Wenn unsere Zeit nach den Stoffen benannt würde, die sie charakterisieren[...], würde sie
als das Zeitalter der Kunststoffe in die Geschichte eingehen. Denn Kunststoffe, hergestellt aus synthetischen Makromolekülen, haben einen dominierenden Einfluß auf die moderne Industriegesellschaft gewonnen. "
Von morgens bis abends bedienen wir uns einer Vielzahl von Gebrauchsgütern, die aus Kunststoffen bestehen, so daß uns ein Leben ohne Kunststoffe kaum noch vorstellbar scheint. Andererseits wissen wir trotz des vielseitiqen Einsatzes von Kunststoffen und ihrer unterschiedlichen Erscheinungsformen sehr wenig über die Chemie der verschiedenen Kunststoffe. Das Gebiet der Kunststoffe, die früher auch als Plaste bezeichnet wurden , ist in wissenschaftlicher und technischer Hinsicht besonders in den letzten 4 Jahrzehnten enorm angewachsen und befindet sich noch immer in stetiger Aufwärtsentwicklung. Inzwischen gibt es zahlreiche Kunststoffe mit speziellen , zweckbestimmten Eigenschaften.
1.1. Definition
Unter Kunststoffen versteht man allgemein Materialien , die in ihren wesentlichen Bestandteilen organischer Natur sind, die aus Makromolekülen aufgebaut sind ("Polymere") und die durch Abwandlung von Naturprodukten oder durch Synthesen entstehen (Gemäß einem Definitionsvorschlag des Normenausschusses Kunststoffe im DIN). Kunststoffe sind in vielen Fällen unter bestimmten Bedingungen (Wärme und Druck) schmelz- und formbar.
Ihre Eigenschaften werden durch die ungewöhnliche Länge der kettenförmigen Moleküle sowie durch funktionelle Gruppen (Ester-, Amid- , Urethan-) bestimmt.
Als Polymer wurde ursprünglich ein Molekül aus vielen (griech. : poly = viel, mehrfach) Grundbausteinen (griech.: meros = Teilchen) bezeichnet. Heute wird jedoch nach IUPAC ein
"Polymer als eine Substanz definiert, die aus Molekülen aufgebaut ist, die sich durch vielfache Wiederholung von konstitutiven Einheiten auszeichnet und die so groß sind, daß sich ihre Eigenschaften bei Zugabe oder Wegnahme einer oder weniger der
konstituti\(~nEinheiten nicht wesentlich ändern."
Kunststoffe Yvoone Wa#acAer
1.2. Historisches (Eine Auswahl)
4
Natürlich vorkommende Polymere werden von der Menschheit schon seit Urzeiten verwendet, Die Proteine des Fleisches und die Polysaccharide des Getreides sind wichtige Nahrungsmittel. Wolle und Seide , beides Proteine , dienen als Bekleidung. Holz mit dem Hauptbestandteil Cellulose wird als Bau- und Brennmaterial verwendet. Bernstein , ein hochmolekulares Harz, wurde bereits von den Griechen als Schmuck getragen.
Im Jahr 1839 beobachtete E. Simon , daß Styrol beim Erhitzen von einer klaren Flüssigkeit in eine feste durchscheinende Masse übergeht, in ein Polystyrol im heutigen Sinne. Es waren die ersten Polymerisationsbeobachtungen bei Styrol. Ch. Goodyear gelingt ebenfalls 1839 die Vulkanisation von Kautschuk .
Baekeland stellte 1907nach intensiver Forschung Phenol - Formaldehyd - Preßmassen her.
Sein besonderer Verdienst war , die Beimengung an Säure oder Alkali so zu variieren , damit man technisch verwertbare Harze erhält. Auch die Anwendung von Druck bei der Aushärtung des Polykondensats , um möglichst blasenfreie Produkte herzustellen, wurde von ihm vorgeschalgen. Bereits im Jahre 1909 begann Baekeland mit der technischen Produktion des nach ihm benannten ersten vollsynthetischen Kunststoffs Bakelit.
1912 schuf Klatte die Grundlaqen für die Polymerisation von Vinylchlorid zu PVC. In einer Patentschrift wurde von ihm vorgeschlagen , PVC durch Lösen in Chlorbenzol und anschließendes Pressen durch Düsen in ein Fällbad zu Fäden zu verarbeiten. Die technischen Möglichkeiten, eine vollsynthetische Faser herzustellen , war 1912 noch nicht gegeben. Erst im Jahre 1928 in den USA und 1931 in Deutschland erlangten diese Vorstellungen praktische Anwendung.
Röhm suchte nach Herstellungsmöglichkeiten von .Glasqurnmi". Experimente erqaben zunächst ein einfacheres Herstellungsverfahren von Acrylsäure. Spätere Forschungen zeigten , daß Methacrylsäuremethylester sich für die Polymerisation besser eiqnet als Acrylsäureester.1928 war damit die Grundlage für Plexiglas-Herstellung gelegt. Die Produktion von Plexiglas konnte schon 1933 beginnen , da hier keine großen technischen Schwierigkeiten wie bei der Faserproduktion zu überwinden waren. Mit Plexiglas war ein vollsynthetischer Glasersatzstoff qefunden.
Carothers gelang es im Jahre 1930 erstmals , aus einer Schmelze von Hexamethylendiamin
und Adipinsäure Fäden zu ziehen . Mit diesem Polyamid hatte er Nylon entdeckt und 1931
wurde das erste Patent für Nylon angemeldet. Es dauerte allerdings noch sieben Jahre , bis
Kunststoffe
YVOIlReWa#acher 5
1938- erhielt Schlack aus reinstem s-Carpolactarn unter Zusatz von Spuren salzsaurer Aminocapronsäure bei einer Temperatur von 230°C eine hornartige Masse. Aus dieser Substanz ließen sich in der Schmelze Fäden ziehen. Die erkalteten Fäden erwiesen sich als äußerst fest und elastisch . I: G. Farben gab diesem Polyamid(6) den Decknamen Perluran, was später zu der Bezeichnung Perlon vereinfacht wurde. Die großtechnische Produktion begann 1939.
Bayer experimentierte mit mehrwertigen Alkoholen und Isocyanaten. Je nach Struktur der Ausgangsstoffe erhielt er durch Polyaddition entwerder vernetzte oder lineare Makromoleküle. In Jahr 1939 gelang es, Fäden aus Polyurethanen herzustellen, die aber im Vergleich zu Nylon und Perlon teurer und weniger haltbar waren . Neue Einsatzmöglichkeiten für Polyurethane ergaben sich, als man die Schäumbarkeit dieser Kunststoffe erkannte. Der Schäumvorgang wird durch Spuren von Wasser bei dem Additionsvorgang erreicht.
Die vom Ethen abgeleiteten Moleküle konnten schon frühzeitig polymerisiert werden , aber
dies gelang lange Zeit nicht bei dem so einfach gebauten Ethen. Als Haupthindernis stellte
sich der gasförmige Zustand des Monomeren dar . Im Jahr 1933 wurde ein Verfahren zur
Polymerisation von Ethen bei 200 bar und 200°C in Gegenwart geringer Sauerstoffmengen
entwickelt. 1953 gelang es Ziegler unter Verwendung bestimmter aluminium-organischer
Verbindungen und Titanterachlorid , Ethen bei "Zimmertemperatur" und Normaldruck zu
polymeristeren. Die verwendeten Initiatoren verhindern die sonst häufigen
Kettenabbruchsreaktionen des Hochdruckverfahrens , wodurch der Aufbau langkettiger
Polyethen-Moleküle möglich wurde. Das Niederdruck-Polyethen ist wärmestabiler und
mechanisch belastbarer als Hochdruck-Polyethen.
Kunststoffe Yvonne Wallacher
2. DarsteHungsmethoden von Kunststoffen
6
Wie der Name schon sagt, werden Kunststoffe auf künstlichem Wege (synthetisch) hergestellt. Ihre Herstellung erfolgt immer durch Verknüpfung vieler kleiner Moleküle (Monomere) , welche Mehrfachbindungen oder mindestens zwei funktionelle Gruppen besitzen müssen, zu den großen Makromolekülen (Polymere) der Kunststoffe. Dies läßt sich vereinfacht mit dem Bau eines Turms -aus vielen kleinen LEGO® -Steinen vergleichen , der später eine neue und größere Gestalt besitzt , als die einzelnen Teilchen zuvor. Die zur Herstellung von Kunststoffen verwendeten Monomere sind zum Teil Produkte der Erdölaufbereitung bzw. aus diesen synthetisiert. Inzwischen wurden aber auch schon eine Reihe von Kunststoffen entwickelt , die aus nachwachsenden Rohstoffen hergestellt werden können .
Trotz des ähnlichen Prinzips der Herstellung polymerer Verbindungen, sind die Reaktionen , die zur Verknüpfung der Monomere führen, verschieden. Je nachdem , welche chemischen Eigenschaften die Monomere besitzen , lassen sie sich durch Polymerisation , Polykondensation oder Polyaddition miteinander verknüpfen.
Allgemeines Reaktionsschema:
Meist reagiert ein elektrophiles Monomer mit einem nucleophilen Monomer zu einem Dimer mit einem elektrophile und nucleophilen Ende. Diese Enden können wieder mit entweder nucleophilen oder elektrophilen Monomeren zu einem Polymer reagieren.
+
Kunststoffe
Yvonne Wallacher 7
Reagiert ein Monomer mit z
.B. drei elektrophilen Enden mit einem Nucleophil, so entstehen vernetzte Polymere
.+
Kunststoffe
Yvonne Walfacher2.1. Polyaddition
8
H~r~i
werden durch wiederholte Addition von Monomeren mit bis- oder polyfunktionellen Edukten über reaktive Oligomere Polymere gebildet. Die Edukte sind meistens Diisocyanate, die mit Diolen bzw. Diaminen verknüpft werden. Bei der Additionsreaktion kommt es dabei zu keiner Abspaltung niedermolekularer Stoffe. Während -der Reaktion kommtes-zueiner Umlagerung von Wasserstoff-Atomen.
Die Polyadition läßt sich einteilen in die Unipolyaddition, bei der zwei unterschiedliche Monomerentypen verwendet werden, und die Copolyaddition , bei der mehr als zwei Monomerentypen verwendet werden. Die Reaktionsprodukte der Polyaddition heißen Polyaddukte .
Allgemeines Reaktionsschema:
Rektion eines Diols mit Diisocyanat:
HO-R1_0H
+O=C=N-R2-N==C=O
I IJ
_Q-RI_O-C-NH-R2..-NH::-C-
" "
o 0
111
Reaktion eines Diamins mit Diisocyanat:
n
~N-R1_NH2+ n O=C=N-R2-N=C=O
.. tNH-R1_NH-C-NH-R2-NH-Ct
" 11
o 0
nI
Quelle: Römpp
Kunststoffe Yvonne Wallacher
Versuch 1: Darstellung eines Polyurethans
9
HmtNeise :
1. Dimethylformamid dient als tose- bzw. Ouellmittelfür die Stärke
2. Wasserzusatz ist zum Schäumen nicht notwend ig, da Stärke ausreichend Wasser enthält.
3. Kein Reagenzglas nehmen, da hiermit die Schaumbildunqnlcht gelingt.
4. Dieser Versuch gelingt auch mit Glucose oder Saccharose . Diese Zucker lösen sich in Dimethylformamid.
Material:
Becherglas (50 ml), beheizbarer Magpetrünrer, Tieqelzanqe
Chemikalien :
Stärke , Dimethylformamid (Xn), Dfpnenyfmetfian-4,4=difsocyanat (Xi)
Durchführung:
In dem Becherglas werden 6 q Stärke und 18 ml Dirnethyltorrnamid aufgeschlämmt. (Zucker werden dabei gelöst.) Dazu werden 15 g Diisocyanat gegeben und vermischt. Man erhitzt die Mischung , bis die Reaktion (erkennbar am Aufschäumen) einsetzt. Lanqsarn abkühlen lassen.
Beobachtung :
i
Es bildet sich ein gelber PU-Schaum , der nach dem Abkühlen hart wird.
Reaktion (Formal):
OH
n Stärke
- - - 1. .~
Polyurethan
Diphenylmethan-4,4- diisocyanat
Kunststoffe Yvonne Wallacher
-Reaktionsmechan1ßmus :
R- O- H
+
" 6 = C = N -R-N=C=D-~
- ~
/10
\~
~ ~C - N -R-N C 0
R- O/
I /
H
\ '
C - N -R - N - Cjö/
R - o/ i I "'u-R
H H
Nebenreaktionen:
~=C=N-R-N-C ~ +
H,O -(~-C N- R-!-c(/)
"6=C N -R-N=C=D-
+
H2N-R-N=C=0',
/ /-'6"
. . ? : _ _
tt
~ H ~O - C - N - -R - - N - C - N -R-N c=o
<, /
Kunststoffe Yvonne Wallacher
Beispiel für ein Polyurethan:
Weichschaumstoff
Eigenschaften:
• Offene Poren
• Bis ca . 100 "C temperaturbeständig
• Bis ca. - 40 "C elastisch
• Bedruckbar
• Unbeständig
g~genheißes Wasser , starke Säu ren oder Laugen
Verwendung:
• Matrazen
• Polstermöbel
• Schwämme
• Kissen
11
Kunststoffe Yvonne Wallacher
2.2. Polymerisation
12
Hierbei werden Monomeren mit Kohlenstoffdoppelbindungen oder Ringen häufig unter Anwesenheit eines Initiators wie Radikale oder Ionen in einer Kettenreaktion zu linearen Makromolekülen verknüpft, indem weitere Monomeren an die Kette angelagert werden. Der Kettenwachstumsmechanismus wird ebenfalls durch Wärme , Licht, ionisierende Strahlung ausgelöst. Die Kettenreaktion läuft in der Schrittfolge Start-, Wachstums- und Abbruch- Reaktionen ohne Bildung von Nebenprodukten und ohne Skelettumlagerungen ab. Die Kettenlänge läßt sich dabei durch Zugabe von Reglermolekülen steuern. Wurde die Kette einmal abgebrochen, so wachsen die vorliegenden Moleküle nicht mehr nach dem gleichen Reaktionsmechanismus weiter.
Die Reaktionsprodukte der Polymerisation werden als Polymerisate bezeichnet.
Man unterscheidet je nach den verwendeten Katalysatoren zwischen radikalischer, ionischer und koordinativer Polymerisation.
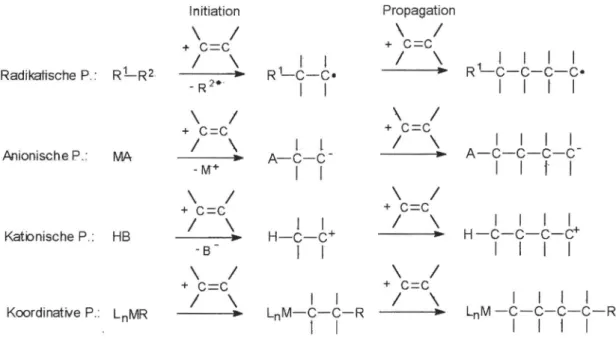
Allgemeines Schema:
Initiation Propagation
\ / \ /
+
c=c
+c=c
/ \
1I I / \
1I I I I
RadikatTsche P.: RLR2. ~ R
-c-c.
~ R-c-c-c-c·
- R
z· · I I I I I I
\ / \ /
+
c=c
+c=c
/ \ I 1 / \ I I I I
AnionischeP.: MA ~ A-C-C-
..
A-C-C-C-C-M+
I I I I f' I
\ / \ /
+
c=c
+c=c
/ \
JI / \ I I I I
Kationische P.: HB
..
H-C-C+..
H-C-C-C-C+-8
I I I I I I
\ / \ /
+
C=C
+C=C
/ \ I
I/ \ I I I I
Koordinative P.: LnMR ~ L M-C-C-R ~ L M -C-C-C-C-R
n I l n
I I
jI
Abbildung entnommen aus Römpp
Kunststoffe Yvonne Wallacher
Versuch 2: Darstellung eines Polyamids (Perlon)
13
Material :
:2 Stative, 2 Doppeimuffen, Reagenzgiaskiammer, Reagenzgias, Aktivkohie-Adsorber- Stopfen (passend zum Reagenzglas), Kühlerklemme, Heizluftfön, Messer, Pipette, 2 Glasstäbe
Chemikalien :
e-Caprotactarn
(frisches und trockenes), Natrium unter SChutzfJüssigkeit
Aufbau:
Heißluftfön
Aktivkohte-Adsoroer
s-Caprolactarn I
Abstand:2 -3cm
Durchführung :
In
das Reagenzglas werden etwa 2,5 9. (etwa 3 cm hoch)
c-Caprolactamgegeben. Mit dem
Heißluftfön (Einstellung. Etwa 120°C) wird das e-Caprolactam (Smp.: 69°C, Sdp.: 269°C)
unter Drehung des Reagenzglases mit der Hand geschmolzen. Ist die Masse geschmolzen
(klar und farblos) wird das Reagenzglas kurz senkrecht gestellt und ein möglichst
krustenfreies Stück Natrium (etwa 1 rnm") zur Schmelze gegeben. Nachdem das Natrium
vollständig reagiert hat (wenige Sekunden; die Schmelze sollte immer noch hell klar und
nicht bräunlich verfärbt sein) und das Reagenzglas währenddessen in die
Schräqstellunqzurückgebracht wurde, wird der Heißluftfön auf 400°C gestellt und die Schmelze möglichst
schnell zum Sieden gebracht (bleibt man knapp unter dem Siedepunkt , zersetzt sich die
Masse (dunkelbraune bis schwarze Verfärbung)). Nach 1 - 2 Minuten wird die Schmelze
zähflüssiger und beginnt sich gelblich zu färben, bleibt aber klar. Der Heißluftfön wird
abgestellt und man läßt die Schmelze etwas abkühlen, aber nicht erstarren Oe heißer die
Kunststoffe
Yvonne Wallacher 14
Schmelze ist, desto weniger viskos ist sie; ist die Schmelze zu dünnflüssig , lassen sich schwer Fäden ziehen). Mit einem Glasstab kann nun etwas klebriges Produkt entnommen werden, das mit einem zweiten Glasstab zu einem Faden gezogen wird; wenn die Schmelze schon stärker abgekühlt ist, kann ein Faden direkt aus dem Reagenzglas heraus gezogen werden. Zur weiteren Verarbeitung sollten die gezogenen Fäden so dick wie möqlich sein;
dies gelingt mit zunehmender Abkühlung der Schmelze immer besser .
Nachdem die Fäden vollständig abgekühlt sind, können sie weiterverarbeitet werden.
Ergebnis :
Man kann aus der Schmelze gelbliche Fäden ziehen.
Reaktionsmechanismus :
Sonderfall der Polymerisation
H
0\ . .
u\+
Na - 1/2~•
Na(B...
• .N~
(1
H'
H
Cf
Kunststoffe Yvonne Wallacller
Perlon
Eigenschaften von Perlon:
• Teilkristallin
• Faserartig
• Hochschmelzend
• Vergilben an Luft
Verwendung:
• Synthesefasem
• Schläuche
• Formteile
n
15
Kunststoffe
Yvonne Wallacher 16
Man kann makromolekulare von niedermolekularen Verbindungen auf rein phänomenologischer Ebene durch den sogenannten Tyndall-Effekt unterscheiden. Lösungen von Polymeren streuen das auftretende Licht in alle Raumrichtungen , so daß der Strahlengang einer punktförmigen Lichtquelle für den seitlichen Betrachter sichtbar wird . Lösungen niedermolekularer Verbindungen werden dagegen ohne sichtbare Lichtstreuung passiert.
Demonstration 1: Veranschaulichung makromolekularer Strukturen
Material:
Starke, gut fokussierbare Lichtquelle, zwei Reaqenzqläser , Reagenzglasstähder, passende Gummistopfen , dunkeln Hintergrund, Stativmaterial , Doppe/muffen, Stativklemmen
Chemikalien :
Styropor, Essigsäureethylester
Durchführung :
Man stellt sich von dem Styropor eine 5%ige-Lösun9. her (als Lösungmittel wird Essigsäureethylester benutzt), in das eine Reagenzglas gegeben und mit einem Gummistopfen verschlossen. Falls es notwendiq ist wird die Lösung zuvor filtriert (bei Schwebstoffen).
In das andere Reagenzglas füllt man Esslqsäureethylester als Blindprobe . Es ist darauf zu achten, das die beiden Flüssigkeiten die gleiche Flüssigkeitshöhe haben.
Probenlösung und Blindprobe werden nacheinander in den Strahlengang der Lichtquelle gehalten.
Beobachtung :
Polymerlösung: Strahlengang sichtbar
Klare Lösung: kein Lichtstrahl sichtbar
Kunststoffe Yvonne Wallacher Erklärung:
;','{,'.-': ",.-".-.-'.:. ....-~.-:.>:,.-. '·:·'-.·-e,'
·· '! Trübungsmessung"
Als Tyndall-Effekt kann man bei diesem Versuch das Streulicht erkennen.
17
Kunststoffe vvonne Wallacher
2.3. Polykondensation
18
Hierbei werden Monomeren mit zwei oder mehr funktionellen Gruppen in einer Stufenreaktion über Oligomeren zu Polymeren verknüpft, wobei die Verknüpfung der Monomeren unter Abspaltung kleiner Moleküle (meist Wasser, Alkohole oder Halogenwasserstoffe) erfolgt. Bei bifunktinellen Monomeren führt die Polykondensation zu linearen, thermoplastischen Kunststoffen, bei höherfunktionellen zu vernetzten, duroplastischen Kunststoffen. Entsprechend der Anzahl der unterschiedlichen Monomeren wird zwischen den Unipolymerisationen (bet ein oder zwei) und den Copolymerisationen (bei mehr als zwei) unterschieden.
Die Reaktionsprodukte der Polykondensation werden als Polykondensate bezeichnet.
Allgemeines Schema:
Kondensation von Disäuren mit Diolen:
Disäure Dlol
Polykondensation der Adipinsäure mit Hexamethylendiamin:
~-ln-liHf>
°f
11 H°1
"HO....C~C N~N...C~C ·N~NH 2
H
n r r
11 0
o
~2Nylon
Kunststoffe Yvonne Wallacher
Versuch 3: Darstellung eines Phenoplasten
Material:
Reagenzglas, Wasserbad, heizbarer MagnetrUhrer, Stativmaterial
Chemikalien :
Resorcin, Formaldehyd-LösungJw = 37%1, Verdünnte KOR-Lösung (ca. 2 %)
19
Durchführung:
In einem Reagenzglas werden zwei Spatel Resorcin in etwa gleichviel Formaldehyd-Lösung aufgelöst. Dann gibt man einige Tropfen verdünnter KOH-Lösung hinzu und erhitzt das Gemisch im Wasserbad .
Beobachtung :
Unter Blasenbildung verfärbt sich das Gemisch rotbraun, wird zähflüssig und verfestigt sich.
Der entstandene Kunststoff läßt sich anschließend durch vorsichtiges Erhitzen aus dem Reagenzglas austreiben.
Reaktionsmechanismus :
1.) Bildung des Elektrophils
- -
H " C=-=O
:::-....+
/ @ "-
H H
Kunststoffe Yvonne Wallacher
2.) Elektrophile Substitution am Aromaten
OH OH
20
H '\.
:--..C=-=-=O
/ <±> "-
H H
HO
OH
HO
Rote Pfeile: Angriffspunkte des Elektrophils
3.} Bildung des
"zweiten Elektrophils" und nachfolqendeSE
HO
OH
HO
OH
HO
+~ HOA) OH
Kunststoffe Yvonne Wallacher
OH
HO
OH
HO
Rote Pfeile
:nächste Angriffspunkte
4.) Nebenreaktion
OH
<±)
..CH
2HO
OH
+
OH
OH
OH OH
OH
OH
OH
21
HO
OH
HO
OH
Kunststoffe Yvoone Wallac-aef Phenoplast
Eigenschaften:
• Löslich in Alkohol,Aceton,niedrige Ester
• Für viele Zwecke zu spröde
• In Gegenwart von O2: Bildung von Chinonmethin q Vergilben der Phenolharze
Verwendung:
• Fasern
• Ersatz für ScheHack
22
Kunststoffe Yvonne Wallac-her
2.4. Weiterverarbeitung
23
Um brauchbare Kunststoffe zu erhalten, werden den polymeren Rohprodukten Hilfsstoffe zugesetzt, z. B:
Weichmacher (z.B. Alkohole) beseitigen Härte und Sprödheit von Kunststoffen
Füllstoffe (z.B. Holzmehl, Kreide, Ruß) verleihen mechanische Festigkeit, z.B. gegen Abrieb .
Stabilisatoren verhindern das Altern der Kunststoffe, bedingt durch Wärme, Licht oder Sauerstoff.
Gleitmittel verbessern die Verarbeitungsmöglichkeiten der Kunststoffe Farbstoffe verleihen ein schöneres Aussehen
Antistatika setzen die statische elektrische Aufladung von Kunststoffolien herab.
Verarbeitung :
Es können die aus der Metallverarbeitung bekannten Verfahren verwendet werden. Für thermoplatische Polymere eignet sich auch die Verarbeitung durch Warmverformen wie:
Hohlkörperblasen:
Das erhalten Hohlprofil (z. 8- . ein dünnes Rohr) wird kontinuierlich aufgeblasen (z. B. zu Flaschen oder Kanistern).
Extrudieren:
Das Ausgangsmaterial kommt vorwiegend als Granulat in den Handel, das durch Extrudieren und anschließendes Abschlagen der abgekühlten Drähte hergestellt wird. Das erneut aufgeschmolzene Material wird kontinuierlich durch eine Düse gedrückt. Man erhält z. B.
endlose Rohre oder Folienbahnen. Fasern werden z. 1. in ähnlicher Weise hergestellt.
Spritzgießen :
Das aufgeschmolzene Material wird durch eine Düse in die Spritzform gespritzt. Das
geformte Stück wird nach dem Erstarren ausgestoßen ; die Maschine arbeitet taktweise.
Kunststoffe
Yvonne Wallacher3. Eigenschaften und Verhalten von Kunststoffen
24
Zwei grundlegende Materialeigenschaften von Kunststoffen sind uns aus dem alltä9.!.ichen Gebrauch und alltäglichen Erfahrungen bekannt. So wissen wir , daß z.B . eine Plastiktüte unter dem Einfluß starker Hitze (z.B. einer heißen Herdplatte) zu schmelzen beginnt, während ein Kochlöffel dieses unbeschadet überstehen würde. Weiterhin kennen wir aus dem Alltag Kunststoffe, die unter dem Einfluß mechanisch einwirkender Kräfte ihre Form behalten , während sich andere , wie z.B. Gummis, dehnen lassen und später ihre ursprüngliche Form wieder einnehmen. Sie zeigen ein elastisches Verhalten. Diese zwei Materialeigenschaften, das Verhalten gegenüber Erwärmung und die Elastizität, werden auch zur Einteilung der Kunststoffe herangezoqen. Thermisch verformbare Kunststoffe heißen Thermoplaste, hitzebeständige Kunststoffe werden als
Duroplasteund elastische Kunststoffe als
Elastomerebezeichnet. Diese verschiedenen Eigenschaften der Kunststoffe basieren auf ihrem unterschiedlichen molekularen Aufbau. Kunststoffe bestehen aus sehr großen Molekülketten (Makromolekülen), die unterschiedlich angeordnet und vernetzt sein können .
Man kennt weiche , elastische. zähe-und spröde Kunststotfe. Sie zeichnen sieh im Geqensatz zu Naturstoffen durch besondere Eigenschaften aus: Geringe Härte, hohe Dehnbarkeit, geringeDichte, geringe Wärmeleitfähigkeit, große Schalldämpfung .
3.1. Thermoptaste
In Thermoplasten liegen die Makromoleküle hauptsächlich nebeneinander vor.
WiF~ein solcher Kunststoff erwärmt , können die Moleküle aneinander entlanggleiten und der Gegenstand verformt sich. Beim Abkühlen erhärtet der Kunststoff zu einer neuen F.orm.
Thermoplastische Kunststoffe wechseln in einem größeren Temperaturintervall vom weichen in den flüssigen Zustand, die Makromoleküle werden bei diesem Vorgang chemisch nicht verändert. Bei hoher Temperatur lassen sich thermoplastische Kunststoffe in unterschiedliche Formen pressen, nach der Abkühlung gewinnt man ein festes Formtell.
dieses Verfahren wird bei der Verarbeitung thermoplastischer Kunststoffe genutzt.
Kunststoffe Yvonne Wallacher
3.2. Duroplaste
25
Die Duroplaste sind aus Makromolekülen autqebaut, die engmaschig miteinander vernetzt sind. Dabei entstehen zwischen den Molekülen feste Bindungen, so daß die Moleküle beim Erhitzen nicht aneinander vorbeigleiten können.
Duroplastische Kunststoffe werden bei hohen Temperaturen nicht weich oder flüssig . Aus diesem- Grund-müssen sie-bereits bei der Synthese- die gewünschte Endterm
emaltefl;~nach dem Aushärten kann ein duroplastischer Gegenstand nur mechanisch bearbeitet werden .
3.3. Elastomere
!Die- Makromote\{ü!e- der Elastomere- bilden dichte- "Knäule-" . Beim Dehne-n eines Gegenstandes aus Elastomeren werden die "Knäule" auseinandergezogen. Läßt man den Gegeflstandwteder-los, "verknäulen" sich- die-MolekQleemeut.
Elastomere verhalten sich bei mechanischer Belastung wie Gummi , sie lassen sich leicht vetferme-n und kehren danach in ihrer ursprflngliche-n Form zurück. Erwärmt--man gespa,nnte Elastomere, schrumpfen diese. Bei der Verarbeitung von Elastomeren werden sie unter Einwirkung von,Hitze und Druck in der Endform synthetisiert.
Bei ausreichend tiefen Tempe raturen sind alle Polymere fest, wobei sie zumeist teikristallin vorliegen, d. h. es gibt in Polyme-re-n in der Regel sowohl amorphe ats- aueh kristalline Bereiche. Ob ein Polymer kristallisierbar ist oder nicht, hängt zunächst einmal von strukturellen- Faktoren ab . WiGh-üge Voraussetzunqen für cüe Krlstallisaäon sind lineare Ketten , Taktizität und intermolekulare Wechselwirkungen .
Unter anderem hängt die Kristalisation auch von der Abkühlungsgeschwindigkeit ab. So führt ein rasches Abkühlen eher zu einer glasigen Erstarrung des Polymers , thermodynamisch betrachtet zur Bildung eingefrorener Ungleichgewichtszustände. Die Konsequenz sind weitgehend amorphe Strukturen und höhere Transparenz des erstarrten Materials.
Langsames Abkühlen hat dagegen höhere-Kristallinität des festen Polymers zur Folge, das Material erscheint daher trüber . Dieser Effekt läßt sich sehr einfach mit einer Probe Polyethylenterephthalat zeigen , welches- üblicherweis-e für Mehrwegflaschen (z. B.
Colaflaschen) verwendet wird.
Kunststoffe Yvonne Wallacher
Demonstration 2: Kristallinität von Kunststoffen
26
Material:
Stativ, Doppelmuffe, Kühlerklemme, HeißTuftfön, heizbarer Magnetrührer, 25 mL S-echerglas (sehr sauber)
Chemikalien:
Polyethylenterephthalat (PET) (Getränke-, Spülftaschen)
Aufbau:
KOhJer1<1emme
Abstand:
etwa1cm
PET·Stücke
Durchführung:
Das Becherglas wird mit etwa- 3 9..PET
9..~füJltund auf den Magnetrührer
g~stellt,dessen Heizplatte auf etwa 300°C gestellt wird. Von oben wird mit dem Heißluftfön beheizt (etwa 300 Oe)
.Betm Aufheizen ist es empfehlenswert, zunächst eine niedrige Gebläsestufe zu wählen, bevor man nach etwa 30 Sekunden die maximale Stufe einstellt. Damit erreicht man ein Zusammenbacken der oberen PET-Stücke
,ohne daß sie herausqewirbelt werden.
Sollten während der Aufheizphase einige Stücke, vornehmlich in den Randbereichen noch
nicht geschmolzen sein
,wird das Becherglas per Hand (=> Lederhandschuhe) durch Drehen
entsprechend in Position gebracht. Es werden nun Heizplatte und Fön abgestellt; das
Becherglas bleibt auf der Platte stehen
.Nach weiteren 5 - 7 Minuten kann es atJf den
kühleren Labortisch gestellt werden. Während des Abkühlens kann das Kristallisieren
anhand der auftretenden Trübung beobachtet werden
.Ist die Schmelze auf Handtemperatur
Kunststoffe
Yvonne Wallacher
27
außen noch einmal kurz (10 - 20 Sekunden) mit dem Heißluftfön (300
Oe)erwärmt. Meistens läßt sich spätestens jetzt das kristallisierte PET herauslösen
.Erklärung:
Übergang von amorphen Strukturen in teilkristalline Strukturen,
amorph
f1üssigkristallin
Kunststoffe Yvonne Wallacher
Demonstration 3: Verstrecken des Polyamid-Rohfadens
Material:
Stativstange, Filfierring, Nähfäden, kreine PE=Fläschen
Chemikalien :
Der in Versuch 2 hergestellte
~ohfaden28
Durchführung :
Ein auf die Weise in Versuch 2_ gezogener Rohfaden ist nicht maximal belastbar. Er muß vielmehr noch weiter .verstreckt" werden. Dazu wird er langsam durch Zug solange belastet , bis sich weiterer Streckung ein erhöhter Widerstand entgegensetzt.
Man befestigt den Rohfaden mit normalen Nähgarn .an dem Filtrierring und hängt unten ein PE-Fläschen an den Rohfaden ._Dann füllt man vorsichtig_ Wasser in das Fläschen.
Beobachtung:
Der Faden verlängert sich und wird dünner.
Erklärung :
Bei der Verstreckung kommt es zur Ouerschnittsverrinqerunq.
Die enorme Reißfestigkeit der Fäden ist auf die Ausbildung der maximalen Anzahl von intermolekularen Wasserstoffbrückenbindungen zwischen gestreckten Zick-Zack-Strukturen im Polyamid-6 zurückzuführen.
~o . .. . "~~~ . . - J o .. "~!
I-t--N-
o
Kunststoffe Yvonne Wallacher
Nachteile von Kunststoffen:
• geringe mechanische Festigkeit
• geringe Formbeständigkeit in der Wärme
• Anfälligkeit gegen Alterung
• Brennbar (wegen organischer Natur)
• teure Abfallbeseitigung
• Einwegprodukte
• Schwierig auszubessern, Reparatur lohnt nur selten
29
Kunststoffe
Yvonne Wallacher4. Umwelt- und Recyclingaspekte 4.1. Der Weg des Mülls
30
Kunststoffe dienen häufig als Verpackungsmittel und Einwegartikel
,so besteht 1/3 des gesamten Hausmülls aus Verpackungen. Problematisch ist die große Menge von Kunststoffabfällen und deren verschiedene Zusammensetzung
,zudem besitzen viele Kunststoffe eine große Beständigkeit.
Was passiert eigentlich mit einem Quarkbecher, nachdem er in den gelben Sack eingeworfen wurde.
Der Quarkbecher wird zu Müll und landet im gelben Sack. Er wird abgeholt und in der Sortieranlage ausgekippt. Der Becher landet auf einem Fließband
,auf dem der Müll von Hand sortiert wird. Der aussortierte Kunststoff wird verladen und zur Methanolsynthese nach Schwarze Pumpe gebracht. Für den Transport werden über 2001 Diesel verbraucht. Hier wird aus dem Kunststoff Methanol synthetisiert, welches als Lösungsmittel in Klebstoffen und Farben eingesetzt wird. Natürlich wird nicht jeder Becher zu Methanol verarbeitet.
Das Duale System Deutschland, DSD, läßt jährlich etwa 600.000 t Kunststoffe sammeln und führt diese Kunststoffmenge einer Verwertung zu. Laut Gesellschaft für Kunststoffrecycling, DKR (VDlnachrichten 5/99) ist für 1-999 geplant: Sammlung von 594.000 t Kunststoffverpackungen.
250.000 t (42 %) fließen in die werkstoffliche Direktverwertung, davon ca. 80 % bzw. 2QQ.000 t als getrennte Fraktionen (Flaschen
,Folien, Becher). Die Verwendung der getrennten Fraktionen ist aufgrund fehlender Marktakzeptanz der Produkte nicht gesichert. 260.000 t (44
%) sind für rohstoffliche Alternativen vorgesehen. Verwendung: Als Reduktionsmittel zur
Stahlerzeugung (Stahlwerke Bremen und Ekostahl); Methanolgewinnung (Schwarze Pumpe,
Brandenburg); ötgewinnung (Veba Bottrop). In der Planung ist eine Mitverbrennung in
Zementwerken und zur Schwefelsäureherstellung. Im November 1999 wurde eine neue
vollautomatische Sort
ieranlage- Sortec 3.0 - in Hannover vorgestellt
,die die Wertstoffe aus
Gelben Säcken der EXPO 2000 sortieren und die Kunststofffraktionen PE, PS und PET
aufarbeiten soll; Stundenkapazität: 5000 kg.
Kunststoffe Yvorme Waltacher
4.2. Verwertung
31
BeLder KunststoffDeseitigung gibt es zwei Möglichkeiten , entweder deren Vernichtung oder die Wiederverwertung (Recycling) .
Nach -§- 5 Abs-. 2 des Kreis1attfwirtschafts-/Abfallgesetz hat der Erzeuger oder Besitzer von Abfällen diese zu verwerten . Nach § 6 desselben Gesetzes bestehen hierzu verschiedene MögOChkeiteA-. Grundsätzfleh können AbfäUe, und damit auch Kunststoffabfälle entweder stofflich verwertet werden oder zur Gewinnung von Energie genutzt werden. Vorrang hat bei der Verwertung die umweltverträglichere Verwertunqsart.
Energetische Verwertung:
Eine energetische Verwertung von Abfällen ist nach dem Abfallgesetz nur dann- zulässig , wenn der Heizwert des einzelnen Abfalls , ohneVermischung mit anderen Stoffen , mindestens 1-100e- kJ/kg beträgt Typische Polymere wie PE, PP und PS_haben einen weitaus höheren Heizwert von 42000 kJ/mol, der in derselben Größenordnung wie der von Heiz öl liegt.
DieVerbrennung erfolgt typiscberwelse in Drehrohröfen . Die etwa 900 bis- 1200
°C heßen Verbrennungsgase werden in einen Wärmetauscher geleitet , wo sie Wasserdampf erzeugen , der zum Heizen oder StromgE3winnung genutzt wird. Die auf etwa 250 bis 300°C abgekühlten Verbrennungsgase durchlaufen noch eine Ruchgasreinigungsanlage und werden anschließend über einen-Kamin aR-die Umwelt angegeben .
Rohstoffliche Verwertung :
Die rohstoffliche Verwertung hat das Ziel, Kunststoffabfälle
~u rchDepolymerisationsreaktionen (je nach Polymer Solvolyse, Hydrolyse , Pyrolyse) , also unter Abbau ihrer makromolekularen Strukturen in nutzbare niedermolekutare Verbindungen umzuwandeln. Vorteil rohstofflicher Verwertungsverfahren ist allgemein, daß die aufwendige Vorsortierung und Reinigung entt
ällt.Bei der Pyrolyse werden die Kunststoffabfälle unter Ausschluß von Sauerstoff erhitzt und damit in ihre chemischen Bestandteile zerlegt. Dabei entstehen flüssige und gasförmige Produkte , die als Brennstoffe oder als Chemierohstoffe geeignetverwertbar sind.
Problematisch an diesem Verfahren ist einerseits die Trennung und Aufbearbeitung der
Pyrolyseprodukte und andererseits. die, Tatsache ... . daß., dieses Verfahren. _ nur
Kunststoffprodukte zuläßt, d.h. der Hausmüll muß vorher sortiert werden.
Kunststoffe
Yvonne Wallacher
32Werkstoffliche·Verwertung:
Bei der werkstofflichen Verwertung. von Kunststoffabfällen soll die makromolekulare Struktur erhalten bleiben. Aus Abfällen soUen nicht durch chemische Reaktion sondern über physikalische Prozesse neue Kunststoffrohstoffe erzeugt werden.
Für diese Art von Recycling können normalerweise nur reine Kunststoffe verwendet werden , die man extra sammeln muß. Das wird nur dort praktiziert, wo sehr große Mengen an Kunststoffabfällen auftauchen. Eine Verarbeitung von Kunststoffabfällen zu neuen Produkten kann durch Umschmelzen geschehen. Hierbei werden sortenreine, sowie auch unsortierte und verunreinigte Thermoplaste (z.B. PVC, Polyethen, Polystyrol usw.) durch Wärme, Druck und Lösemittel in neue Formen gegossen.
Schema zur Verwertung von Kunststoffen:
WerbtDfftiche -Rot-efn"icbe Energetische
Ve~ng V8rNertunll - V8f\Y8t1ung
l I I
Werkstoff bzw. o · MakromoIPOIa-f-_. MakromolekOIe
MalaomolekOIe werden Mrden
bhJiban.malten abgebaut verbrannt
..
I
'0
I =~-t-I
' : : : gI
~;..Hydltll)set" H =; t ' - -
WArme;Strom .I I l L
1
Regranulat11
Misehlcu _. IrI MORe.'. ,·~~ IKunststoffe
Yvonne Wa1l.a.cher
Versuch 4: RecycHng von TetraPak
33
MC!tfrial:
Heizbarer Mägnettührer mit Rührfisch, l\iteß"zyrtnder zs-
rnt,und
1Q()mt, Ehghals- Erlenmeyerkolben 250 mL, dazu passenden Gummistopfen mit einer Bohrung, Aktivkohle- Adsorber, Büchnertrichter oder Teesieb, Stativ, Doppelmuffe, Filtierring, Bechergläser (250 ml und 400 mL) Glasfilter, Filterpapier
Chemikalien:
Ethanol, TetraPak-SChnipsef, Xylol
Durchführung:
In einem_Erlenmeyerkolben werden 20 mLXylol und 1 gTertraPak-Schnipsel vorqeleqt, Man -, schließt den Kolben mit einem passenden Stopfen inkl. Aktivkohle-Adsorber und erwärmt die Mischung auf dem Magnetrührer. Das Xylol wird als Lösungsmittel für eine quantitative Bestimmung wegen des niedrigeren Dampfdruckes und einer notwendigen Mindesttösüchkett verwendet. Die-Schnipsellassen sich schnell mit einem guten Locher herstellen
.Innerhalb von 10 -15 Minuten wird nun unter Rühren auf ca. 120
0C aufgeheizt. Dann ahben sich Aluminium und Papier voneinander getrennt; PE und etwas Farbstoff ist in Lösung gegangen
.Mit einem Büchnertrichter (oder Teesieb): wird das Schnipselgemisch aus Aluminium und Papier von der PE-Lösung getrennt, indem man die Lösung langsam in ein mit 100 mL Ethanol
~efülltes250 mL Becherqlas filtriert
,Es entsteht sofort ein weißer NiderschlaQ, aus PE. Läßt man die Fällung wenige Minuten stehen, agglomeriert das PE zu gut sichtb~ren
Flocken,
I
Dann-wird der
PE-Niederschla~Lmiteinem Glastrichter mit Faltenfilter abfiltriert, im Abzug (1 Tag) oder im Ablufttrockenschrank (1 h bei 60° C) getrocknet und gewogen.
Zur quantitativen Überführung des Pes sollten die benutzten Bechgläser noch zweirnq) mit etwa 20 mL des letzten Filtrats ausgespütrwerden.
Ergebnis:
Einqewoqenes TetraPak: 3 g Erhaltene Masse an PE: 0,517 g
Gesamtmasse: 26,7 g
PE im TetraPak: 17,32%
Kunststoffe Yvonne WalJacher
Versuch 5: Pyrolyse von Styropor
Bau eines Pyrolyse-Stopfens
34
Material: Gummistopfen
,Glasrohr mit Pipettenspitze, Glasrohr, Bunsenbrenner, Glassäge, Aktivkohle-Adsorber
Bauanleitung:
,AkI:McDhIe.
gekömt
!-
! Kühlfinger
I
I _____
H
Der Gummistopfen wird zweimal durchbohrt, einmal für einen Aktivkohle-Adsorber und einmal für einen Kühlfinger.
Das Glasrohr mit der Pipettenspitze wird an der spitzen Seite zugeschmolzen. Auf diese Spitze wird das andere Glasrohr angesetzt. Dazu erhitzt man beide Teile in der Bunsenbrennerflamme, fügt sie zusammen und nimmt sie langsam aus der flamme nach oben heraus. Nach dem Abkühlen wird das angeschmolzene Stück auf etwa 1,5 cm gekürzt.
Das angesetzte Glasrohr vergrößert die Haftfläche des fertigen Kühlfingers und verhindert
ein zu leichtes Abtropfen des Kondensats.
Kunststoffe
Yvonne Wallacher-
Nachweis- der Doppelbindung:
35
Material:
Heizplatte, 3 Erlenmeyerkolben (25(t mt, enghatsig ; Z- x 25 mL, weithalsiq) . mit dazu passenden Gummistopfen , Pyrolyse-Stopfen , Trichter , 2 Pasteurpipetten mit Hütchen
Chemik~lien:
Sauberer und farbloser P5=M"illf, Plitfialsäuredieetf'lytester, B"rom in Phthalsäurediethylester, Eiswasser
Durchführung:
)
Zuerst wird die Eintauchtiefe des Kühlfingers so eingestellt , daß dieser sich kurz über dem Boden des 250 mL Erlenmeyerkolbens befinden . Dann werden beide 25 · mL Erlenmeyerkolben mit je 10 mL Phthalsäuredieethylester und etwa 1,5 mL der Bromlösung befüllt und mit Gummistopfen verschlossen .
In einem der 25 mL ErlenmeyeFkolben wird etwas PS aufgelöst, wobei sich die Lösung- nicht entfärbt (Blindprobe).
Der 250 mL Erlenmeyerkolben wird fast bis obenhin mit Pofystyrol befüllt und mit dem Pyrolyse-Stopfen verschlossen . Die Apparatur wird auf eine Heizplatte gestellt und erhitzt bzw. damit es schneller geht wird der Kolben über der Bunsenbrennerflamme- erhitzt. Der Kühlfinger der Apparatur wird mit Eiswasser befüllt. Es wird so lange erhitzt bis die PS-Probe geschmolzen ist und sich starker Nebel gebildet hat. Ist dies geschehen , wird die Heizquelle ausgeschaltet. Nach kurzer Zeit beobachtet man , daß am Kühlfinger Pyrolysat kondensiert ist.
Nachdem das Eiswasser abpfpettiert wurde, wird vorsichtig der Pyrolyse-Stopfen
i
herausgezogen und auf den anderen Erlenmeyerkolben mit der Bromlösung gesteckt. Es
kommt zu einer Entfärbung der Bromlösung , da sich das Brom an die Doppelbindung der
Produkte addiert hat.
Kunststoffe Yvonne WaJlacher
F.ormale
Reaktion:n Polystyrol
Reaktionmechanismus (Idealfall):
Il
Styrol
36
Ph
)
Kunststoffe Yvonne Wallacher
Nachweis der Doppelbindung:
37
+ J
-8
SrlKunststoffe
Yvonne Wartacner5. Literaturverzeichnis
38