Philipps-Universität Marburg Fachbereich Chemie
Veranstaltung: Übungen im Experimentalvortrag Sommersemester 2007
Protokoll
zum Experimentalvortrag
Kalk –
Das Gespenst in der Wasserleitung
vom 20.06.2007
vorgelegt von
Franziska Behrmann Zwischenhausen 5
35037 Marburg
Inhaltsverzeichnis:
0. Einführung……... S. 3
1. Kalk
1.1 Eigenschaften und Verwendung.……… S. 5
2. Wasserhärte
2.1 Was ist Wasserhärte?... S. 7 2.2 Bestimmung der Wasserhärte………... S. 9 2.3 Wie kommt die „Härte“ ins Wasser?... S. 13 2.4 Vor- und Nachteile von hartem Wasser……….. S. 20
3. Wasserenthärtungsmöglichkeiten
3.1 Ausfällen……… S. 24 3.2 Komplexieren……… S. 24 3.3 Auflösen……… S. 25 3.4 Ionenaustauscher……… S. 27
4. Kalk und Wasserhärte - Ein Thema in der Schule?... S. 32
0. Einführung
Dieser Vortrag, welcher sich mit dem Thema Kalk, Wasserhärte und den daraus resultierenden Eigenschaften und Folgen, sowie deren Bekämpfung beschäftigt, wird zunächst durch folgende Demonstration motiviert.
Demonstration 1: Eindampfen verschiedener Wasserarten
Geräte:
- 2 Wassergläser
- 2 farbige (schwarz, dunkelrot, blau, etc.) Unterteller - Wärmequelle (Ofen, Heizplatte, Bunsenbrenner)
Chemikalien:
- Leitungswasser - Entionisiertes Wasser
Durchführung:
Einen Teller mit Leitungswasser füllen, den anderen mit entionisiertem Wasser.
Anschließend das Wasser entweder unter Zuhilfenahme der Wärmequelle oder an einem sonnigen Platz verdunsten lassen. Jeweils ein Wasserglas mit der entsprechenden Wasserprobe neben den Teller stellen.
Beobachtung:
Obwohl beide Wasserproben optisch nicht voneinander zu unterscheiden sind,
hinterlässt die eine Wasserprobe weiße Ränder auf dem Teller, während der zweite
Teller sauber bleibt.
Auswertung:
Der weiße Rand tritt bei dem Leitungswasser auf und bleibt bei der Probe des entionisierten Wassers aus. Zurückzuführen ist dieses Phänomen auf die im Leitungswasser gelösten Ionen, welche beim entionisierten Wasser entfernt wurden.
Genauer gesagt ist es Kalk, welcher zunächst in gelöster Form als Hydrogencarbonat im Wasser vorliegt und beim Verdunsten des Wassers als weißer Rand auf dem Teller auskristallisiert.
3 2( ) 2 ( ) 2( ) 3( )
( ) aq Erwärmen g g s
Ca HCO H O CO CaCO
Diese Beobachtung, dass in einer der zwei zunächst völlig identisch aussehenden
Wasserproben etwas enthalten sein muss, dass jede Hausfrau täglich ärgert und
mehrere Stunden am Tag die Werbung füllt, gibt Anlass, sich genauer mit „Kalk –
dem Gespenst aus der Wasserleitung“ zu beschäftigen.
1.Kalk
1.1 Eigenschaften und Verwendung von Kalk
Kalk oder auch Calciumcarbonat (CaCO 3 ) ist ein weißer Feststoff mit einer Molmasse von 100,09 g/mol und einer Dichte von 2,71 g/cm 3 . Je nach Temperatur, bei der Calciumcarbonat kristallisiert, kommt es in mehreren Modifikationen vor.
Bei einer Entstehungstemperatur von unter 30°C entsteht Calcit, welches außerdem unter dem Namen Kalkspat bekannt ist. Calcit hat eine ditrigonal-skalendoedrische Kristallform.
Abbildung 1: Calcit-Kristall
Bei über 30°C wird Aragonit, bekannt als Perlmutt, gebildet, welches rhombisch-
dipyramidal aufgebaut ist.
Abbildung 2: Aragonit-Kristall
Aragonit bildet außerdem radialstrahlige bis büschelige Aggregate aus spitzpyramidalen Nadeln.
Zudem ist außerdem eine hexagonal-trapezoedrisch aufgebaute Form des Calciumcarbonats bekannt, welche jedoch sehr instabil ist und daher in der Natur praktisch nicht vorkommt.
In der Natur kommen diese Modifikationen in Kalkstein, Dolomit, Kreide und Marmor vor und bilden daher den Grundstoff vieler Gebirge.
Ein besonders schönes Beispiel, welches die beiden häufigsten Modifikationen vereinigt, ist eine Muschel, da deren Schale aus Calcit und das Innere aus Perlmutt (Aragonit) aufgebaut ist.
Kalkstein ist ein außerordentlich festes Rohmaterial und wird daher häufig für Baustoffe in Form von Steinen und Zement verwendet.
Veredelte Produkte von Kalk sind Branntkalk und gelöschter Kalk, sowie Deckweiß für Wandfarben und Calciumhydroxid (Ca(OH) 2 ), welches eine der billigsten Basen darstellt und somit sehr häufig industriell verwendet wird. Außerdem ist Kalk in vielen alltäglichen Dingen enthalten oder wird zu deren Herstellung benötigt. Einige Beispiele hierbei sind: Zahnpasta, Seife, Butter, Zucker, Waschmittel, Glas und Keramik, Düngemittel oder Schotter und Splitt im Straßenbau. Zudem kann Kalk sehr gut für Wasserbehandlung oder als Luftreiniger, z.B. bei Entschwefelung von Rauchgasen verwendet werden.
Jedoch soll sich dieser Vortrag nicht mit Kalk im Allgemeinen, sondern mit Kalk im
Wasser beschäftigen.
2. Wasserhärte
2.1 Was ist Wasserhärte?
Allgemein kann Wasserhärte als „Eigenschaft von Wasser, bei Anwesenheit von Calciumionen die Waschwirkung von Seife herabzusetzen“ definiert werden.
Chemikalisch betrachtet wird Wasserhärte durch so genannte Härtebildner verursacht. Dies sind im Wasser gelöste Calcium- und Magnesiumsalze in Form von Hydrogencarbonaten, Chloriden, Sulfaten oder Ähnliches.
Man unterscheidet dabei die so genannten temporäre und die permanente Härte.
Die temporäre oder auch zeitweilige bzw. vorübergehende Härte trägt zudem den Namen Carbonat-Härte, diese Form der Härte unter Bildung von unlöslichen Carbonaten durch Erhitzen entfernt werden kann. Im Haushalt ist dieser Vorgang als Bildung von so genanntem Kesselstein in Wasserkesseln zu beobachten.
3 2( ) 3( ) 2( ) 2 ( )
( ) aq s g g Kesselstein
Ca HCO CaCO CO H O
Die Calciumhydrogencarbonationen, welche für diese Härte verantwortlich sind, sind
als Substanzen nicht isolierbar, sie liegen folglich nur in dissoziierter Form als
hydratisierte Ionen vor.
Die permanente oder auch bleibende Härte wird auch Sulfat-Härte genannt. Sie wird durch die Calciumsalze der Salzsäure, Salpetersäure, Kieselsäure, etc. verursacht.
Diese Härte bleibt selbst beim Erhitzen von Wasser unverändert.
Die Summe aller im Wasser gelösten Salze ergibt schließlich die Gesamthärte des Wassers.
Angegeben wird die Wasserhärte bezogen auf die Konzentration der gelösten Erdalkali-Ionen in mmol/L oder °dH (Grad Deutscher Härte). Dabei gilt:
1mmol CaO/L = 56 mg CaO/L = 5,6°dH 1mmol MgO/L = 40,3 mg MgO/L = 5,6°dH.
Je nach Härtegrad können 6 Wasserhärtebereiche von sehr weich bis sehr hart unterteilt werden.
Härtegrad Härtebereich
0-4°dH sehr weich
4-8°dH weich
8-12°dH mittelhart
12-19°dH ziemlich hart
19-30°dH hart
>30°dH sehr hart
Mit Hilfe einer Wasserhärtemessung kann der jeweilige Wasserhärtebereich ermittelt
werden.
2.2 Wasserhärtebestimmung
Versuch 1: Bestimmung der Wasserhärte
Geräte:
- Bürette
- Erlenmeyerkolben
- Magnetrührer mit Rührfisch - Stativmaterial
- 100 mL Vollpipette
Chemikalien:
- Salzsäure (c = 2 mol/L) - Salzsäure (c = 0,01 mol/L) - Natronlauge (c = 2mol/L) - EDTA-Lösung (c = 0,01 mol/L) - Konz. Ammoniak-Lösung - Metyhlorange
- Indikator-Puffertablette
- Leitungswasser
Durchführung:
1. Bestimmung der Carbonathärte
In einem 300 mL Erlenmeyerkolben 100 mL zu untersuchende Leitungswasserprobe mit 5 Tropfen Methylorange-Lösung versetzen. Diese Lösung anschließend mit Salzsäure (c = 0,01 mol/L) bis zu einem Farbumschlag von gelb nach orange titrieren.
2.Bestimmung der Gesamthärte
In einem 300 mL Erlenmeyerkolben 100 mL zu untersuchende Leitungswasserprobe mit 2-3 Tropfen Salzsäure (c = 2 mol/L) versetzen. Anschließend die Probe zur Vertreibung des gelösten Kohlenstoffdioxids ca. 1 Minuten sprudelnd kochen.
In der abgekühlten Lösung eine Indikator-Puffertablette lösen und anschließend 10 mL konz. Ammoniak-Lösung hinzufügen. Diese Lösung mit EDTA-Lösung (c = 0,01 mol/L) bis zu einem Farbumschlag von rotorange nach grün titrieren.
Auswertung:
1. Bestimmung der Carbonathärte
Bei der Titration mit Salzsäure werden die Hydrogencarbonat-Ionen, welche für die Carbonathärte verantwortlich sind, neutralisiert.
- +
3(aq) 3 (aq) 2(g) 2
HCO +H O CO +H O
Dabei wird Wasser und Kohlenstoffdioxid gebildet, welches entweicht.
Hydrogencarbonat reagiert in Wasser alkalisch, daher färbt Methylorange die Lösung zunächst gelb und später, sobald der Neutralisationspunkt erreicht ist, orange.
Berechnen lässt sich die Carbonathärte nach folgender Formel:
1 mol H3O+ = 1 mol HCO3- = 0,5 mol Ca2+ = 0,5 mol CaO 1 mmol CaO/L = 5,6 °dH
Somit gilt für eine 100 mL Wasserprobe:
Der Verbrauch von 1 mL HCl (c = 0,01 mol/L) entspricht einem Gehalt von 0,05 mmol CaO/L, was wiederum einer Härte von 0,28°dH entspricht.
Beispiel: 100 mL Marburger Leitungswasser:
Verbrauch: 20,8 mL HCl (c = 0,01 mol/L) = 1,04 mmol CaO/L
= 5,82°dH = Carbonathärte
2.Bestimmung der Gesamthärte:
EDTA (Ethylendiamintetraacetat) ist ein Komplexbildner, der neben den zwei freien Elektronenpaaren der Stickstoffatome auch 4 Carboxylgruppen zur Bindung zur Verfügung stellt. Es ist somit ein 6-zähniger Ligand, welcher sehr stabile Komplexe, so genannte Chelat- oder auch Krebsscherenkomplexe, bildet.
O -
N
O - O
O N
O
O - O -
O
Im Wasser sind Calciumionen oktaedrisch von Wassermolekülen umgeben. Gibt man
EDTA-Lösung zu diesen Ionen, so werden ebenfalls oktaedrisch koordinierte
Komplexe gebildet.
2+ 2- 2- +
2 6 (aq) 2 (aq) (aq) (aq) 2
[Ca(H O) ] +H EDTA [Ca(EDTA)] +2H +6H O
Neben der Bildung des sehr stabilen Chelatkomplexes ist diese Reaktion zusätzlich Entropie getrieben, da aus 2 Molekülen 9 neue Moleküle gebildet werden.
Berechnen lässt sich die Gesamthärte demnach mit folgender Formel:
1 mol EDTA = 1 mol Ca2+ = 1 mol CaO 1 mmol CaO/L = 5,6 °dH
Somit gilt für eine 100 mL Wasserprobe:
Der Verbrauch von 1 mL EDTA-Lösung (c = 0,01 mol/L) entspricht einem Gehalt von 0,1 mmol CaO/L, was wiederum einer Härte von 0,56°dH entspricht.
Beispiel: 100 mL Marburger Leitungswasser:
Verbrauch: 15,3 mL EDTA-Lösung (c = 0,01 mol/L) = 1,53 mmol CaO/L
= 8,87°dH = Gesamthärte C a 2 +
O H 2 O H 2 H 2 O
H 2 O
O H 2
O H 2
N N
C O 2 C O 2 C O 2 C O 2
C a 2 + O
O N
N
O
O O
O
O
O
6 H 2 O
2.3 Wie kommt die „Härte“ ins Wasser?
Versuch 2: Kalkgleichgewicht
Geräte:
- 2 Bechergläser - Demoreagenzglas - Trichter
- Reagenzglas mit durchbohrtem Stopfen - Einleitungsrohr
Chemikalien:
- Trockeneis - Calciumhydroxid
- 30-40°C warmes Wasser - ention. Wasser
Durchführung:
Eine Spaltespitze Calciumhydroxid in ca. 50 mL ention. Wasser lösen und die
Lösung einige Minuten stehen lassen. Anschließend abfiltrieren und die klare Lösung
in ein Becherglas füllen. Das Trockeneis in das Reagenzglas füllen und mit dem durchbohrten Stopfen, in dem das Einleitungsrohr steckt, verschließen. Das Einleitungsrohr nun in die Lösung halten und das Reagenzglas mit Hilfe des 30-40°C warmen Wasserbades erwärmen.
So lange Kohlenstoffdioxid, welches durch Sublimation des Trockeneises gebildet wird, in die Lösung einleiten, bis eine deutliche Trübung eintritt.
Das Demoreagenzglas ca. ¼ hoch mit der getrübten Lösung füllen und erneut Kohlenstoffdioxid einleiten. Der Versuch gilt als beendet, sobald sich die Trübung in dem Demoreagenzglas vollständig aufgelöst hat.
Auswertung:
Kalk, welcher das Calciumsalz der Kohlensäure ist, bildet in wässriger Lösung zunächst folgendes Gleichgewicht:
2 2
3( ) s ( aq ) 3( aq )
Kalk Calciumionen Carbonationen
CaCO Ca CO
Die Carbonationen bilden mit physikalisch gelöstem Kohlenstoffdioxid und Hydrogencarbonat das so genannte Kalkgleichgewicht
2
3 2 2 2 3
CO CO H O HCO
Leitet man in kalkhaltiges Wasser Kohlenstoffdioxid ein, so wird unter Bildung von Hydrogencarbonat die Konzentration der Carbonationen verringert. Das Gleichgewicht wird folglich nach dem Prinzip von Le Chatelier auf die Seite der Hydrogencarbonate verschoben.
2 2 3
CO H O HCO H
Somit kommt es zur Überschreitung des Löslichkeitsproduktes von Calciumcarbonat, welches durch das Ionenprodukt c(Ca 2+ )•c(CO 3 - ) beschrieben wird. Es tritt folglich durch ausfallendes Calciumcarbonat eine Trübung in der Lösung ein.
2
2+ 2- -9
3 3 2
L(CaCO ) = c(Ca ) c(CO ) = 4,7 10 mol L
Durch weitere Zugabe von Kohlenstoffdioxid in die getrübte Lösung kommt es nach folgender Gleichung zur Bildung von Calciumionen
2
3( ) s 2 2( aq ) ( aq ) 2 3( aq )
CaCO H O CO Ca HCO
Das Löslichkeitsprodukt wird schließlich wieder erreicht, so dass der Rückstand wieder vollständig in Lösung geht.
Diesen Vorgang kann man auch häufig in der Natur beobachten.
Beispielsweise bei der Bildung von Tropfsteinen.
Demonstration 2: Bildung von Tropfsteinen
Geräte:
- Trichter
- 2 Bechergläser - saugfähiger Faden - Büroklammern
Chemikalien
- Wasser
- Calciumhydroxid
Durchführung:
Zunächst ist eine gesättigte Calciumhydroxidlösung anzusetzen und anschließend abzufiltrieren. Mit dieser Lösung beide Bechergläser bis zum oberen Rand füllen.
Den Faden zwischen den beiden Bechergläser so spannen, dass er leicht durch hängt. Gegebenenfalls den Faden mit den Büroklammern an den Bechergläsern befestigen.
Diese Apparatur einige Tage stehen lassen und die Bechergläser täglich mit Calciumhydroxidlösung auffüllen.
Beobachtung:
Nach wenigen Tagen wird von dem Faden herab ein Stalaktit abfangen zu wachsen und am Boden wird sich allmählich ein Stalagmit bilden, der dem Stalaktit entgegen wächst.
Abbildung 3: Entstehung von Tropfsteinen
Abbildung 3: Tropfsteinhöhle
Auswertung:
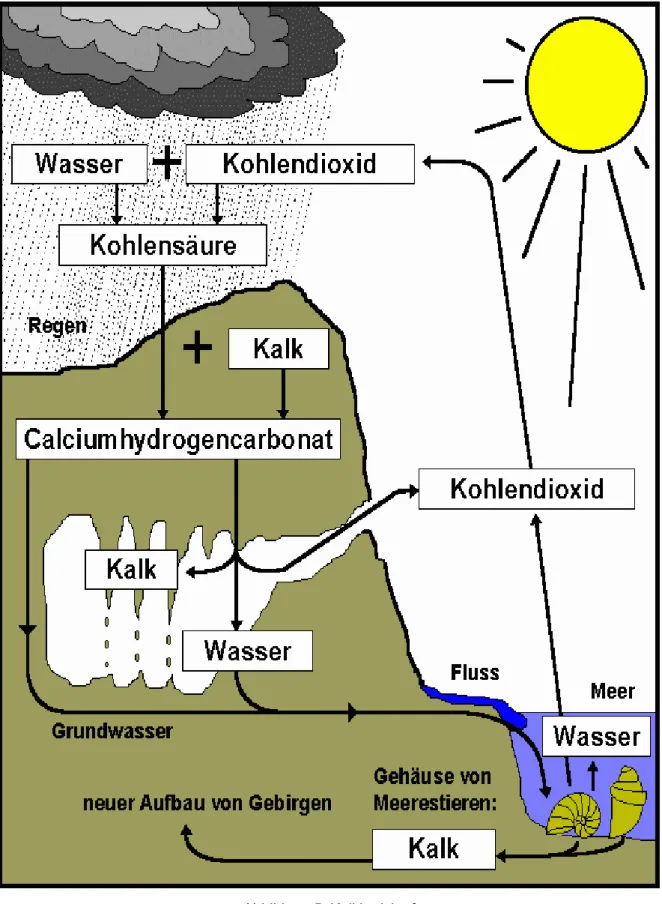
Die Vorgänge in diesem Versuch lassen sich sehr gut anhand des Kalkkreislaufes
erklären
Abbildung 5: Kalkkreislauf
In der Natur wird sich zunächst in der Atmosphäre befindliches Kohlenstoffdioxid im Regenwasser lösen, so dass zu einem geringen Teil Kohlensäure gebildet wird.
" "
CO H O H CO
Der Regen reagiert dadurch leicht sauer.
Diese Kohlensäure löst nun bei Berührung mit kalkhaltigem Gestein den Kalk auf, so dass die Ionen in gelöster Form als Hydrogencarbonate im Wasser vorliegen.
2
3( ) s 2 3( aq ) 2 3
CaCO H CO Ca HCO
Durch den Kohlenstoffdioxidgehalt der Luft ist eine maximale Wasserhärte von 4°dH möglich, somit wird klar, dass das Wasser beim Durchsickern durch den Boden weiteren Kohlenstoffdioxid aufnehmen muss, um Härten von bis zu über 30°dH zu erreichen. Dieses Kohlenstoffdioxid wird dabei von Pflanzen und Mikroorganismen in Bodennähe oder im Boden direkt gebildet.
Tritt das Wasser schließlich wieder an die Oberfläche, B. in Höhlen, so führt zum einen eine Erwärmung des Wassers zur Verdunstung, wodurch wiederum Kalk auskristallisiert.
3 2( ) 2 2 3
( ) aq Erwärmen
Ca HCO H O CO CaCO
Zudem führt eine dünne Flüssigkeitsschicht (wie bei Wassertropfen) oder eine feine Verteilung des Wassers (wie beim Auftreffen von Wassertropfen auf den Fußboden) zu einer verstärkten Abgabe von Kohlenstoffdioxid aus dem Wasser an die Außenluft, wodurch das Kalkgleichgewicht so verschoben wird, dass ebenfalls Calciumcarbonat auskristallisiert.
2
3 2 2 2 3
CO CO H O HCO
Auf diese Art entstehen im Laufe der Jahre Tropfsteinhöhlen, in denen riesige Stalaktiten von den Decken herab wachsen und vom Boden lange Stalagmiten in den Himmel ragen.
Zudem entstehen nach der gleichen Methode tiefe Klüfte in Felswänden,
ausgedehnte Höhlensysteme und weite Karstlandschaften mit dichten Wäldern in
den Tropen und kargen Wiesen in unseren Breiten.
Jedoch nutzen auch Lebewesen diesen Kalkkreislauf zur Bildung von kalkhaltigen Skeletten oder Gehäusen. Somit ist Kalk in seinen verschiedenen Mineralformen genauso oft in Mikro- und Makroorganismen wie in großen Gebirgen zu finden.
Durch Absinken und Ablagerung von kalkhaltigen Skeletten, Muscheln, etc. auf Meeresböden oder Verdunstung von austretenden Quellen kommt es somit ständig zur Neubildung von Kalksedimenten. Diese fallen jedoch wiederum der Verwitterung zum Opfer, so dass ein ewiger Kreislauf bestehen bleibt.
2.4 Vor- und Nachteile von hartem Wasser
Versuch 3: Schaumbildung
Geräte:
Tropfpipette
50 mL Vollpipette
Peleusball
1 mL Messpipette
4x 100 mL Schraubdeckelgläschen
Becherglas
Chemikalien:
Regenwasser
Leitungswasser
ention. Wasser
Mineralwasser
Phenolphthalein
Seifenlösung
Durchführung:
Jeweils 50 mL der unterschiedlichen Wasserproben in jeweils ein Schraubdeckelgläschen füllen und zu jeder Probe 10 Tropfen Phenolphthalein hinzugeben. Ebenfalls in jedes Glas 0,5 mL Seifenlösung geben und die Gläser gut verschließen. Anschließend kräftig schütteln.
Beobachtung:
Während in den Gläschen mit Regenwasser und entionisiertem Wasser ein stabiler Schaum gebildet wird und sich die Lösung rot färbt, fällt in den Gläschen mit Leitungs- und Mineralwasser ein gräulicher Niederschlag aus. Zudem wird kein stabiler Schaum gebildet und auch der Indikator zeigt keine Veränderung an.
Auswertung:
Mineralwasser und Leitungswasser enthalten Calciumionen. Diese reagieren mit Seifenlösung zu Kalkseife. Bei Seifen handelt es sich um die Salze von Fettsäuren.
Gibt man Seifenlösung zu kalkhaltigem Wasser, so lagern sich zwei Fettsäurereste um ein Calciumion an und bilden wasserunlösliche Kalkseife, wobei Natriumionen an das Wasser abgegeben werden.
C O
O n CH 3
2Na + + 2
+
C 18-20
Ca 2+ C
O
O CH 3
2
Ca 2+
n
Kalkseife
+ 2Na + (aq)
(aq)
Seifenlösung
(aq)
(s)