Hinweis
Bei dieser Datei handelt es sich um ein Protokoll, das einen Vortrag im Rahmen des Chemielehramtsstudiums an der Uni Marburg referiert. Zur besseren
Durchsuchbarkeit wurde zudem eine Texterkennung durchgeführt und hinter das eingescannte Bild gelegt, so dass Copy & Paste möglich ist – aber Vorsicht, die Texterkennung wurde nicht korrigiert und ist gerade bei schlecht leserlichen Dateien mit Fehlern behaftet.
Alle mehr als 700 Protokolle (Anfang 2007) können auf der Seite
http://www.chids.de/veranstaltungen/uebungen_experimentalvortrag.html eingesehen und heruntergeladen werden.
Zudem stehen auf der Seite www.chids.de weitere Versuche, Lernzirkel und Staatsexamensarbeiten bereit.
Dr. Ph. Reiß, im Juli 2007
Experimentalvortrag ws
1995/96Wi/ch und Wi/chprodukle
Andreas Wagner Bergstraße 12
35091 Cölbe
INHALTSVERZEICHNIS
I) DEFINITION 1
11) ALLGEMEINES , 1
1) Milchleistung 1
2) Milch als Lebensmittel 2
3) Zusammensetzung von Milch verschiedener Tierarten 2
4) Zusammensetzung von Kuhmilch 3
5) Disperse Zustandsformder Milchbestandteile 3
6) Farbe der Milch 4
III) INHALTSSTOFFE DER MILCH 4
1) Milchfett 4
a)Allgemeines , '" 4
b) Fettsäurender Milch 5
c)BesonderheitendesMilchfettes 6
d) Aufrahmen derMilch 8
e) Homogenisierung 10
2) Milchproteine 10
a) Allgemeines 10
b) Casein 11
c)Molkenprotein 16
3) Milchzucker (Lactose) 17
4) Mineralstoffe der Milch 20
5) Vitamine der Milch 21
6) Enzyme der Milch 23
IV) JOGHURT 26
V) DURCHGEFÜHRTE VERSUCHE. 31
VI) LITERATURVERZEICHNIS 32
I)DEFINITION
Milch ist die aus Milchdrüsen weiblicher Säugetiere während der Lactation abgesonderte weiße, un- durchsichtige Flüssigkeit. Als Lactationsperiode bezeichnet man in diesem Zusammenhang die Zeit von der Geburt bis zu dem Zeitpunkt, an dem der Milchfluß erliegt (bei der Kuh ca. 6 Wochen vor dem nächsten Abkalben;Lactationszeit insgesamt etwa 300 Tage).
11) ALLGEMEINES
t)MILCHLEISTUNG
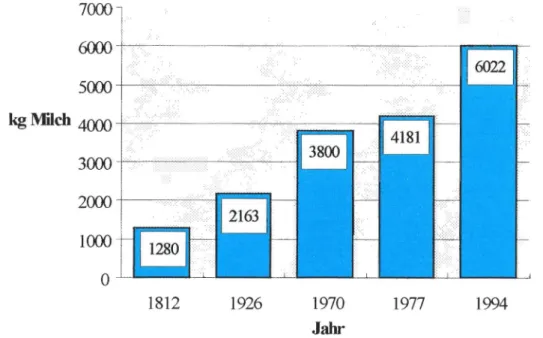
Zum Aufwachsen benötigt ein Kalb etwa 1000 I Milch und diese Milchmenge hat die Natur bei jeder Mutterkuh vorgesehen.Durch gezielte Züchtung ist die Milchleistung einer Kuh in den letzten Jahren erheblich gestiegen. Dabei ist sie rassenspezifisch und kann bei einigen Kühen (vornehmlich der schwarzbunten Rasse) durchaus die 12000 kg/Jahr übersteigen.
7roJ
6000-tT---"---,'-~---,,'-~~--Ti"""'=~
5000+-++-~.._,'=---++-++-,---~~,':-Jr"'--~
kgMilch 4roJ+----F2~-~+--s~;;;;;;;;;;.,--tr::ll_1K~~~~:~~il socof7.'"--'---cc=-:-~I~-Jt
2000
+-~~IE'-~~ri lS4 ~t~~4~~~ · 1~~r~~
1000
o
lJt~L~~~~U~~~~L1812 1926 1970
Jahr
1977 1994
Abb. 1 Milchleistung pro Kuh in Kilogramm
2) MILCH ALS LEBENSMITTEL
Milch ist ein bedeutendes Lebensmittel. Sie ist die einzige Nahrung junger Säugetiere in der ersten Zeit ihres Lebens und in ihrer biologischer Zusammensetzung optimal für die Ernährung und Be- dürfnisse ei-nes jungen Lebewesens zugeschnitten. Sie enthält alle notwendigen Nähr- und Mineral- stoffe in nahezu idealer Kombination. Außerdem schützen Abwehrstoffe das junge Säugetier vor Infektionen.
Lebensmittelrechtlich wird in der Bundesrepublik unter Milch ausschließlich Kuhmilch verstanden, während Ziegen- oder Schafinilch stets als solche eindeutig zu kennzeichnen ist. Aus diesem Grunde ist auch nachfolgend - wenn nicht ausdrücklich anders vermerkt - immer Kuhmilch gemeint. Typische Verbraucher von Büffelmilch sind Ägypten, China, Indien, Pakistan, Ostasien, von Schafmilch Tür- kei, Frankreich, Italien sowie Iran und von Ziegenmilch Indien, Pakistan, Griechenland und Frank- reich.
3) ZUSAMMENSETZUNG VON MILCH VERSCffiEDENER TIERARTEN
Die Zusammensetzung von Milch verschiedener Tierarten in % ist in nachstehender Tabelle aufge- fuhrt. Man erkennt, daß die Zusammensetzung unterschiedlich und den natürlichen Lebensbedingun- gen angepaßt ist. Tiere kalter Klimazonen besitzen Milch mit einem hohem Fettgehalt, da dieser ver- bunden ist mit einem hohen Energieinhalt, der dem Nachwuchs größtmögliche Überlebenschance bietet. Dies ist zum Beispiel beim Rentier der Fall. Eiweiß ist wichtig für schnelles Wachstum. Aus diesem Grunde besitzen Hunde, aber auch Kleinsäuger wie Mäuse eine sehr eiweißreiche Milch. Vorteil von dieser ist, daß die Jungtiere das ihnen zur Verfugung gestellte Eiweiß in körpereigenes Eiweiß umwandeln und so sehr schnell ihr Geburtsgewicht verdoppeln können. Zu erkennen ist auch, daß die Zusammensetzung von Kuhmilch der der Frauenmilch am ähnlichsten ist, weshalb sie auch am ehesten zur Säuglingsernährung geeignet ist.
davon:
BütTelmilch.~,..>
Kuhmilch<c "
Frauenmilch
67,3 81,7 82,1 87,3 88,0
32,7 18,3 17,9 12,7 12,0
Fett 18,1 6,3 8,0 3,7 3,3
Eiweiß Zucker
10,5 1,5
6,2 4,9
4,5 4,5
3,6 4,7
1,8 6,5
4) ZUSAMMENSETZUNG VON KUHMILCH
Im Folgenden soll die Zusammensetzung von Kuhmilch als bedeutendste Milch ein wenig näher be- trachtet werden. Sie schwankt bedingt durch Rasse, Alter, Gesundheitszustand, Lactationsstadium, Pflege und Beanspruchung der Tiere,Futter sowie Melkeinflüsse.
Milch
1
Wasser 87...88%
1
Trockenmasse 12... 13%
1
~
Milchzucker 4,6 ...4,70/0
l
Casein 2,8 ...3,20/0
Fett
3,0...5,6%
l
Molkenproteine 0,5 ...0,6%
fettfreie Trockemnasse 8...9%
1
Salze, Enzyme, Vitamine 0,7,..0,8%
Abb.2 Zusammensetzung von Kuhmilch
5)DISPERSE ZUSTANDSFORM DER MILCHBESTANDTEILE
Die Bestandteile der Milch liegen aufgrund unterschiedlicher Größe in unterschiedlichen Zustands- formen vor.
Echte Lösung: Salze und Lactose « 1 nm) Kolloidale Phase: Eiweiß (1...500 nm)
Emulgierter Zustand: Fett (» >500 nm)
Fazit: Milch ist ein polydisperses Gemisch aus Trockenmassebestandteilen und Wasser. Das Fett liegt emulgiert, die Proteine kolloidal in der wäßrigen Lösung der übrigen Milchbestand- teile vor.
6) FARBE DER MILCH
Die Farbe der Milch ist weiß bis gelblich-weiß. Die weiße Farbe kommt durch Lichtstreuung und -absorption an Fetttröpchen und Proteinmicellen zustande (auch Magermilch ist weiß). Die gelblich- grüne stammt vom ß-Carotin der Fettphase (vor allem im Sommer während der Weidefutterung) und vom Riboflavin [= Lactoflavin (lat.:Gelbstoffin Milch) = Vitamin B2].
III) INHALTSSTOFFE DER MILCH
Im folgenden sollen die wichtigsten Milchinhaltsstoffe ein wenig näher betrachtet werden. Aufgrund der zur Verfugung stehenden Zeit ist es jedoch nicht möglich, alle ausfuhriich zu besprechen und mit Experimenten zu untermauern
1) MILCHFETT a) Allgemeines
Milchfett hat mit mehr als 200 verschiedenen Fettsäuren die mannigfaltigste Zusammensetzung aller natürlichen Fette und auch die beste Verdaulichkeit. Jedoch nur 14 kommen als Hauptfettsäuren mit einem Anteil von über 1% vor, der Rest als Minorfettsäuren.
Milchfett
J
Reines Fett
99,2%(Triglyceride)
1
Fettbegleitstoffe 0,8%
1
Phospholipide
1
Lecithin Kephalin
r
Sterine
1
Cholesterol Lanosterin
Fettlösliche
r
Vitamine
1
Vitamin A Vitamin 0 Vitamin E
1
Kohlenwasserstoff
1
Squalen
Abb.3 ZusammensetzungdesMilchfett es
b) Fettsäuren derMilch
Nachfolgend sind die 14 Hauptfettsäuren des Milchfettes aufgefuhrt. Auffallend ist der hohe Gehalt an den niedermolekularen Fettsäuren Buttersäure(C4 ) , Capronsäure (C6 ) , Caprylsäure (Cs) und Ca- prinsäure (CIO), die relativ häufig in der Milch zu finden sind. Sie haben einen unangenehmen, schweißigen und ranzigen Geruch und Geschmack, der schon in geringsten Spuren wahrnehmbarist. Kommen diese Fettsäuren frei im Milchfett vor,dann verursachen sie die Fehler"alt" und ,,ranzig".
wissenseh. Name Trivialname Summenformel % in Gesamtfett
Butansäure- Buttersäure- C3H7COOH 2,5" .5%
n-Hexan- Capron- CSHl1COOH 2,5".3, 5%
n-Octan- Capryl- C7H1SCOOH 1...3%
n-Decan- Caprin- C9H19COOH 1,6...3,6%
n-Dodecan- Laurin- Cl1H23COOH 2,3...7%
n-Tetradecan- Myristin- C13H27COOH 5...30%
n-Hexadecan- Palmitin- C1sH31COOH 13...52%
n-Octadecan- Stearin- C17H3SCOOH 2... 15%
n-Eicosan- Arachin- CI9H39COOH 0,4...1,2%
9-Tetradecen- Myristolein- C13H2SCOOH 0,9".1,6%
9-Hexadecen- Palmitolein- C1SH29COOH 2,8...4%
9-0ctadecen- ÖI- C17H33COOH 25...45%
9,12-0ctadecadien- Linol- C17H31COOH 2...6%
Tab.] Die 1-1Hauptfettsäurendes Milchfettes
Versuch 1) Direktfärbung von Milchfett mit Sudan III
Andieser Stelle sei darauf hingewiesen, sich über Gefahren und Sicherheitsvorschriften aller verwen- deten Chemikalien der folgenden Versuche zu informieren!!!
Materialien: Demonstrationsreagenzglas Chemikalien: Sudan-IH Milch
Durchfuhrung:
In 5 ml Milch gibt man eine Spatelspitze Sudan-Ill-Pulver und schüttelt kräftig. Ein kleiner Teil des Farbstoffs löst sich in den Fetttröpfchen der Milch und färbtdiese rosarot. Eine Blindprobe mit Was- ser verläuft negativ.
Erklärung:
Bei dem Farbstoff Sudan-Ill (Ceresinrot) handelt es sich um einen Azofarbstoff, der wasserunlöslich, aber sehr gut löslich in Fetten, Ölen und Harzen ist.
HO
< >-N~N-o-N=N
Sudan III= Ceresinrot
c) BesonderheitendesMilchfettes
Eine interessante Frage ist, warum sich das Fett nicht wie sonst üblich auf der wäßrigen Phase, son- dern gleichmäßig in ihr verteilt befindet?
Fett kommt in Form kleiner Fettkügelchen mit Durchmessern von 0,1-10 my vor. Die größte Häufig- keit liegt bei 3-6 my (3000-6000 nm).Die Anzahl der Fettkügelchen beträgt 1,5 - 3 Milliarden je ml.
Wegen der großen Anzahl kommt es zwischen den Fettkügelchen zu Zusammenstößen, und sie müßten sich infolge ihres hydrophoben Verhaltens zu größeren sichtbaren Tröpfchen vereinigen.Das ist jedoch nicht der Fall. Um diese Tatsache zu verstehen, muß man den Aufbau der Fettkügelchen in der Milch einmal genauer betrachten.
Man erkennt von innen nach außen betrachtet den flüssigen Fettkern im Zentrum des Fettkügelchens, der umgeben ist von einer kristallisierten Triglyceridschicht. Weiter nach außen befindet sich eine Schicht aus Phosphatiden (Lecithinmolekülen), anschließend eine aus Hüllenproteinen. Dort eingela- gert sind Kupfer- und Eisenionen, die Membranlipase und Enzyme in Form von Mikrosomen. Nach außen hin wird das Fettkügelchen von einer Hülle aus Hydratwasser abgeschlossen.
---
..
... --"'"..
6e"Z"f....
1) flüssiger Fettkem -F
2) kristallisierte Triglyceridschicht 3) Lipoidschicht (Lecithin) o-F
4) Fettkügelchenhüllenproteine 0 - -
5) Hydratwasser 6) Membranlipase 0
Lecithin (chematisch) lipophiler- hydrophiler Teil
~
Lecithin
Abb 4Aufbau der Fettkügelchen
Die Verteilung der Fettkügelchen im Wasser wird durch die Phosphatidhülle (Lecithin) ermöglicht, welches einen hydrophilen und einen hydrophoben Molekülrest besitzt. Dadurch ist sie ein guter Emulgator. Mit dem hydrophoben Molekülteil ragt das Lecithinmolekül in das Fett, mit dem hydro- philen in die wäßrige Phase. Die Schutzhülle verhindert das Zusammenfließen des Fettes und schützt es vor Oxidation und Spaltung.
CI7H~~-CO-O-CH.,.).) I -
CI-H~l-CO-O-CH 0
) .) I 11 +
H2 C - O -
1-0-CH
2-CH2-N (CH3h0-
Fazit: Milch ist eine beständige Emulsion
Versuch 2) Demonstration von "Fett-in-Wasser-Emulsion"
Materialien: Mikroprojektor Objektträger Deckgläser Pipette
Chemikalien: Rohmilch
Durchfuhrung: 1 Volumenteil Milch wird mit 8 Volumenteilen Wasser gemischt und etwas davon auf einen Objektträger gegeben. Anschließend projeziert man das Bild auf die Wand. Man erkennt ver- schieden große Fettröpchen (bei Verwendung von H-Milch sind diese aufgrund der Homogenisie- rung zu klein und nicht deutlich zu erkennen), die in der Milch gleichmäßig verteilt sind.
d) Aufrahmen der Milch
Rohmilch bildet schon beim Stehen nach 30-60 min eine sichtbare Rahmschicht (an dieser Stelle kann man ein Reagenzglas mit aufgerahmter Milch zeigen). Ursache dafur ist der Dichteunterschied zwi- schen den Fettkügelchen und der Milchflüssigkeit. Beim Aufrahmen ändert sich das Verteilungs- gleichgewicht der Fettkügelchen, eine Zerstörung der Emulsion tritt nicht ein, daß heißt, durch schütteln kann der alte Zustand wieder erreicht werden.
Die Aufrahmungsgeschwindigkeit folgt mit einigen Einschränkungen der Gleichung nach Stokes:
2 2
(d, -d
2 )V=-xr
Xxg
9 1]
Abb5Gleichung nach Stokes
Dabei bedeuten: V= Aufsteiggeschwindigkeit (cm S·I )
r= Radius der Fettkügelchen (cm)
d, = Dichte des Dispersionsmittel (1,034 g cm" ) d2= Dichte des Kügelchens (0,931 g cm")
11 =Viskosität der Milch (cm' gs' )
g =Erdbeschleunigung (981 cmS·2)
Aus obiger Gleichung sind die Einflußfaktoren der Aufrahmung zu erkennen:
• Ursache der Aufrahmung ist der Dichteunterschied
• Eine hohe Viskosität behindert das Aufrahmen
• Die großen Fettkügelchen steigen schneller nach oben als die kleineren, da das Quadrat der Kugelradien in die Gleichung eingeht
Aus dem bisher Gesagten müßte sich ergeben, daß ein normales Fettkügelchen Stunden bräuchte, um 1 cm aufzusteigen. Die Aufrahmung erfolgt jedoch viel schneller. Um das zu verstehen, muß man den Aufrahmvorgang etwas näher betrachten.
Die schnelle Aufrahmung ist auf eine Traubenbildung zurückzufuhren, bei der die großen Fetttröpf- chen aufgrund der oben genannten Faktoren schneller emporsteigen als die kleinen, diese dabei ein- holen und sich mit ihnen zu größeren Einheiten verbinden.Bei diesem Vorgang haften die Tröpfchen mit Hilfe der Fettkügelchenhüllenproteinen aneinander.
a) vor b) während c) nach dem Aufrahmen
Abb 6,.jufrahmvorgang von Rohmilch
e) Homogenisierung
Durch Homogenisierung wird die Aufrahmgeschwindigkeit bedeutend verlangsamt. Die auf 60°C vorgewährmte Milch wird mit ca. 100 atm (bar) durch feine Düsen gepumpt, wobei der Fettkügel- chendurchmesser von 4 auf 1 my reduziert wird.Dadurch wird die Oberfläche etwa vertausendfacht.
Als Folge daraus ergibt sich geringeres Aufrahmen, leichtere Verdaulichkeit sowie erhöhte Weißkraft durch verstärkte Lichtreflexion infolge der Oberflächenvergrößerung. Durchgefuhrt wird diese Art der Milchbehandlung bei Trinkmilch, Kondensmilch, Sahne und Käsereimilch, also bei den Produk- ten, bei denen sich ein Aufrahmen besonders nachteilig auswirkt. Ein Nachteil der Homogenisierung ist das (teilweise) Zerstören der Membranschicht der Fettkügelchen und die damit verbundene Freile- gung von Fett.
2) MILCHPROTEINE
a) Allgemeines
In der Milch wurden mehrere 100 verschiedene Proteinarten nachgewiesen. Sie werden in die histo- risch entstandene (1872) und aus praktischen Gründen beibehaltene Einteilung in Casein (Käsestoff) und Molkenproteine eingeordnet, obwohl bekannt ist, daß es sich um keine einheitlichen Verbindun- gen handelt.
Milchproteine 100%
Casein
1
78-85%
Hauptfraktionen:
u- Casein 35-45% (199 AS)
ß-
Casein 25-35% (209 AS)x-
Casein 8-15% (169 AS) y- Casein 3- 7%.Ihh 7Milchproteine
Molkenproteine
1
15-22%
u- Lactalbumin 2-5%
ß-
Lactglobulin 7-12%Membraneiweiß 40/0 Immunglobuline 3%
Die Proteine der Milch sind kolloidal gelöst, daß heißt, endständige Carboxyl- bzw. Aminogruppen sorgen durch Dissoziation bzw.Protonenaufuahme für elektrische Aufladung an der Proteinoberflä- ehe. Infolgedessen lagert sich Wasser an die geladenen Gruppen an und bildet so eine Hydrathülle. Stoßen zwei solcher Teilchen zusammen, verhindert die Hydrathülle das Verbinden zu einem größe- ren Teilchen und damit das Ausflocken der Proteine.
fhO
fhO
fhO H H
o
1/
-Nlh+ H-O/ HOOC- -COO· H fhN-
·OOC- -NHz
H3+N- 1 -COOH
+ /H
-NHJ 0:-
·OOC- -COOH H -NHz
2
fhO
HzO
1) Proteinteilchen mit endständigen Gruppen 2) innere Hydrathül1e 3) äußere Hydrathülle
3 HzO
Abb8Proteinteilchen mit Hydrathü//e
b) Casein
Nachfolgend werden zwei Wege aufgezeigt, mit denen das Casein ausgefällt und von den übrigen Milcheiweißen abgetrennt werden kann.
1) Caseinfällung mit Hilfe von Säure 2) Caseinfällung mit Hilfe des Labenzyms
Versuch Ja) Säurekoagulation von Casein
Materialien: Zentrifuge
Zentrifugengläser Becherglas (250 ml) Meßpipette ( 10 ml) Glasstab
Chemikalien: Rohmilch (ISO mi) konz.Essigsäure (10 mi)
Durchfuhrung:
Die konzentrierte Essigsäure wird in die Milch eingerührt. Sofort ist ein weißer flockiger Nieder- schlag von Casein zu erkennen, der abzentrifugiert werden kann. Der Überstand - die Molke - ist gelbgrün gefärbt. Weniger aufwendig, aber etwas langwieriger ist das Abfiltrieren des Caseins.
- - - --=----
---~~~~~~~~~~~~~~---
- - ----="'--_-::::_-- - - - - - - - - ----=---==-'
~O
--- ...
J''' -NH ,
"HOOC- 3
, -coorr,
I HzN- \
I -NH
'·ooC- 2 \
I '
I,H3'N- -COOH: ges hwächte
\, HOOC- -NH],-/ Hy athülle
"·OOC- -COOH"
'... -NH., "
..._--.;-'
~O
~O
~O
~O
,,----....
'" NH _...
,',...HOOC-=-_c300·
I I-bN- '
I - \
I·ooc- -NH2L\ _ _- I I
'HI 3'N-
\ HOOC-, ,
',-ooc- -coo,:-"
" -NH., ,
- c:':»>:
pH>IP(isoelektrischer Punkt) (-) >(+)
pH=IP (+)=(-) Abb 9 Säurekoagulation von Casein
pH-Wert-Erniedrigung bis zum isoelektrischen Punkt (4,6)
• Proteine werden elektrisch neutral
• Hydrathülle wird geschwächt
---> Proteine lagern sich zusammen und flocken aus
Erklärung:
Die Größe der Oberflächenladung ist pl-I-Wert abhängig. Eine Zu- oder Abnahme der Wasserstoffio- nenkonzentration, d.h. die Erniedrigung des pH-Wertes, stört das Gleichgewicht. Dabei gehen La- dungen verloren und die Hydrathülle wird geschwächt. Dieser Vorgang vollzieht sich so lange, bis die Zahl der negativen und positiven Ladungen ausgeglichen ist. Der pH-Wert, bei dem dieser Zu- stand vorliegt, ist der isoelektrische Punkt des Proteins. An diesem Punkt ist die Hydrathülle am schwächsten, die Proteine lagern sich aneinander und flocken aus.
Als Caseinfraktion bezeichnet man den bei pH 4,6 ausfällbaren Anteil der Proteine. Casein ist im Gegensatz zu den meisten anderen Proteinen bis 150°C hitzebeständig, da die Aminosäuren Cystin
Versuch 3b) XantllOprotein - Reaktion au(Casein
Materialien: Demonstrationsreagenzglas Reagenzglasklammer Bunsenbrenner
Chemikalien: Casein aus Versuch 3a NaOH (c= 2 mol/l) HN03 (konz.)
Durchfuhrung:
Etwas des Caseins, welches in NaOH aufgelöst wird (auch Rohmilch kann direkt verwendet wer- den), wird mit wenig konzentrierter Salpetersäure versetzt.Bereits in der Kälte fallt das Eiweiß blaß- gelb, in der Hitze wird es wesentlich intensiver. Der Nachweis funktioniert nur bei Vorhandensein von den aromatischen Aminosäuren Phenylalanin, Tyrosin und Tryptophan durch Nitrierung des Benzolringes (Nitrobenzole sind gelb gefärbt). Da diese drei Aminosäuren jedoch in nahezu jedem Eiweiß vorkommen, verläuft der Nachweis fast immer positiv. Auch die Gelbfärbung der Haut bei Kontakt mit Salpetersäure beruht auf dieser Reaktion.
1)Bildung des Elektrophils durch Eigenprotonierung:
2) Elektrophile Substitution (am Beispiel Phenylalanin)
~ ;g- ~N
..--....N02+ + ~\
0
CH2-CH-COOH :;;;;..:==~. - - - (~) CH2-CH-COOHH ~TU_ H ....-. I
1 ...1.2 NH2
-
ebenso:
OHyCHr-rH-COOH NH2
02
Tyrosin Tryptophan
Aufbau des Caseins
Bevor auf die zweite Möglichkeit der Caseinfällung eingegangen werden kann, muß etwas Grundsätzliches zum Wesen des Caseins gesagt werden.
• Alpha-Kasein
• Beta-Kasein
Abb 10Caseinmicelle
Casein ist kein chemisches Individuum, sondern besteht aus CaseinmicelIen, die sich aus Caseinsub- micellen aufbauen. Diese SubmicelIen bestehen aus Caseinkomplexen der ungefähren Zusammenset- zung U9ß4Y1X3,500 dieser SubmicelIen bilden eine Caseinmicelle (15*1012in 1 ml). Die Bindung der Caseinkomplexe untereinander erfolgt über Calciumphosphat-Brücken an den Aminosäuren Serin, deren Reste phosphoryliert sind. In Gegenwart von Calciumionen sind u- und ß-Caseine unlöslich, x-Casein dagegen löslich.Zu der Micellenbildung, die dann ja kolloidal gelöst in Milch vorkommen (und nicht ausfallen), kommt es, da sich vornehmlich das x-Casein an den Außenstellen der Casein- micellen befindet. Die hydrophilen Enden der x-Caseine (rot) bewirken so eine Art Emulgatorfunk- tion.
Abb 11 Verbrückungvon PeptidkettendurchCalciumionen
Versucll4) Calciumabllängige Caseinfällung mit Lab
(NlL)2C204 (c=2 rnol/l) CaCh - Lsg.
Chemikalien: RohrniIch Labtablette Demonstrationsreagenzgläser
regelbares Wasserbad Thermometer
Materialien:
Meßpipette (IOml) Durchfuhrung:
Die zweite Möglichkeit der Caseinfällungist die enzymatische mit Lab. Dazu löst man 0,5 g Labfer- ment (erhältlich in Apotheken oder Molkereien) in 20 mldestilliertem Wasser. Nun befullt man ein Demonstrationsreagenzglas (a) mit 20 mlfrischer Milch und 10mlLablösung, ein zweites (b) mit 20 ml Milch, 10 ml Lablösung und 2 ml Ammoniumoxalatlösung. Seide Reagenzgläser werden gut durchgernischt und in ein 60°C warmes Wasserbad gestellt. Nach kurzer Zeit ist die Milch im Rea- genzglas a geronnen, die des Reagenzglases b jedoch nicht. Zu diesem gibt man etwas Calciumchlo- ridlösung, durch die auch die Milch in b gerinnt.
a) Gerinnung der Milch durch Lab:
1 105 106 169
Pyg Phe - Met.. Val x-Casein
1 105
Pyg...Phe + Paracasein-l +
106 169
Met......Val Glycopeptid
b) bei (NH4h(C204)-Zugabe:
Ca2+ + (NH4h(C204) ~ CaC204.J, + 2NHt (keine Proteinfällung)
Erklärung:
Das Labenzym Rennin (Chymosin), das aus der Schleimhaut des Labmagens säugender Kälber ge- wonnen wird (neuerdings wird ein bakterielles Enzym in Holland produziert, indem das Gen des Kal- bes in Escherichia co li verpflanzt wird) Der Milch zugesetzt, spaltet es selektiv die Peptidbindung des x-Caseins an der Stelle Phe105 - Met106 , und zerstört es und somit auch die Schutzwirkung vor Ausflockung. Es entsteht ein lösliches Glycopeptid (64AS; in Abb 10 rot) und ein unlösliches, als Paracasein (105AS; in Abb 10 weiß) bezeichnetes Bruchstück. Dieses verbindet sich über Calcium- brücken mit dem a- und ß-Casein zu einem Gel, fallt zusammen mit ihnen aus und legt die Milch dick. Dieses ist der grundlegende Prozeß der Labkäserei, die von großem wirtschaftlichen Interesse ist. Wird, wie im Versuch, das Calcium durch Oxalat gefallt, kommt es nicht zur Proteingerinnung.
c) Molkenprotein
Neben dem Casein befindet sich im Milcheiweiß das hitzekoagulierbare Molkeneiweiß (Lactalbumin und Lactglobulin).Hitzekoalgulierbar deshalb, da ein höherer Anteil an schwefelhaltigen Aminosäu- ren Cystein und Cystin vorhanden ist. Bei Denatuierung durch Erhitzen tritt eine Disulfidbrücken- spaltung ein. Dabei wird Dimethylsulfid gebildet, welches für den Kochgeschmack von UHT -Milch verantwortlich ist. Das Molkeeiweiß ist deshalb nicht durch Säure ausfällbar, da es eine sehr fest gebundene Hydrathülle besitzt. Außer durch Kochen (Denaturierung) ist es durch Aussalzen zu er- halten. Beim Aussalzen dissoziiert das im Überschuß zugegebene Ammoniumsulfat in wäßriger Lö- sung in Ammonium- und Sulfat-Ionen. Diese Ionen entziehen den Molkenproteinen aufgrund ihrer größeren Ladungsdichte die Hydrathülle, sodaß sie ausflocken.
Versuch 5) Biuret-Reaktion aufMolkenproteine
Materialien: Demonstrationsreagenzgläser Pipette
Chemikalien: Molke aus Versuch 3a NaOH (c= 2 mol/l) CUS04 - Lsg. Durchfuhrung:
Man gibt etwas von der Molke in ein Reagenzglas und versetzt sie mit der halben Menge Natron- lauge. Anschließend schüttelt man und gibt wenige Tropfen der stark verdünnten (1 %ig !) Kupfer- sulfatIösung hinzu. Eine Violettfärbung zeigt Protein an. Zum Vergleich ist eine Blindprobe mit de- stilliertem Wasser durchzufuhren.
O H R 2-
R ~-t/ 0
I I I 11
----C-NIG GIN- C - - - -
I -', r:
H " t
\ ;2+- Cu
,4 lt, H
.
,," '\ I
----C-NIGelN- C - ---
11 I I I
o C--C R
/ I 11
R H O
Protein - Kupfer - Komplex Erklärung:
Beim Nachweis bilden die Kupfer-Ionen mit den Eiweißen in alkalischer Lösung violett gefärbte Protein - Kupfer-Komplexverbindungen. Bei der Blindprobe ist kein Komplexbildner vorhanden und
3)MILCHZUCKER (LACTOSE)
Lactose ist das charakteristische Kohlenhydrat der Milch und kommt in Mengen von 4 - 6% in der u- und ß-Form (Ll,55%) vor. Die Einzelbestandteile des.Disaccharides.Dcfilucose und D-Galacto- se treten nur in Spuren auf Zwischen der Galactose und der Glucose besteht eine 1-4-Verkettung, und zwar eine ß-galactosidische (a-Galactosidase fuhrt nicht zur Spaltung).
D-Galactose D-Glucose
Lactose =4-0-(ß-D-Galactopyranosy1)-D-glucopyranose
Lactose besitzt nur etwa 30% der Süßkraft der Saccharose (Wert auf 100% festgelegt) und wird durch Eindampfen der enteiweißten Molke gewonnen.
120 r~'-~~····~~=~~=~~·-~======":':=~
Süßkraft in %
100
80 ·
60 +----1'>" . ""F~"--"';';" ;'~ 'I---k~::':~:"---J
40
20
o.J....:.;:...:.JIo.ioi_'"'--'--L...=~il;:;.;L.--'-~!ii.ooIIli~
Fructose Saccharose Glucose Galactose Lactose Abb12Süßkraft von Lactose
Versuch 6) Fell/ing - Reaktion au(Milchzucker
Materialien: Demonstrationsreagenzglas Reagenzglasklammer Bunsenbrenner
Meßpipetten versch. Größe
Chemikalien: Molke (enteiweißt) Fehling I/lI NaOH (konz.)
Durchfuhrung:
Man versetzt 5mlder enteiweißten Molke (zum enteiweißen salzt man die Molke aus,indem man sie mit gesättigter Ammoniumsulfat-Lösung kocht. Dabei entzieht das Salz dem Eiweiß das Hydratwas- ser.Albumin und Globulin flocken aus und werden abfiltriert.) mit etwas konz. Natronlauge (Lösung muß alkalisch sein!) und anschließend mit 3 ml frisch bereiteter Fehling-Lösung. Fehling I ist eine Lösung von I,73g kristaIIisiertem Kupfersulfat in 25 ml Wasser, Fehling II eine Lösung von 8,5g Natrium-Kalium-Tartrat und 2,5g NaOH in 25 rnl Wasser. Einzeln aufbewahrt sind die Lösungen stabil und deshalb erst kurz vor Gebrauch zu gleichen Teilen miteinander zu mischen. Anschließend wird vorsichtig erwärmt. Dabei fälltder charakteristische ziegelrote Cu20-Niederschlag aus, der re- duzierende Zucker anzeigt.
Erklärung:
Lactose enthält eine Aldehydgruppe und wirkt deshalb reduzierend. Sie reduziert Fehlingsche Lö- sung zu rotem Kupfer (I)-oxid nicht stöchiometrischer Zusammensetzung und wird dabei zur Lacto- bionsäure oxidiert.
OH
~r----OH ~r----OH
Ringform
..
---~OHC_H\\o
OH
offenkettige Form (ca. 2%)
Reduktion: 2CuZT + 2e" + 20H- -+ [CuzO]-!.. (rotbraun) + HzO
Oxidation:
HC-CH
11 11 qO
HO-CH2-C C-C
\ / 'H
o
Lactobionsäure Eigenschaften
Bei der Herstellung zahlreicher Molkereierzeugnisse ist die Lactose wichtigstes Nährsubstrat fur Mikroorganismen, wobei die Milchsäuregärung die größte Rolle spielt (Sauermilchprodukte s. spä- ter). Von untergeordneter Funktion sind die alkoholische Gärung (Kefir), die Propionsäuregärung (Käse) oder die unerwünschte Buttersäuregärung (Käse) und die Essigsäuregärung (Sauermilch- quark). Da Lactose durch Microorganismen nicht direkt vergoren werden kann, ist eine vorherige enzymatische Spaltung (Lactase) erforderlich. Neugeborene besitzen dieses Enzym, viele Erwach- sene nicht mehr (Lactoseunverträglichkeit; 3% der Mitteleuropäer, 97% der Thais).
Lactose ist auch an vielen unerwünschten sensorischen Veränderungen (Bräunung, Geruch, Ge- schmack) von hocherhitzten Milchprodukten (H-Milch, Kondensmilch, Milchpulver) beteiligt. Neben Karamelisierung (intramolekulare Wasserabspaltung) treten Maillard-Reaktionen auf (Reaktionen zwischen Lactose und Aminosäuren).
H ~O 'C~
H-C-OIH]I
r1HOl- t-
H )'-..Lill-~oHI
~c-illHl
CHI 20H
Glucose
Abb /3KaramelisierungderLactose
5 Hydroxymethylfurfural
4) MINERALSTOFFE DER MILCH
Der Mineralstoffgehalt der Milch liegt bei etwa 0,7%.Auf Experimente zum Nachweis der Mineral- stoffe wird im Rahmen dieses Vortrages verzichtet, alle Salze sind jedoch einfach mit den herkömm- lichen Nachweisverfahren nachzuweisen. Die Mineralstoffe fungieren als Puffer und Stabilisator auf den kolloidalen Zustand der Milchproteine.
Bestandteil Gehalt in mg/Liter
Natrium 500
Kalium 1450
Calcium 1200
Magnesium 130
Phosphor (gesamt) 950
Phosphor (anorg.) 750
Chlorid 1000
Carbonat 200
Citrat 1750
Tab 3 Mineralstoffe der Milch
Die bedeutendsten Mineralstoffe sind Calcium und Phosphat, nicht zuletzt aufgrund der Tatsache, daß das Verhältnis dieser beiden Mineralien in der Milch recht identisch mit dem des Zahnschmelzes ist. Kalium wirkt sich zudem positiv auf die Herzfunktion aus. In der Ernährung älterer Menschen wird eine erhöhte Calciumaufuahme wesentlich für die Verminderung von Osteoporose angesehen.
Die Deckung der täglich empfohlene Menge von 800 mg Calcium kann durch Verzehr folgender Nahrungsmittel erreicht werden:
660 ml Milch 120 g Käse
6200 gRindfleisch 29 Stck. Eier 6500 g Tomaten
An dieser Auflistung erkennt man, daß eine ausreichende Deckung des lebensnotwendigen Calcium- bedarfes ohne Milchprodukte kaum möglich ist.
5) VITAMINE DER MILCH
Vitamine sind essentielle Nahrungsbestandteile, die dem Menschen mit der Nahrung zugefuhrt wer- den müssen. Milch enthält alle Lebensnotwendigen Vitamine, kann jedoch den Vitaminbedarf des Menschen nicht vollständig decken (außer Vitamin B2). Der Vitamingehalt schwankt stark, da er äußerst futterungsabhängig ist. Neben ihrem ernährungsphysiologischen Wert haben die Vitamine Einfluß auf die Beschaffenheit von Milch und Milchprodukten:
Vitamin C. E: Antioxidantien der Milch Vitamin B2: gelbgrüne Farbe der Molke Vitamin A: gelbe Farbe der Butter
allgemein: Prosthetische Gruppen in Enzymen
Vitaminrnangel fuhrt zu Mangelerscheinungen (Avitaminosen). Fehlen Vitamine in unserer Nahrung, bedeutet dies bei:
Vitamin A: Nachtblindheit;Infektionsanfälligkeit Vitamin Bi: Wachstumsstörungen
Vitamin B2: Appetitlosigkeit; Verdauungsstörungen
Vitamin C: Müdigkeit;Paradontose; Infektionsanfälligkeit Vitamin D: Deformation des Skeletts
Nachfolgend sind die wichtigsten Vitamine der Milch (in mg/I) und der Tagesbedarf eines erwachse- nen Menschen (in mg) angegeben.
Vitamin mg!Liter Tagesbedarf (mg)
Vitamin A (Retinol) 0,1...0,5 1...5
Vitamin D (Calciferol) 0,2...0,4Ilg 0,01...0,02
Vitamin E (Tocopheroi) 1,0 10...30
Vitamin BI (Thiamin) 0,3...0,5 0,8...2
Vitamin B;! (Lactoflavin) 1•••2 0,9...3
Vitamin Bl2 (Cobalamin) 0,2...0,5 ug 2...10 Ilg
Vitamin C (Ascorbinsäure) 20 50...100
Tab-IVi/amineder Milch
Versuch 7) Vitamin B1 - Nachweis
Materialien: UV-Lampe
Demonstrationsreagenzglas
Chemikalien: Molke (enteiweißt) Na2S204 - Lsg.
Durchfuhrung:
Man gibt etwas der gelbgrünen, enteiweißten Molke in ein Reagenzglas und betrachtet sie unter der UV-Lampe bei einer Wellenlänge von 366 nm.Zu erkennen ist eine deutlich gelbe Fluoreszenz. An- schließend werden wenige Tropfen einer (stark verdünnten!) Natriumdithionit-Lösung zugegeben, gerade soviel wie benötigt wird, um eine Fluoreszenzlöschung zu erreichen.Nun wird das Reagenz- glas geschüttelt und die Fluoreszenz kehrt nach einiger Zeit zurück, da der vom Vitamin gebundene Wasserstoff vom Luftsauerstoff gebunden wird.
Na.,fu042-als Reduktionsmittel:
Reduktion des Vitamins:
s20l + 2H20 --+ 2S0/- + 2e- +4H+
S032- + 2H+ --+ S02t + H20
Flavinmonon ucleotid intermediäres Semichinon
- +
e H..
red. Flavinmononucleotid
(FMN) fluoreszierend (FMNHz) keine Fluoresz.
Erklärung:
Vitamin B2 (= Lactoflavin = 6,7-Dimethyl-9-ribityl-isoalloxazin) ist Wasserstoffiiberträger in jeder lebenden Zelle (als prostethische Gruppe der Flavinenzyme FMN und FAD) und dient dort in der Atmungskette dem Energiegewinn. Dabei wird Wasserstoff in einer knallgasähnlichen Reaktion auf Sauerstoff übertragen, jedoch in kleinen Raten, die dem Körper angepaßt sind und ATP liefern. Das Iso-alloxazin-System wirkt hier als reversibles .Redoxsystem", der Wasserstoff wird am NI und NIO angelagert. Milch ist,wie tierische Organe (Leber),aber auch Hefe, Schwarzbrot und Spinat wichtig- ster Vitamin B2Lieferant.
6) ENZYME DERMILCH
Enzyme beeinflussen chemische Reaktionen im Organismus sowohl in ihrer Richtung als auch in ihrer Geschwindigkeit und werden daher als Biokatalysatoren bezeichnet. Die Enzamtätigkeit wird durch die Temperatur und den pH-Wert gesteuert. Am wirksamsten sind Enzyme in einem Temperaturbe- reich von 25-50oe.Die Aktivität geht zurück, wenn die Temperatur über das Temperaturoptimum des jeweiligen Enzyms hinausgeht, da sie als Eiweiße hitzeempfindlich sind. Im allgemeinen werden die Enzyme zwischen 500
e
und 1400e
inaktiviert, wobei jedes Enzym eine spezielle Inaktivie- rungstemperatur aufweist. Aus diesem Grunde können negativ ausfallende Enzymnachweise Rück- schlüsse auf die Erhitzungstemperatur von Lebensmitteln zulassen.Enzym Wirkung
Lipasen spaltet Fett
Proteasen spaltet Peptidbindungen
Lactase spaltet Lactose
Dehydrogenase spaltet H2 ab und überträgt ihn
Tab5Enzyme derMilch
An dieser Stelle, vor dem nächsten Versuch muß etwas über die Methoden der Milchbehandlung gesagt werden. Prinzipiell wird unterschieden in Pasteurisierung und Ultrahocherhitzung. Bei der Pasteurisierung sind drei Verfahren bekannt, die sich in Temperatur und Zeit, in der die Milch erhitzt wird unterscheiden.Alle drei sind jedoch wesentlichschonender als das der Ultrahocherhitzung.
Pasteurisierung: • Dauererhitzung:62-65°C/30 min
• Kurzzeiterhitzung:71-74°C/30-40 sec.
• Hocherhitzung: 85-90°C/2-4 sec. Ultrahocherhitzung: • 135-150°C/4-20 sec.
Der Vorteil dieser Milcherhitzung liegt auf der Hand. Durch das Abtöten von pathogenen Keimen wird die Haltbarkeit des Produktes wesentlich verlängert, die Milchinhaltsstoffe werden jedoch nach- teilig beeinflußt. So werden die Molkenproteine zum Teil denaturiert, dadurch kann ein Kochge- schmack durch Bildung von Dimethylsulfiden und H2S auftreten, Maillard-Reaktionen und Karame- lisierung kommen vor und Vitaminverluste von bis zu 15% können beobachtet werden. Zudem wer- den einige der Enzyme deaktiviert,was im nächsten Versuch demonstriert werden soll.
Versuch 8) Schardinger-Enzvm als Nachweis aufHitzebehandlung
Materialien: regelbares Wasserbad Thermometer
Glaswanne o.Becherglas (> 2 Liter) 2 Demonstrationsreagenzgläser Stativmaterial mit Klammern Meßpipetten verseh. Größen
Chemikalien: Rohmilch H-Milch
Formalin (0,4%ig)
Methylenblaulsg.(0,04%ig) Paraffinöl
Durchfuhrung:
Zwei Reagenzgläser werden mit jeweils 20ml Milch befullt, das erste mit frischer Rohmilch, das zweite mit H-Milch. Nun gibt man in beide 3ml der 0,4%igen Formalin-Lösung und 2ml der 0,04%igen (wäßrigen!) Methylenblau-Lösung. Die Milch sollte deutlich blau gefärbt sein. Die An- sätze werden gemischt, 2 cm hoch mit Paraffinöl (zum Sauerstoffausschluß) überschichtet und in ein ca. 40°C warmes Wasserbad gestellt. Bei dieser Temperatur besitzt das Enzym sein Wirkungsopti- mum. Das Gemisch mit der Rohrnilch entfärbt sich nach ca. 2 min, das mit der H-Milch bleibt auch nach längerer Zeit blau.
Prinzip: • Schardinger-Enzym überträgt Wasserstoff auf geeignete Rezeptoren
• Enzym wird durch Erhitzen der Milch über 60°C zerstört
Formaldehyd als Wasserstoffdonator:
Methanal
Methylenblau als Wasserstoffakzeptor:
..
H-C-OH,
/OHH Methandiol
--.~ H-C?o + 2[H]
'OH
Ameisensäure
H3C'N~S ~N~ -~/CH3
I X I
CH3 CH3
Methylenblau
Schardinger-Enzym/2[l-Q
...
Luftsauerstoffa Jn
HH3C,
~ I _ I
# /GI3N S N
I I
O-I3 CH3
Leukomethylenblau (farblos)
Erklärung
Formalin (Methanal) liegt in wäßriger Lösung zu einem kleinen Anteil auch als Methandiol vor. Mit Hilfe des Schardinger-Enzyms (Aldehyddehydrogenase) aus der Milch wird Wasserstoff aus dem Diol abgespalten, wobei Methylenblau als Wasserstoffakzeptor wirkt und in das farblose Leukome- thylenblau übergeht. Frische Milch enthält dieses Schardinger-Enzym, welches durch Erhitzen über 60°C zerstört wird. Dieses ist bei der H-Milch der Fall. Somit kann das Methylenblau nicht zu der farblosen Leukoverbindung reduziert und der Ansatz nicht entfärbt werden. Je nach Erhitzungsver- fahren kann sogar die Art der Pasteurisierung (Dauererhitzung, Kurzzeiterhitzung, Hocherhitzung) erkannt werden, die von Handelsmarke zu Handelsmarke verschieden sein kann. So wird man bei einer dauererhitzten Milch eine rasche, bei einer kurzerhitzten eine langsamere und bei einer hocher- hitzten Milch keine Entfärbung mehr feststellen.
IV) JOGHURT
Nachdem bisher die Milch und ihre Inhaltsstoffe besprochen wurden, soll nun etwas über ein sehr wichtiges Milchprodukt, den Joghurt gesagt werden. Es gibt verschiedene Legenden um die Her- kunft dieses Sauermilchproduktes. Nach der Ersten soll ein Engel den Joghurt in einem Gefäß vom Himmel gebracht haben, eine Zweite besagt, daß ein Nomade Milch in einer Ziegenhaut als Behälter durch die Wüste auf dem Rücken eines Kamels beförderte. Als er Stunden später von der Milch probierte, war er überrascht, daß sie geronnen war und empfand den sauren Geschmack als sehr an- genehm. Aus dieser Geschichte erkennt man die Umstände und Bedingungen, die zur spontanen Milchsäuerung fuhren. Die Milch benötigt Wärme, Zeit und säurebildende Mikroorganismen.
Ausschlaggebender Faktor der Joghurtbereitung ist die Bildung von Milchsäure (und Aromastoffen) aus Lactose durch Milchsäurebakterien und das damit verbundene Dicklegen der Milch. Dabei er- folgt eine Phasenumwandlung der Milch von flüssig nach fest, die deshalb so interessant ist, da sich der Wassergehalt während des Vorgangs nicht ändert. Bei normaler Säuerung (Zugabe von Essig- säure bei 20°C) erfolgt keine Gelbildung, sondern lediglich eine Ausfällung des Caseins, da der Säu- erungsvorgang zu schnell vonstatten geht, um ein Netzwerk aufzubauen.
Eine Möglichkeit, auf direktem Wege ein Milchgel zu erhalten, ist die des folgenden Versuchs.
Versuch 9) Herstellung eines Joghurts
Materialien: regelbares Wasserbad Thermometer
Eisbad (O°C)
Becherglas (250 ml) Glasstab
Meßpipette (10 ml)
Chemikalien: H-Milch (100ml)
Milchsäure (2ml;40%ig) Magermilchpulver (3 Gramm)
Durchfuhrung:
Das Milchpulver wird in die Milch eingerührt und (am Besten über Nacht) stehengelassen. Dieses dient zur Erhöhung des Trockenmassbestandteils im fertigen Produkt und damit zu einer größeren Festigkeit. Die Milch und die Milchsäure werden getrennt in einem Eisbad auf O°C herabgekühlt und anschließend in einem Becherglas zusammengegeben. Man rührt kurz mit einem Glasstab durch und stellt das Gemisch in ein ca. 70°C warmes Wasserbad. Nach etwa 30 min ist ein relativ festes Gel (Joghurt) entstanden, das sich, wenn man es anschließend kaltstellt weiter verfestigt. Dieser Joghurt entspricht jedoch nicht dem Handelsüblichen, denn dort sorgen Milchsäurebakterien für die langsa- me, gleichmäßige Säuerung (s. später).
Erklärung:
Bei niedriger Temperatur wird die Gelbildungsgeschwindigkeit sehr gering (auch bei der herkömmlichen Joghurtbereitung, da die Milchsäurebakterien ihre optimalen Lebensbedingungen bei 40°Cbesitzen und somit auch bei dieser Temperatur erst ein Netzwerk in optimaler Geschwindigkeit ausgebilden können).Bei O°C, wie im Versuch tritt keine Koagulation ein, auch wenn mit Milchsäure spontan gesäuert wird. Die Milchsäure kann gleichmäßig in der Milch verteilt werden und erst bei der Erwärmung im Wasserbad wirkt sie gleichmäßig auf die Caseinmicellen ein (erschütterungsfreier Zustand vorausgesetzt). Säuerung und Gelbildung sind somit entkoppelt.
Milchsäuregärung
kolloidale Lösung (Versuch 9)
Gel(Joghurt) Niederschlag
(Versuch 3a)
kolloidale Lösung
Abh 14 Mögli chkeitenderMilchsäuerung
Bei der herkömmlichen Milchsäuerung sorgen Milchsäurebakterien fur die langsame (6-8 h), gleich- mäßige Säuerung der Milch. Die Bakterienstämme besitzen unterschiedliche Eigenschaften (Lebens- bedingungen), die zu unterschiedlichen Produkten fuhren (Art der gebildeten Milchsäure).Die Kultu- ren bestehen aus verschiedenen Stämmen, die symbiontisch zusammenleben. Bebrütet wird unter Zu- satz von ca. 2% Betriebskultur bei 42-45°Cca.4 Stunden. Genußfähiger Joghurt hat einen pH-Wert von etwa 4 - 4,5 und enthält 0,7 - 1,2% Milchsäure (säuert im Becher noch nach).
Art
Lactobacillus acidophilus Lactobacillus lactis Streptococcus lactis
Streptococcus thermophilus Bifidobakterium bifido
Tab 6 Milchsäurebakterien
Milchsäure. .. Bemerkungen
DL thermophil homofermentativ D(-) thermophil heterofermentativ L(+) mesophil homofermentativ L(+) thermophil homofermentativ L+>D- mesophil heterofermentativ
Die Milchsäure kann je nachArt der Milchsäurebakterien auf verschiedenen Wegen gebildet werden.
An dieser Stelle sind deren drei zu nennen, bei denen neben Lactat auch noch Acetat und CO2
gebildet werden:
Glucose a) Homofennentative Gärung
~
t
~ b) Bifidus-Weg (pentosephosphat)Fru- I.6- DP Fru-6-P Glc-6-P c)Heterofennentative Gärung
1
I1 !
Acetyl-P Erythrose-4- P Gluconat-6-P
}--Fru-6-P
1
Pentosc-P Xylulose-5-P+ cO2
~
i 1
~Triose-3-P Acetyl-P Triose-3-P Triose-3-P Acetyl-P
! ! !
j
Pyruvat Pyruvat Pyruvat
1 1 !
Lactat Aceat Lactat Lactat Acetat
(Ethanol)
A B C