Hinweis
Bei dieser Datei handelt es sich um ein Protokoll, das einen Vortrag im Rahmen des Chemielehramtsstudiums an der Uni Marburg referiert. Zur besseren
Durchsuchbarkeit wurde zudem eine Texterkennung durchgeführt und hinter das eingescannte Bild gelegt, so dass Copy & Paste möglich ist – aber Vorsicht, die Texterkennung wurde nicht korrigiert und ist gerade bei schlecht leserlichen Dateien mit Fehlern behaftet.
Alle mehr als 700 Protokolle (Anfang 2007) können auf der Seite
http://www.chids.de/veranstaltungen/uebungen_experimentalvortrag.html eingesehen und heruntergeladen werden.
Zudem stehen auf der Seite www.chids.de weitere Versuche, Lernzirkel und Staatsexamensarbeiten bereit.
Dr. Ph. Reiß, im Juli 2007
Experimentalvortrag im Rahmen des Lehramtsstudiums für Chemie an der Philipps-Universität-Marburg
Fachbereich Chemie
Leiter: Prof Dr. Perst, Dr. Gerstner, Dr. Butenuth Referentin: Vera Kessel
Vortrag vom 08.05.96
Stoffwechselprodukt des l\lenschen
RUild Uln dei] Urin( .:
SS 1996
- ..
"I-~/ \,
"
:1 ,
Inhaltsverzeichnis
1.Einleitung 3
2.Bildungund Bedeutung des Urins in unserem Körper.. 3
3.DieInhaltstoffe des Harns .4
3.1. Der Harnstoff 4
3.1.1. Bildung des Harnstoffs 4
3.1.2. Harnstotfuachweis über Biuret 8
3.2. Die Harnsäure 9
3.2.1. Bildung der Harnsäure 9
3.2.2.Harnsäurenachweis 11
3.3.Glucose 12
3.3.1.Glucosenachweis mit der FehlingschenProbe 12
3.4.Proteine .- 13
3.4.1.Eiweißbestimmung mit Ninhydrin 13
4.Anwendung des Urins und seiner Bestandteile 15
4.1.Der Schwangerschaftstest 15
4.1.1.Durchfuhrungdes Schwangerschaftstests 15 4.1.2.Das Prinzip des Schwangerschaftstests 16
4.2.Urin alsWaschmittel.. 18
4.2.1.Waschen mit Urin 18
4.3.Historische Indigofärbung mit Urin 19
4.3.1. Färben von Wollstoff mit Indigo 19
4.4.Aminoplasten 21
4.4.1.Darstellung von Aminoplasten " 21
5.Literatur 22
1. Einleitung
Im Zuge einer sich verstärkenden Diskussion über Urin als Naturstoffund Medikament, kann es interessant sein, sich auch in naturwissenschaftlichen Kreisen mit diesem Thema ausein- anderzusetzen. Dabei sollten uns Aussagen von Anwendern, die häufig von großen Erfolgen bei der Eigenurinbehandlung berichten, hellhörig machen. Insbesondere, da viele Ratschläge unserer Großmütter über die Medikation mit Urin, eine wissenschaftlich begründete Erklärung gefunden haben.
In meinem Vortrag sollte es jedoch nicht um solche Heilungsmethoden, oder deren wissen- schaftlichen Erklärung gehen. Es sollte eher der Blick für dieses Naturprodukt geschärft und der Versuch gestartetwerden, den uns anerzogenen Ekel zum Urin abzubauen.
r,
2. Bildung und Bedeutung des Urins in unserem KörperUrin ist neben dem Kot die wichtigste Ausscheidung des Körpers. In ihm werden viele Stoffe, die der Organismus nicht direkt benötigt, ausgeschieden, wobei der wichtigste Bestandteil des Urins der Harnstoffist. Dieser Harnstoff wird in der Leber produziert und über die Blutbahn zur Niere transportiert, wo er über semipermeable Membranen angereichert und über die Harnwege als Urin ausgeschieden werden kann.
Neben dem Harnstoff, als Hauptbestandteil des Harns, befinden noch viele weitere Stoffe im Urin. Meist nicht in angereicherter Form, aber doch in ähnlich hohen Konzentrationen wie im Blut. Zu nennen wären hier:die Harnsäure als Abbauprodukt purinreicher Nahrungsmittel, das Creatinin als Abbauprodukt der Muskelkontraktion, Proteine in Form von Antikörper,
, ,.
Substanzen Proteine
Glucose
ß,mylase (4-Nitrophenyl-a,D-Maltoheptaosid) . (4-Nitrophenyl-a, D-Maltopenta/hexaosld) . (2-Chlor-4-Nitropheny1-ß,D-Maltoheptaosld) Kalium
Natrium Chlorid Phosphat Calcium
Ammoniu mionen titrierbare Acidität Creatin
Creatinin (pro kg Körpergewicht)
Harnstoff-N(abhängig von der Proteinzufuhr) Harnsäure (abhängig von der Purinzufuhr)
o
-Aminolävulinsäure Porphobilinogen Uroporphyrine Coproporphyrine DopaminNoradrenalin Adrenalin
3 - Methy1-4 - Hydroxymandelsäure (Vanillinmande lsäure) 5-Hydroxyindo1essigsäure
.,~..
Ausscheidung/24 Stunden 45 - 75 mg 15 - 130 mg unter 600 U /1 unter 300 U/1
unter 600 U /1
35 - 80 mmol ~
c'. , - .!,a,.
100 - 220 mrnol~ ~,Ir-S'"~
100 - 240 mmol~ 3, )-I,G',.
25- 50mmol~.,t$-..(.~~
3 - 8 mmol:
t'. ...'
-~f3, 20 - 70 mmolunter 40 mmol 15 - 250 mg Männer 15 - 30 mg/kg
Frauen 10 - 25 mg/kg 6 - 15 g
0,2 - 1,0 g unter 7 mg unter 2 mg . unter 20 p.g
unter 80 ug 200 - 450 ug
20 - 100 ug 5 - 15 p.g 3 - 7 mg 2 - 7 mg
Tab.I:Ausscheidung von Harnb estandteilenbeimgesundenErwachsenen (Quelle:Rick 1990,S.409)
3.Die Inhaltstoffe des Harns
3.1. Der Harnstoff
I )
3.1.1. Bildung des HarnstoffsÜberschüssige Aminosäuren, die nicht zur Synthese von Proteinen und anderen Biomolekülen verwendet werden, lassen sich im Gegensatz zu Fettsäuren und Glukose im Körper nicht speichern; sie werden aber auch nicht ausgeschieden, sondern dienen im Stoffwechsel als Brennstoff. Das Kohlenstoffgerüst wird im Citratzyklus zu C02 oxidiert oder in wichtige Bausteine derZellen, wie:Acetyl-CoA oder Pyruvat umgewandelt. Die meisten Aminogruppen der überschüssigen Aminosäuren werden jedoch in Harnstoff umgewandelt, der in >der ' Hauptsache mit dem Urin ausgeschieden wird. Ein Teil des Urins wirdauch im Darm wieder zu C02 und 1\TH3 zersetzt.
...
a) Der Amionsäureabbauabbau
Der Abbauprozess der Aminosäuren ist in der Leber lokalisiert. Hier wird zunächst die a- Aminogruppe der entsprechenden Aminosäure auf cc-Ketoglutarat übertragen, wobei Glutamat entsteht. Diese Reaktion wird von der Aminotransferase katalysiert. Das Enzym überträgt 0.-
Aminogruppen von verschiedenen Aminosäuren auf cc-Ketoglutarat. Zurück bleiben 0.- Ketosäuren.
HI
+H N-C-R
J I
coo-
Aminosäure Glutamat
Reaktion 1: Transaminierung von AminosäurenzuGlutamat (Quelle:Stryer 1990, S.51?)
Diese Übertragung ist wichtig, da zum emen der nächste wichtige Schritt für den Aminosäureabbau, die oxidative Desaminierung, hoch selektiv nur mit Glutamat abläuft und zum anderen in dieser Reaktion .die Schaltstelle zum Ein- und Ausschalten des Aminosäureabbaus liegt, denn nur bei einem Aminosäureüberschuß soll die Reaktion ablaufen.
In der Natur werden viele wichtige Reaktionen in Teilreaktionen zerlegt, um dem Organismus eine größere Kontrollmöglichkeit über den Reaktionsablauf zu geben.
Bei der anschließenden oxidativen Desaminierung wird Glutamat wieder zu u-Ketoglutarat und einem Ammoniumion gespalten. Diese Reakion wird von der Glutamat-Dehydrogenase katalysiert, der NAD+ als Coenzym dient. Es reicht als Erklärung aus, Daß NAO+
(Nikotinamidadenosindinukleotid) eine Verbindung ist, die in der Lage ist Hydridionen auf- zunehmen. Es ist also ein Oxidationsmittel.
NH +
I J
H-C-COO- CHI 2
CHI 2
coo-I
Glutamat
+ NAD+ +H20
===
NH4+ +(oder NADP+)
°
c-coo-11CHI 2
CHI 2
coo-I
a-Ketoglutarat
+ NADH +W (oder NADPH)
Reaktion2:Oxidative Desaminierung des Glutamats (Quelle:Stryer 1990,S.518 .)
Das gebildete Ammonuimion ist giftig für den Organismus. Daher wird der Teil, der nicht,für . die Synthese neuer Aminosäuren gebraucht wird, bei den Landwirbeltieren auf dem schnellsten Wege in Harnstoff überfuhrt und in dieser Form über den Urinausgeschi'~~en.
... . ...
I.-Am'",,'u,') (
a-Ketosäure
a-Ketoglutarat
Glutamat
o
11
H2N-C-NH 2 Harnstoff
Abb.l:Schematische Darstellung des Werdegangs der a.-Aminogruppen vom Proteinen bis zum Harnstoff (Quelle: Stryer 1990, S.518)
b) Der HarnstoffzykJus
Die Umwandlung der Ammoniumionen in Harnstoff findet im Harnstoffzyklus statt, der eben- falls in der Leber lokalisiert ist. Hier wird über einen mehrstufigen Prozess aus C02 und NH4+
das Diamid der Kohlensäure synthetisiert.
Der Harnstoffzyklus (nach Hans Krebs auch Krebszyklus genannt) ist der erste zyklisch ver-
( 1
laufende Stoffwechselweg, der entdeckt wurde (5 Jahre früher als der Citratzyklus). Eines der Stickstoffatome des in diesen Zyklus synthetisierten Harnstoffs stammt aus einer Aminosäure, dem Aspartat. Der andere Stickstoff und der Kohlenstoff stammen von NH4+ und C02.Ornithin ist der Carrier dieser C- und N-Atome.
Fum",! ~~";"
~91";)\
Aspartat Citrullin R''''':''NH2
Abb 2: Der Harnstoffzyklus
(Quelle: Stryer 1990, S.522)
Ornithin
) / ->:
CarbamoylphosphatV' R-C-NH2
o11
Zunächst wird in einer komplexen Reaktion aus NH4+, C02, ATP (Adenosintriphosphat) und H20 das Carbamoylphosphat. Diese Reaktion wird von der Carbamoylphosphat-Synthetase katalysiert.
o 0
+ 11 11
cO2 +NH4 +2 ATP+H20 ---.. H2N - C- O- ) - 0 - +2 ADP +Pi+3 H+
0- Carbamoylphosphat
Reaktion 3:Bildung des Carbamoylphosphats (Quelle:Stryer 1990,5.523)
Das Posphatderivat besitzt aufgrund seiner Anhydridbindung ein hohes Übertragungspotential der Carbamoylgruppe, welche mit Ornithin zu Citrullin reagiert. Die Ornithin- Transcarbamoylase ist das katalysierendeEnzymdieser Reaktion.
o
"
+H N H-N-C-NH
31 I 2
CH2 0 0 CH2
I 11 11 f
?H
2 +H
2 N - C - 0 - f - 0 -~?H
2 +Pi
?H
20- ?H
2H-C-NH+ H-C-NH+
I 3 f 3
coo- coo-
Ornithin Carbamoylphosphat Citrullin Reaktion 4:' Bildung von Citrullin
(Quelle: Stryer 1990, S.523)
+H N COO-
211 I
H-N-C-N-C-H
I I I
CH2 H CH2
I 1
CH2
coo-
CHI 2
H-C~NHI +
I 3
coo-
ATP AMP+ PPj
~L
coo-I ++H N-C-H
3 I
CH2
coo-
IDie Argininosuccinat-Synthetase katalysiert dann die Kondensation von Citrullin und Aspartat, wobei ATP in AMP (Adenosinmonophosphat) umgewandelt wird. Da indieser Reaktion ATP verbraucht wird, ist der Reaktionsschritt irreversibel.
o
H-N-C-NHI 11 2
CH2
CHI 2
CHI 2
H-C-NHI +
I 3
coo-
Citrullin Aspartat Argininosuccinat
Reaktion 5: Kondensation von Citrullin und Aspartat (Quelle: Stryer1990, 5.523)
Aus dem Argininosuccinat wird unter Abspaltung von Fumarat Arginin, das, durch die
Ti
Arginase katalysiert, hydrolytisch in Ornithin und Harnstoff gespalten wird.+H N COO-
2" I
H-N-C-N-C-H
I I 1
CH2 H CH2
I t
CH2
coo-
~CH1 2 H-C-NHI +
I 3
coo-
Argininosuccinat
+H N2 HN-C-NH11
I 2
CH2
CHI 2
CHI 2
H-C-NHI +
1 3
COO-
Arginin Fumarat Harnstoff
NH +
I 3
CH2
CHt 2 CHI 2
H-C-NHI +
I 3
COO- Ornithin Reaktion6: Bildung von Harnstoff aus Argininosuccinat
(Quelle: Strycr 1990, S.522)
Auf diese Weise wird also in den terrestrischen Wirbeltieren der Harnstoff gebildet. Vögel . scheiden aufgrund ihres begrenzten Wasserhaushaltes Harnsäure Anstelle von Harnstoff aus.
Aber auch Menschen bilden zu einem gewissen Teil Harnsäure, die bei Gesunden ebenfalls mit dem Urin ausgeschieden wird.
3.1.2. HarnstotTnachweis über Biuret
(Quelle:Beyer 1976,S.302)
Materialien: Trockenschrank Becherglas Filter
Bunsenbrenner
Demonstrationsreagenzglas
Chemikalien:
Ethanol (technisch) IO%-ige Natronlauge 1%-ige Kupfersulfat-Lsg.
Urin
Zunächst wurde der Harnstoff durch Einengen des Urins im Trockenschrank ausgefallt und über UmkristaIIisieren mit Ethanol gereinigt.
Der so isolierte Harnstoff wurde über der Bunsenbrennerflamme erhitzt. Zunächst schmolz der Feststoff. Bei weiterem Erhitzen zerfiel der Harnstoff, wobei Ammoniak ausgaste und ein weißer Feststoff zurück blieb.Dieser wurde in etwas lO%-iger Natronlauge aufgenommen und tropfenweise mit 1%-iger Kupfersulfatlösung versetzt. Die Lösung färbte sich zunächst rosa 9und bei weiterer Zugabe der Kupfersulfatlösung violetrot.
Den Reaktionsmechanismus muß man sich folgendermaßen vorstellen:
Zunächst hat sich aus einem Molekül Harnstoff, unter Abspaltung von Ammoniak Isocyansäure gebildet.
o
11
HIJ-C-AJH
~
:c
~•HA;
=C =0Reaktion 7:Bildung der Isocyansäureaus Harnstoff (Quelle:Beyer 1976,5.302)
Mit einem weiteren Molekül Harnstoff reagiert diese zum Biuretreagenz.
I-I{;=c=o
11
o
-I-
~ JJ-c -IJ~ ~
,0
0Ir 11
HoG,
)J -C -JJII - c
-A.J~&~,L Reaktion 8:Bildung des Buiretrcagenzes aus Isocyansäureund Harn stoff
(Quelle:Bcycr 1976.S.:102)
Aber auch Menschen bilden zu einem gewissen Teil Harnsäure, die bei Gesunden ebenfallsmit dem Urin ausgeschieden wird.
3.1.2. Harnstoffnachweis über Biuret
(Quelle: Beyer1976, S.302)
Materialien:
Trockenschrank Becherglas Filter
Bunsenbrenner
Demonstrationsreagenzglas
Chemikalien:
Ethanol (technisch) 10%-ige Natronlauge 1%-ige Kupfersulfat-Lsg.
Urin
Zunächst wurde der Harnstoff durch Einengen des Urins im Trockenschrank ausgefallt und über Umkristallisieren mit Ethanol gereinigt.
Der so isolierte Harnstoff wurde über der Bunsenbrennerflamme erhitzt. Zunächst schmolz der Feststoff Bei weiterem Erhitzen zerfiel der Harnstoff: wobei Ammoniak ausgaste und ein weißer Feststoff zurück blieb. Dieser wurde in etwas lO%-iger Natronlauge aufgenommen und tropfenweise mit 1%-iger Kupfersulfatlösung versetzt. Die Lösung färbte sich zunächst rosa 9und bei weiterer Zugabe der Kupfersulfatlösung violetrot.
Den Reaktionsmechanismus muß man sich folgendermaßen vorstellen:
Zunächst hat sich aus einem Molekül Harnstoff: unter Abspaltung von Ammoniak Isocyansäure gebildet.
o
11
H -e IJ-C-/uH :c
Reaktion 7: Bildungderlsocyansäure aus Harnstoff (Quelle: Beyer 1976, S.302)
Mit einem weiteren Molekül Harnstoff reagiert dieseZUlU Biuretreagenz.
11
o
"- ~ u-c -IJ~ ~
(,.0
0'11 11
11<, ,u -c
-J..JII-C -.lJ~t8~~
Reaktion 8: Bildung des Buiretreagenzes aus Isocyansäure und Harnstoff (Quelle: Bcyer 1976, 5.302)
-
I...,.,. ';', ,',,'", ',-,<.~.:... ;....\Im Basischen bildet sich über eine Säure-Base-Reaktion und unter Zugabe von Kupfer U- Ionen ein Chelatkomplex mit Kupfer II als Zentralatom und vier Stickstoffatomen aus Biuret als Liganden.Dieser Komplex ist violettrot.
I .
Reaktion 9:Bildung eines Kupfer Il-Komplexes aus Biuret und Kupfer Il-Ionen (Quelle:Beyer 1976, S.302)
Der Nachweis ist spezifisch für Harnstoff
3.2. Die Harnsäure
3.2.1. Bildung der Harnsäure
(Quelle:Stryer 1990,S.645)
Auch die Harnsäure ist ein Abbauprodukt, das, bei gesunden Organismen, über den Harn aus
I '
dem Körper ausgeschieden wird.Bei Säugetieren ist es jedoch kein Abbauprodukt der Aminosäuren (Vögel scheiden aufgrund ihres geringen Wasserhaushaltes auch bei Aminosäureabbau Harnsäure aus), sondern entsteht beim Zersetzen von Nucleosiden.NucIeoside sind die kleinsten Bausteine der DNA und sind aus den entsprechenden Basen:
Tymin, Adenosin, Cytosin und Guanin aufgebaut, die über eine Stickstoff-Sauerstoff-Bindung mit einem Ribosemolekül am l'-Ende verbunden sind. Am 5'-Ende ist die Ribose über eine Anhydridbindung mit einem Phosphat verbunden.
Die Nucleoside einer Zelle unterliegen einem kontinuierlichem Umsatz. Am Beispiel 'des' Abbaus von AMP (Adenosinmonophosphat) läßt sich die Umwan~lung von Purinen zu
Harnsäure exemplarisch darstellen. ( ;
o
11
HN/C'-C---N~
----> I 11 ~C H
HC"", / C---NI
N I
Ribose- ® IMP
o11
Hypoxanthin
/
..._..' ;...•......:.. '.':::
Harnsäure (Ketoform)
Reaktion 10:Der Abbau von AMP zu Harnsäure (Quelle:Stryer 1990, S.645)
Xanthin
AMP wird zunächst zu IMP (Inosinmopophosphat) hydrolysiert und anschließend hydrolytisch in Hypoxanthin (die freie Base) und Ribose-S' -Phosphat gespalten.Die Xanthin-Oxidase kata- lysiert dann die Oxidation des Hypoxanthin zu Xanthin und weiter zu Urat.Oxidationsmittel ist bei dieser Reaktion der molekulare Sauerstoff; er wird zu H202 reduziert, das dann durch die Katalase in H20 und 02 zelegt wird.
Auch die Harnsäure gelangt über die Blutbahn in die Niere und wird dort im Urin angereichert und über die Harnwege ausgeschieden. Die Harnsäurekonzentration im Urin sagt also nichts über die Konzentrationen im Blut aus.Es gibt Menschen die aus einem Defekt heraus nicht in der Lage sind Harnsäure anzureichern und auszuscheiden.-Dieser Defekt tritt verstärkt im fort- geschittenen Alter auf. Bei diesen Menschen kristallisiert die Harnsäure in den Gelenken aus und sie bekommen Gicht. Sie müssen purinreiche Nahrungsmittel wie Fleisch meiden. Eine ent- sprechende Diät kann die Symtome nur lindern jedoch nicht beheben, da der eigene Organismus ja ebenfalls Purine erzeugt und wieder abbaut.
( ;
3.2.2. Harnsäurenachweis
3.) Fällung der Harnsäure
(Quelle: Holleman; Schuler 1965, S.92)
Materialien:
11 Standrundkolben 1DOml Meßzylinder Filter
Chemikalien:
Hel(konz.)
Ethanol (technisch) Urin
Zur Vorbereitung des Hamsäurenachweises muß die Säure zunächst aus demUrin gefallt wer- den. Dazu wurde 11 Urin mit IOOml konz. Hel versetzt und 48-72 Stunden zum Kristallisieren ruhen gelassen. Das Reaktiongemisch färbte sich tief dunkelbraun und die Harnsäure fiel als dunkelbraune Kristalle aus. Diese Kristalle wurden 4-mal mit Ethanol gewaschen und ge- trocknet.
b.) Nachweis als Murexid
(Quelle: Beyer 1976, S.704-705)
Materialien:
Porzellanschale -Tropfpipette
Chemikalien:
HN03 (konz.) 2nAmmoniak gefällte Harnsäure
In einer Porzellanschale wurde eine Spatelspitze Harnsäure mit zwei Tropfen konz.
Salpetersäure versetzt und über der Bunsenbrennerflamme zur Trockne eingedampft. Der Rückstand wurde in 2n NH3aufgenommen, wobei ein purpumer Farbstoff entstand.
Der Mechanismus dieser Reaktion kann folgendermaßen erklärt werden:
o o ?
0 0 0U.H
lc
T 11~ ~. 1I. )l ~H
T~~ . T r ~HC-~H2 . : ~HC-~H:!HX Y ~
H~
)Lll
)=0 HIt) H)~ I ~ H~I
"'1 i ·'H1
I
- - - +I - , - I I
~l io~x ~ 0 "~.... OH oAx~o
-
~HJ o~x--AoH H H II H
Harnsäure
o
0Ä
",,0 NH2 " .//~
H~
r
I H../f,. ~HI ':1' - -
I I I !
1),0~N ~-o ~-~
, c-: "'_ . /~" ()~ '~/ ....0
H H
Alloxan Urarnit
Reaktion 11: Reaktionsmechanismus der Murexidreaktion (Quelle: Bcyer 1976, S.7(6)
~rarnil
.._•...__I _.~" .':'
Beim Erhitzen der Harnsäure mit Salpetersäure laufen zwei Reaktionen parallel ab; zum einen wird ein Teil der Harnsäure zu Alloxan oxidiert, zum anderen findet eine hydrolytische Spaltung der Harnsäure unter Abspaltung von CO2 und NB3 zu Uramil statt. Uramil und Alloxan vereinigen sich im Alkalischen zu Murexid, einem purpurfarbenem Farbstoff.
3.3. Glucose
Im Gegensatz zur Harnsäure und zum Harnstoff, spiegelt die Glucosekonzentration im Urin jene im Blut wieder, da Zucker durch die Niere nicht angereichert werden können. Wie aus Tabelle 1 ersichtlich ist, scheidet der Mensch im Schnitt 45-75 mg Glucose täglich aus. Liegt die Menge an ausgeschiedener Glucose wesentlich höher, so ist der Mensch zuckerkrank.
Ein qualitativer Nachweis der Glucose im Harn gesunder Menscher also bei einer Konzentration von 25-50 mg/l ist mit der Fehlingschen Probe gut möglich.
3.3.1. Glucosenachweis mit der Fehling'schenProbe (Quelle: Rick 1990, S.428)
Materialien 50ml Becherglas Bunsenbrenner
Dreifuß mit Drahtnetz 50ml Meßkolben
Chemikalien
Fehlingsches Reagenz:1,5g CUS04.5 H20 6,OgNa,K-Tartrat in 3,3%-iger NaOH zu 11 gelöst
Urin
1 1
20 ml Urin wurde mit der gleichen Menge Fehlingschem Reagenz versetzt und über dem Bunsenbrenner erhitzt. Während des Erwärmens entfärbte sich die Reaktionslösung zunächst allmählich, um in der Siedehitze ziegelrot zu werden.Grundlage des Reaktionsmechanismus' ist die reduzierende Wirkung der Glucose.Die Glucose besitzt eine Keto-Enol-Tautomerie, wobei die Enolfonn leicht durch CuII-Ionen oxidiert werden kann. Es wird das di-Keton gebildet. Das Kupfer-Il-Sulfat wird zum ziegelroten Kupfer-I-Hydroxid reduziert.Bei besonders hohen Zuckerkonzentrationen fällt das CuOH als' ziegelroter Niederschlag aus.
, ,.
u 0
" C ~ /-I, ()fI. 1-1
0/' <, //
I C
c
H C , 0/-1- J.l
C-OI-J11
f.JC==OI
J.l
0 c 1-1
~, ,
,
~ I-IOCI+ +Ut.S~41IUR I-IOCI-I+ Cu- 01-1
J.JcoH-
I -- J.I<-SOq,
I
#4COIJ 1-1
L 01-1("hf.)
1-1(01-1 , ,
I
/-ICOII I-JColI
C~OH J I
C /J.l
o 1-1 CH,zOI-l
Reaktion 12: Oxidation der Glucose in der Fehlingschen Probe
'I
(Quelle: Rick 1990, 5.428)3.4. Proteine
Beim gesunden Erwachsenen liegt die Tagesmenge der ausgeschiendenen Proteine bei 15-130 mg. Sie bestehen in der Regel aus Antikörpern und spiegeln ähnlich der Glucosekonzentration die Mengen im Blutserum wieder. Zusätzlich kommt es aber auch zu Verunreinigungen durch Fremdkörper in der Harnblase. Diese Verunreinigungen sind be- sonders hoch, bei einer entzündlichen Erkrankung der Harnwege. In diesem Fall bestehen die Proteine in der Hauptsache aus Erytrocyten. Es ist möglich einen spezifischen Nachweis von Proteinen getrennt nach Erytrocyten und anderen Eiweißen zu machen. Im Rahmen meines Vortrags wäre dies jedoch zu aufwendig gewesen. Daher habe ich mich auf die allgemeine Proteinbestimmung beschränkt.
3.4.t. Eiweißbestimmung mit Ninhydrin
(Quelle: Brewer; Pesce; Ashworth 1977, S.78fi)
Ninhydrin ist eine Substanz, die in der Biochemie vorrangig zur Proteinbestimmung im Rahmen der Chromatographie angewandt wird. Sie ist aber auch im wässrigen Melieur wirk- sam. Für die Reaktion müssen die Proteine jedoch zunächst in die Aminosäuren gespalten
:!' •
werden.
a) Aufbereitung der Proteine
Materialien:
Wasserbad mit Termostat Demonstrationsreagenzglas
Chemikalien:
konz. Hel Urin
Zu Spaltung der Proteine in die entsprechenden Aminosäuren, wurden 40 mlUrin mit 4 ml konz. Hel versetzt und 24 h imWasserbad bei 900e inkubiert. Anschließend wurde bis zur Trockne eingedampft, um die Salzsäure aus dem Reaktionsgemisch zu entfernen, und in 40 ml H20 aufgenommen.
b) Nachweis mitNinhydrin
Materialien:
Dmonstrationsreagenzglas 50ml Meßzylinder
Meßpipette
Chemikalien:
ges. Ninhydrin-Lsg.
aufbereiteter Urin
Zu dieser vorbehandelten Urinprobe wurden 3mI einer gesättigten Ninhydrinlösung gegeben.
Nach einer Inkubationszeit von 10 min färbte sich die Lösung allmählich violett. Nach weiteren 10minwar die Violettfärbung abgeschlossen.
Die Reaktion beruht auf der reduzierenden Wirkung der Aminogruppe einer Aminosäure.
Dabei wird die Aminogruppe am a-C-Atom der Säure zur Schiffsehen Base oxdiert und an- schließend zum entsprechndem Aldehyden und Ammoniak hydrolysiert. Gleichzeitig geht ox- Ninhydrin in seine reduzierte Formüber. Zusammen mit einem weiteren Molekül ox-Ninhydrin und dem gebildeten Ammoniak entsteht Ruhemanns-Purpur, ein purpur- bis blaufarbener Farbstoff.
o
2-Hydroxy-1,3·;ndandion (f'tdulftt1., Ntnhydnn)
H OH
o
212-Othydroxy-1,] -ind.ndion
~teu.rttS Nlnhydnn)
HzO (°2
R
Hp
R Rt I
1,°
HC-NH+) (-NH C
t 'H
~
coo-
I COOHI' Amfnosäure 0 Aldehyd
.N
o
0Ru~-Purpur
---
Reaktion 13: Reaktionsmechanismus der Ninhydrinrcaktion (Quelle: Brcwer; Pcscc; Ashworth 1977, S.78)
4. Anwendung des Urins und seiner Bestandteile
Neben der Analyse des Urin in der Medizin, gibt es weitere Anwendungsmöglichkeiten des Urins und seines Hauptinhaltstoffs, dem Harnstoff Eine moderne Anwendung ist der Schwangerschaftstest, wobei man sich streiten kann, ob dieser nicht noch zu den Analysen zu zählenist.
Für weitere Bereiche muß man häufig tief in der Geschichte zurück gehen, da der Urin als Rohstoff heute in den Hintergrund getreten ist. Anwendungbereiche waren der Urin als Waschmittel oder zur Indigofärbung.
4.1. Der Schwangerschaftstest
Ist eine Frau schwanger, so streut ihr Körper ein Hormon aus, das Choriongonadotropin (heG), oder auch Gelbkörperehenhormon heißt. Da es sich um ein Hormon handelt, das die semipermeablen Membranen der Niere überschreiten kann, ist es im Urin in gleich hoher Konzentration wie im Blut vorhanden. Der Schwangeschaftstest beruht nun auf dem Nachweis dieses Hormons im Urin.
Da das Hormon nicht wärend der gesamten Schwangerschaft konstant im Körper vorhanden ist, sondern seine Konzentration bis zum funften Monat ansteigt, am Anfang des fünften Monats sein Maximum hat und anschließen wieder steil abfällt, ist ein Nachweis nur bis zum sechsten Schwangerschaftsmonat möglich.
4.1.1.Durchführung d-es Schwangerschaftstests
Materialien:.
käuflicher Schwangerschaftstest (Eva-Test)
Tropfpipette
Chemikalien:
Urin
Der Urin wurde mit einer Pipette gemäß der Anleitung auf die Auftragszone gegeben, mit dem beigegebenen Deckel geschlossen und das Teststäbchen umgedreht. Nach etwa 5 min konnte das Ergebnis abgelesen werden.
1 !
4.1.2. Das Prinzip des Schwangerschaftstests
das Prinzip des Schangerschaftstests beruht auf einer Antigen-Antikörper-Reaktion. Der Begriff Antigen bezeichnet eine Fremdsubstanz in einem Körper, die vom Organismus auch als solche erkannt wird und gegen die Antikörper gebildet wird.In diesem Fall ist das Antigen das Gelbkörperehenhormondas über eine Präzibitatbildung mit Antikörper nachgewiesen wird.
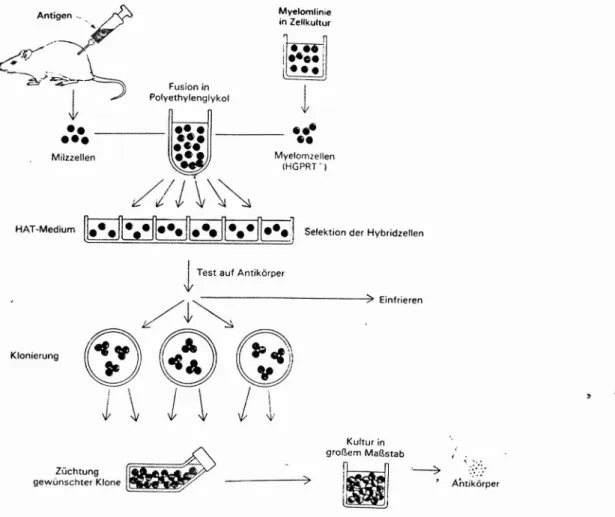
Der monoklonale Antikörper kann folgendermaßen hergestellt werden (vgl. Abbildung 3): Zunächst wird das isolierten Gelbkörperehenhormon einer Schwangeren in eine Maus injiziert. Der Organismus der Maus erkennt das Hormon als Antigen und bildet innerhalb von 3 Wochen die entsprechenden Antikörper.Die Antikörper reakieren spezifisch nur auf dieses Hormon und ihre Schablone für die Bildung ist in der Milz lokalisiert. Daher werden der Maus nach 3 Wochen Milzzellen entnommen und mit Myelomzellenfusioniert.Myelomzellen sind eine Form von Krebszellen, die eine ungebremstes Zellwachstum besitzen. So kann der genetische Code der Milzzellen beliebig oft repliziert werden.Zur Selektion ausschließlich hybridisierter Zellen wachsen sie auf einem Medium, das nur fusionierte Zellen überleben läßt.
Die Zellen werden entsprechend der gewünschten Antikörper selektiert und anschließend kloniert. Ist eine ausreichende Menge antikörperbildender Zellen vorhanden, kann der monoklonale Antikörper über diese Zellen gebildet und isoliert werden.
- - - _ ... ••
Myelomzellen /HGPRT'1
••• ••
Milzzellen
Fusion in Polyethyleng lykol
Myelomlinie in Zellkultur
:
.. ~ .
i" o.!
~
...
,1
/Ij ~\~
HAT-Medium ~l Selektionder Hybridzellen
1
Testauf Antikörper- - - ; ; . ) Einfrieren
/t~
Klonierunq
® @ C2
J \ . , 1 1.
..
{ ~ "..
.:~.: ::
AntikÖrper Kultur in
großemMaßstab
)
ZÜChtung
~
gewünSChte rKlone~ - - - - - ; >
Abb.3: Darstellung monoklonaler Antikörper (Quelle:Stryer 1988,S.932)
16 Chemie in der Schule: www.chids.de
... ,.,.. ..-:
Die Antigen-Antikörper-Reaktion wird auch enzym-linked immunoassay kurz ELISA genannt.
Für diese Reaktion wird der Antikörper zwischen der Auftragszone für den Urin und der Ablesezone des Testergebnisses auf einer festen Matrix im Schwangerschaftstester appliziert. Wird Urin in den Tester gegeben, so wandert er entlang der Matrix vom Auftrage- zum Ablesebereich. Der Antikörper kann nur in die mobile Phase übergehen, wenn eme Präzipitatbildung zwischen Antikörper und Gelbkörperehenhormon stattgefunden hat (vgl.
Abbildung 4). Ist kein Hormon im Urin enthalten, so verbleiben die Antikörper im ursprünglichen Auftragebereich.
In einem zweiten Schritt reagiert der Antigen-Antikörper-Komplex mit emem weiteren Antikörper, der im Ablesebereich installiert wurde und an ein Enzym gebunden ist. Durch die Bindung des Hormons findet eine Konformationsänderung des Enzyms statt, die eine Rotfärbung zur Folge hat.
Antikörper 1
~L·.~te·P9 f2 eftMt2;~:--~
1
Zugabe derProbeinteressierend es
~~tein
zu bes timmendes Protein
Abb. 4:cnzym-linkedimmunoassay (ELISA) (Quelle:Sirver 1988,S.65)
I ·
Ein positver Schwangerschaftstest wird durch Rotfärbung angezeigt, wogegen bei einem negativem Testergebnis keine Farbreaktion zu bemerkenist.
4.2. Urin als Waschmittel
Schmutz ist immer und überall. Als Straßenstaub ist er ein Gemenge von winzigen Gesteinsteilchen, Ruß, pflanzlichen Bestandteilchen und Fetten. Flecken sind in der Regel natürlicher Schmutz in konzentrierter Form. Unsere Kleidung wird allerdings auch von innen schmutzig. Durch Talg- oder Haardrüsen sondert die Haut außerdem ständig Hautfett ab.
Dieses Hautfett mit Sporen, Pilzen und Bakterien durchsetzt die Kleidung.
Zur Gesunderhaltung ist es unbedingt notwendig diesen Schmutz aus der Kleidung zu entfernen. Vor der Entdeckung der Seife (in Europa wurde sie durch Karl den Großen verbreitet) wurde vergorener Urin zum Waschen der Wäsche verwandt. Bereits von den Römern ist das Waschen mit Urin überliefert.
Da der Urin in großen Mengen gebraucht wurde, entwickelte sich in Rom ein besonderer Berufsstand, der sich mit dem Einsammeln von Urin und der Wäsche beschäftigte; die Fullons oder Fuller. Es wurden an allen Ecken der römischen Siedlungen irdene Töpfe aufgestellt, in die die Bürger urinierten. In dieser Flüssigkeit wurde dann die Wäsche, unter Treten und Stampfen mit den Füßen, vor der Stadt gewaschen. Anschließend wurde die Wäsche in am Bach gepült und durch Schwefeln gebleicht. Nichts erinnerte hinterher an die unappetitliche Prozedur.
Aus dieser Zeit hat sich auch ein Sprichwort gehalten, und zwar bekammen die Fuller für ihre unangenehme Arbeit sehr viel Geld, wodurch sie sehr reich wurden. Also bat der Kaiser Titus Vespasian (69-79) die vermögenden Fuller zur Kasse und belegten sie mit hohen Steuern. Als die Fuller sich beim Kaiser beschwerten und ihre übelriechende Arbeit beschrieben, bemerkte der Kaiser nur: "PeCU11ia 110nolet n_ Geld stinkt nicht (Thomas 1995, S.2lt).
4.2.1. Wasellen mitUrin (Quelle: Thomas 1993, S.26)
t\1aterialien:
Kristallisierschale verschmutzter Stoff
(Schmutz muß Fett enthalten')
Chemikalien:
10Tage alter Urin
Der verschmutzte Stoff wurde in dem vergorenem Urin (Abzug' stinkt ekelerregend) gewalgt • und gewaschen bis der Stoff gereinigt war. Anschießend wurde der Stoff mit klarem Wasser gut nachgespült und getrocknet.
Die Wirkung des Urins ist sehr simpel und entspricht fast der waschaktiver Subsstanzen. Beim Gärungsprozess wird der Harnstoff im Urin enzymatisch gespalten. Es entwickelt sich C02 und Ammoniak. Der Ammoniak verseift die Fette im Schmutz und es bilden sich die
..
Amoniumsalze der entsprechenden Fettsäuren.Diese sind bekanntlich waschaktive Substanzen, die den Reinigungsvorgang unterstützen.
/t
o
fttC-O-c-R
I 0
11
J-J
C-o-
c-I(I 0
J.lC-O-c-1(11
~
Fett Ammoniumhydroxid
H~C-O/l I J.IC-OII
I
~c -Oll
Glycerin
e
(i)o
/0 1J1I4~C
+ 3
1R.
Ammoniumsalze der Fettsäuren
Reaktion14: Bildung waschaktiverSubstanzen aus Amoniumhydroxid und denFellen des Körpertal gs
4.3. Historische Indigofärbung mit Urin
Der Ursprung der Blaufärberei mit Indigofera-Arten ist nach heutigem Wissensstand auf dem indischen Subkontinent zu suchen. In alten Ausgrabungsstätten lassen sich eindeutig entsprechende Einrichtungen aus dem 3.Jahrtausend finden.
Das Färben mit Indigo kann als das erste biotechnologische Verfahren bezeichnet werden. In ihm spielte der Urin eine herausrangende Rolle. Gefärbt wurde mit den farbstofthaltigen Pflanzenteilen des Färberwaids (isatis linktorea) und seines tropischen Bruders indigofera tinctorea.
Dazu wurden das zerstoßene Pflanzenmaterial angemaischt und unter Zusatz von Urin vergoren. Dieser Prozeß erfolgte in Kübeln, und die erhalten Brühe nannte man - den Wortstamm folgend - Küpe.Das gesponnene Gewebe wurde mit der Küpe getränkt und an der Luft getrocknet. Dabei färbte sich der Stoffallmählichblau und zwar in einer Lichtechtigkeit, der selbst die Tropensonne praktisch nichts anhaben konnte.
4.3.1. Färben von Wollstoff mit Indigo
(Quelle:Kreher;Hammerschmidt 1994, S.S3)
Materialien: . Kristallisierschale Wollstoff
Spatel
Chemikalien: Färberwaid CaC03 KC03 NaC03 Urin
Traubensaft Waschpulver
- '.,.
Zunächst wurde aus den Pflanzenstielen des Färberwaids und dem Urin eme Maische angesetzt, der Traubensaft und Kalk zugegeben wurde, um den,Gärungprozess in Gang zu setzen. Als basische Zusätze wurden noch NaC03 und KC03 zugegeben. Nach zwei Wochen war die Gärung so weit fortgeschritten,daß mit der Färbung begonnen werden konnte.
Gefärbt wurde mit Wolle, denn dieser Natustoff ist am besten in der Lagen, Naturfarbstoffe aufzunehmen. Die Wollfaser wurde unter Waschen von jeglichen Appreturen und Imprägnierungsmitteln befreit und in die auf 500C erhitzte Maische gegeben (Abzug).
Der eigendliche Färbevorgang in der Maische dauerte ca. 1/2 Stunde.Wärend dieser Zeit sollte der Farbstoff tief in das Gewebe eindringen. Anschließend wurde der gelblich-farbende Stoff an der Luft getrocknet, wobei er sich tiefblau färbte.
Ähnlich wie beim Waschen mit Urin, wird auch bei diesem Verfahren das Zersetzen des Harnstoffes wärend der Gärung für die Färbezwecke genutzt. Betrachtet man die Struktur des Indigofarbstoffes, so wird deutlich, daß er in der Pflanze zum einen in der reduzierten Form vorliegt und zum anderen an ein Zuckermolekül gebunden ist. Beim Gärunsprozess der Maische wird der Zucker abgepalten und das Indican geht so in das wasserlösliche Indoxyl über. Die Gärung fuhrt aber auch zum Freisetzen von Ammoniak durch das Zersetzen des Harnstoffes. Dieser Ammoniak als ein schwaches Reduktionsmittel verhindert ein Oxidieren des Indoxyls zu wasserunlöslichem Indigo in der Lösung. So kann der Farbstoff tief in das Gewebe eindringen. An der Luft verflüchtig sich das Reduktionsmittel und Indoxyl wird vom Luftsauerstoff zum blaufarbendem, wasserunlöslichenIndigo oxydiert (Seefelder 1994,S.15ft).
Indigo
• Indoxyl Indican (Indigofera tinctoria)
Jt<
:- - , c;-;.c-H
" ,Jt<
~
"'-.
/ .O=-< C 'J ·:>H OI-l
i OH
~! o~
1 0-/
o CH,OH -,
i
(X)-"
rl
lsatan 8 (Isatis tinctoria)
Reaktion 15:Fennentation und Oxidation desIndicanszu Indigo (Quellc:Secfelder 1994,S.I(»
..
I4.4. Aminoplasten
Nach den Krieg, als Rohstoff knapp wurden, war es üblich, Harnstoff, der für die Darstellung einiger Kunststoffe, zum Beispiel den Aminoplasten, nötig ist, aus Urin zu isolieren. In der heutigen Zeit wird der Harnstoff jedoch aus C02 und NH 3 unter Druck und bei hohen Temperaturen dargestellt. Trotzdem kann die Darstellung von Aminoplasten als em Anwendungsbeispiel für Urininhaltsstoffe angesehen werden.
Aminoplasten werden heute in der Industrie als Isolierungmaterial für Kabel eingesetzt.
4.4.1. Darstellung von Aminoplasten (Quelle:Hollernan;Schuler 1965, S.43)
Material:
Reagenzglas Handschuhe!
Spatel Wasserbad
Chemikalien: Formaldehyd Harnstoff
Harnstoffwurde in wenig Formaldehyd (so wenig wie möglich) gelöst und im Wasserbad auf 600C erhitzt (Abzugl). Nach einer Reaktionszeit von 10 Min hatte sich ein weißer Feststoff gebildet.
Bei dem Reaktionsmechanismus handelt es sich um eine einfache polymere Additionsreaktion. Der Stickstoff im Harnstoffmolekül greift mit seinem freien Elektronenpaar nucleophil am Kohlenstoffatom des Aldehyden an. Unter Umlagerung des Protons bildet sich ein Alkohol.
Mit einem weiteren Molekül Harnstoff findet eine Kondensationsreaktion statt, wobei ein Amidgebildet wird.
1_ .
"
o
Reaktion 16:Darstellungvon Aminoplasten
Dieser Vorgang wiederholt sichbeliebig, wobei das Polymer entsteht. Durch Quervernetzung kann dem Kunststoff eine größere Festigkeit gegeben werden.
5. Literatur r: I
... Beyer, H. (1976):Lehrbuch der organischen Chemie, Stuttgart.
Brewer, lM.; Pesce, Al; Ashworth, R.B. (1977): Experimentelle Methoden 10 der Biochemie, Stuttgart.
Cooper, T.G.(1981):Biochemische Arbeitsmethoden,Berlin.
Holleman,A.F.;Schuler, L. (1965):Einfache Versuche auf dem Gebietder organischen Chemie, Berlin.
Kilmartin, A (1982): Zystis-Urethritis, München.
Kreher, R.P.;Hammerschmidt, K.(1994):Indigo - Farbstoff der Antike und der Moderne.
Naturwissenschaften im Unterricht Chemie,24, S.53-57 . Rick, W.(1990):Klinische Chemie und Mikroskopie.Heidelberg.
Seefelder,M.(1994):Indigo:Kultur,Wissenschaft und Technik, Landsberg.
Stryer,L. (1990):Biochemie, Heidelberg.
Thomas,C. (1995):Ein ganz besonderer Saft-Urin, Köln.