AUS DEM LEHRSTUHL FÜR ANÄSTHESIOLOGIE PROF. DR. BERNHARD GRAF, MSC.
Volltext
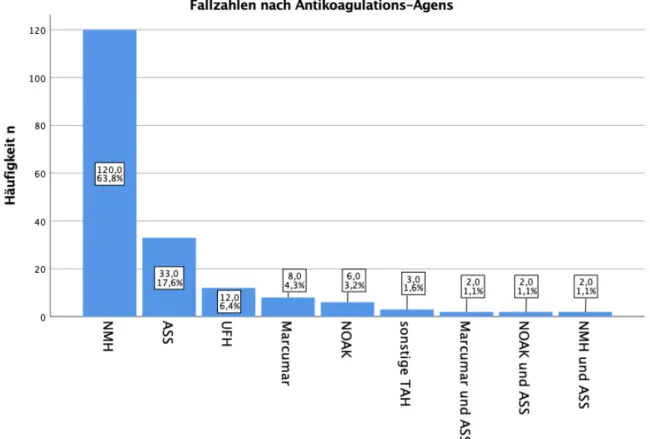
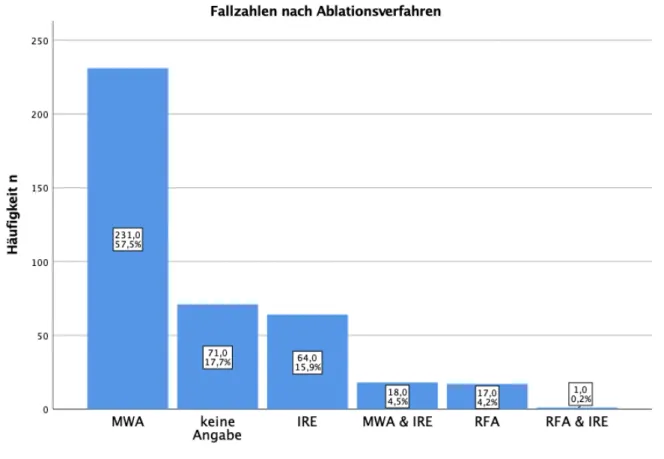
Abbildung
ÄHNLICHE DOKUMENTE
Bei Kindern ab 6 Jahren sollte für Dosierungen unter 250 mg, für Do- sierungen, die kein Vielfaches von 250 mg sind, oder wenn die Dosier- empfehlung nicht
Ähnlich wie bei den anderen drei Vertretern der NOAKs waren Patienten mit Vorhofflimmern reversibler Ursache, CrCl < 30 ml/min, hohem Blutungsrisiko, dualer
3.3 (4P) Wieviel von der Gebietsfläche-1 zur Verfügung gestellt werden, wenn man das dort, im Gebiet-1 anfallende Regenwasser nicht wie in 3.1 berechnet, in den Kanal
Jedem akuten Schlaganfall innerhalb des 4,5-Stunden Zeitfensters Bei progredienter oder wechselnder Symptomatik. auch außerhalb des Zeitfensters
Das sind gerade die beiden Grössen, von denen wir im vorhergehenden Kapitel gesagt haben, dass sie entscheidend sind, ob sich zwei Flüssigkeiten homogen
Auch in der Studie von Edwards M und Aldous I (1996) konnte ähnliches festgestellt werden: Nämlich, dass Medizinstudenten verglichen mit Studenten der Anglistik
Die Lösungen entfärben sich von violett über weinrot und gelbbraun nach farblos; gleich- zeitig wird eine Gasentwicklung beobachtet.. Die Entfärbung beginnt jedoch im zweiten
In dieser Behandlung ist eine Reinigung, ein Peeling, eine Gesichtsmassage sowie eine Maske enthalten.. 50 min