Physikalisch-Chemisches Fortgeschrittenen Praktikum
Iod-Fluoreszenz
Version: April 2017
PCF Iod-Fluoreszenz
2
1. Theorie
1.1.Molekülspektroskopie
Die Molekülspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung mit Molekülen. Trifft ein Photon einer geeigneten Frequenz ν auf ein Molekül im Grundzustand so besteht die Möglichkeit zur Absorption der Strahlung und eine damit einhergehende molekulare Zustandsänderung. Dieses Molekül, welches sich jetzt in einem angeregten Zustand befindet, kann nun durch Abgabe von Energie in den Grundzustand zurückkehren. Im Gegensatz zur Atomspektroskopie kommt es dabei nicht nur zu elektronischen, sondern auch zu Schwingungs- und Rotations- zustandsänderungen, wobei sich die Gesamtenergiedifferenz ΔE nach (1) zusammensetzt.
ΔE h ∙ ν h ∙ c ∙ ν ΔE ΔE ΔE (1) Größenordnungstechnisch gilt folgende Relation:
E ≫ E ≫ E (2)
Um sowohl die Grundlagen der Molekülspektroskopie als auch Interpretationen von aufgenommenen Spektren gut verstehen zu können, sind die Kenntnisse einfachster quantenmechanischer Modelle unabdingbar.
1.2.Spektroskopie zweiatomiger Moleküle – I2
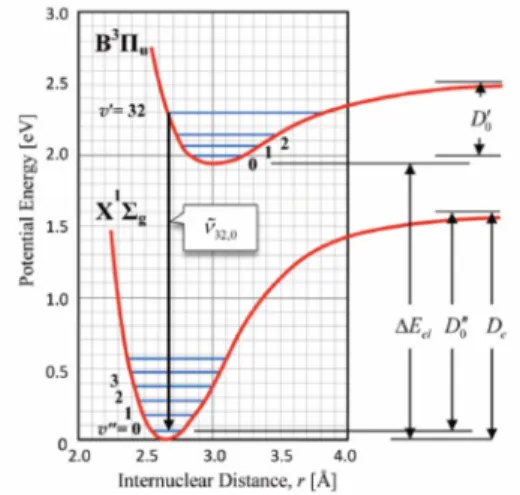
Naheliegender Weise sind zweiatomige Verbindungen die einfachsten Vertreter der Moleküle und damit sehr gut geeignet für das grundlegende Verständnis der Spektroskopie. Dabei hat sich gasförmiges Iod als interessantes und leicht beobachtbares System herausgestellt. Die Absorption bestimmter Wellenlängen im sichtbaren Bereich sorgen für einen Übergang der Iod Moleküle in einen angeregten Zustand (B3Πu) gefolgt von einer Fluoreszenzemission zurück in den Grundzustand (X1Σg). Da diese Relaxation in verschiedene Schwingungsniveaus v nach dem Franck-Condon Prinzip erfolgt, können charakteristische Informationen über den Grundzustand von I2 erhalten werden. Die beiden elektronischen Niveaus lassen sich quantenmechanisch mithilfe des anharmonischen Oszillators beschreiben (Abbildung 1).
Abbildung 1: Potentialkurven von I2 der beiden betrachteten Zustände.
PCF Iod-Fluoreszenz
3 Mathematisch lässt sich die potentielle Energie V des anharmonischen Oszillators in Abhängigkeit des Kernbindungsabstands r näherungsweise aus der Lösung der Schrödinger-Gleichung nach (3) beschreiben.
V r D 1 − e !" (3) DE ist die Dissoziationsenergie des Iod Moleküls bezogen auf das Minimum der Potentialkurve. Die Konstante α ist abhängig von der Kraftkonstante k der Iod-Iod- Bindung (4).
α $"&%' (4)
Die erlaubten Energieniveaus sind gegeben durch (5), welche die Schwingungsfrequenz ν0, die Schwingungsquantenzahl v und die Anharmonizitätskonstante xe von I2 enthält.
E hν()v +", − x hν()v +"," (5)
Durch Bildung der Energiedifferenz zweier benachbarter Schwingungsniveaus wird Gleichung (6) erhalten, welche durch Kombination mit (1) zu (7) vereinfacht werden kann.
ΔE E .+− E −2x hν( v 1 hν( (6) Δν −2x ν( v 1 ν( (7) Durch Birge-Sponer-Auftragung der Energiedifferenzen Δν gegen (v+1) wird eine Gerade erhalten aus welcher Grundlegende Informationen des elektronischen Grundzustands von Iod berechnet werden können.
2. Versuch
2.1.Zielsetzung
Ziel dieses Versuchs ist die Aufnahme der Fluoreszenzemission molekularen Iods mithilfe unterschiedlicher Strahlungsquellen. Der Aufbau des Experiments soll dabei selbst entwickelt und praktisch umgesetzt werden.
Eingangskolloquium
Bereiten Sie sich bitte eigenständig auf folgende Themengebiete vor:
• Optische Übergänge zweiatomiger Moleküle
• Birge-Sponer-Auftragung
• Fluoreszenzspektroskopie
• Grundlagen der Optik
• LEDs und Laser
PCF Iod-Fluoreszenz
4 2.2.Versuchsdurchführung
Erstellen Sie zunächst gemeinsam mit dem Betreuer einen Plan zum schematischen Aufbau des Versuchs. Zur Umsetzung des experimentalen Aufbaus stehen Ihnen dabei eine Reihe optischer Bauteile (z.B. Linsen, Spiegel und Filter) zur Verfügung. Als Strahlungsquelle dienen sowohl eine LED (565 nm) als auch ein Laser (532 nm).
• Bauen Sie das Experiment mit beiden Strahlungsquellen je einmal auf
• Nehmen Sie nach Möglichkeit ein Fluoreszenzemissionsspektrum des Iods auf
• Nehmen Sie die Emissionsspektren der Strahlungsquellen auf und bestimmen Sie deren Leistung
2.3.Auswertung
• Skizzieren und erklären Sie Ihre beiden experimentellen Aufbauten (in die Durchführung!).
• Vergleichen Sie die beiden Strahlungsquellen hinsichtlich ihrer Eigenschaften und der Verwendung für dieses Experiment.
• Auswertung der Iod-Fluoreszenzemission:
Bilden Sie Ihre erhaltenen Iod Emissionsspektrum ab
Ordnen Sie den beobachteten Banden (bis 700 nm!) jeweils einem optischen Übergang zu (ν32→0 entspricht einer Wellenlänge von 532 nm) Berechnen Sie die Energiedifferenzen aller unmittelbar benachbarter Schwingungsniveaus in [cm-1]
Erstellen Sie eine Birge-Sponer Auftragung nach (7) Bestimmen Sie ν0 und xe
Bestimmen Sie die Dissoziationsenergien D(00 und DE des elektronischen Grundzustands in [eV]
Literatur
• T. Engel und P. Reid, Physikalische Chemie, Pearson Sudium, 2006, 1. Auflage.
• P. W. Atkins und J. de Paula, Physikalische Chemie, Wiley-VCH, 2013, 5. Auflage.
• S. B. Bayram und M. V. Freamat, Am. J. Phys., arXiv:1507.02600, 2015.