Glas
Herstellung und Analytik
AC-Experimentalvortrag von Sarah Magull am 06.06.2018
In Zusammenarbeit mit dem Institut für Glas- und Rohstoffforschung in Göttingen
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas
Was ist Glas?
Definition nach DIN 1259:
„Glas ist ein anorganisches Schmelzprodukt, das im Wesentlichen ohne Kristallisation erstarrt.“ [1]
Gustav Tammann (1861-1938):
„Der Glaszustand ist der eingefrorene Zustand einer unterkühlten Flüssigkeit, die ohne zu kristallisieren erstarrt ist.“ [1]
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 2
Rohstoffe und ihre Funktion [2]
3
Rohstoff Wirksamer Bestandteil im Glas
Funktion
Quarz, SiO
2SiO
2Netzwerkbildner
Borsäure, H
3BO
3B
2O
3Salze der Phosphorsäure,
z.B. CaHPO
4*2 H
2O
P
2O
5Soda, Na
2CO
3Na
2O Netzwerkwandler
Kalk, CaCO
3CaO
Pottasche, K
2CO
3K
2O
Mennige, Pb
3O
4PbO Netzwerkbildner und
Netzwerkwandler
Zinkoxid, ZnO ZnO
Kalifeldspat, KAlSi
3O
8Al
2O
3Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas
Rohstoff- mischung
=
Gemenge
Tab. 1: Wichtige Glasrohstoffe und ihre Funktion
Glasstrukturen – nach Zachariasen und Warren [3]
Quarzglas Alkali-Silikat-Glas
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 4
Abb. 1:
a) Geordnete [SiO
4]-Tetraeder in kristalliner Kieselsäure
b) Ungeordnete Vernetzung von [SiO
4]- Bausteinen in Quarzglas
Abb. 2:
Mögliche Anordnung
in einem Natrium-Silikat-Glas
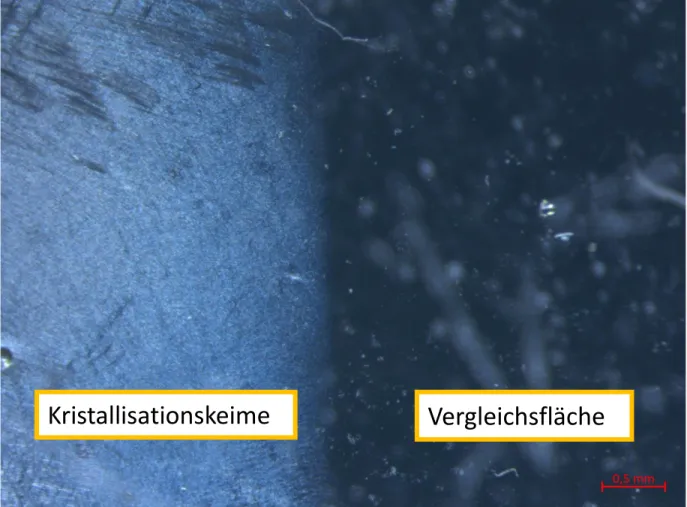
DV1: Entglasen
5
Erklärung:
[4]• Kristallisation durch längerfristiges Temperieren
Bildung von Kristallisationskeimen Kristallwachstum über Jahre
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas
Der kristalline Zustand ist energetisch günstiger!
Abb. 3: Entglastes Glas unter dem Mikroskop mit 15-facher Vergrößerung
Kristallisationskeime Vergleichsfläche
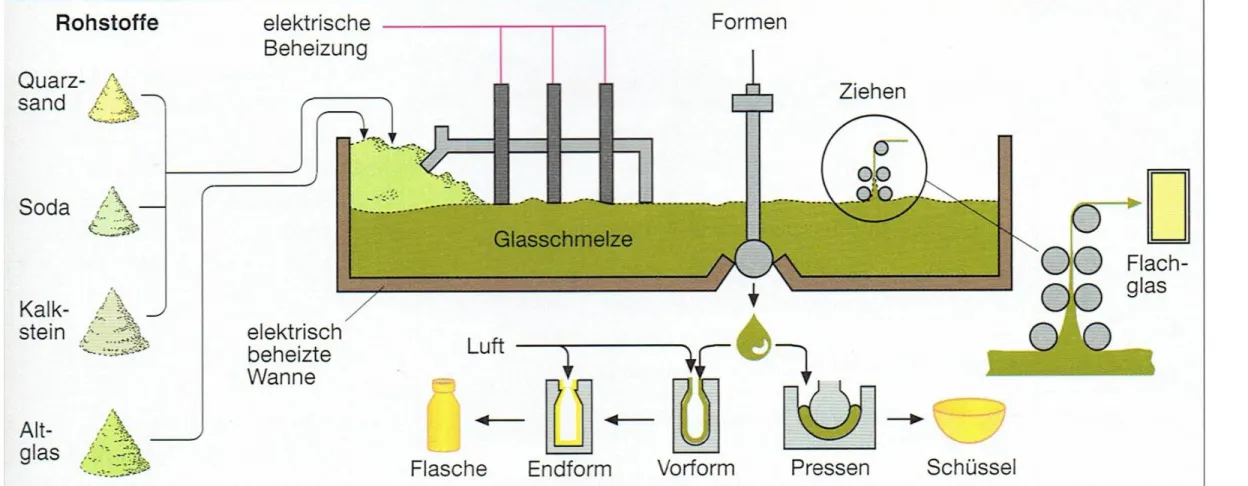
Industrielle Glasproduktion [5]
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 6
Abb. 4: Industrielle Glasproduktion, Schulbuch-Darstellung
Glasherstellung in der Schule
a) DV2: niedrigschmelzendes Glas im Simon-Müller-Ofen herstellen
Durchführung:
[6]1. 2. 3.
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 7 min.
800 °C
Gemenge
einfüllen Mit Deckel
30 min
> 10 min
abkühlen lassen!
Simon-Müller-Ofen vorgewärmter
Tiegel
Graphittiegel auf Ceranplatte
Abb. 5: Herstellung von niedrigschmelzendem Glas im Simon-Müller-Ofen
Glasherstellung in der Schule
a) DV2: niedrigschmelzendes Glas im Simon-Müller-Ofen herstellen
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 8
Vorteile Nachteile
Rohstoffe aus Glasindustrie Borsäure als
Hauptbestandteil statt Quarzsand
resistentes Glas Tiegelreinigung Produktionsschritte
erkennbar
langwierig,
unschöne Qualität
Abb. 6: niedrigschmelzendes Glas im Tiegel
Tab. 2: Beurteilung von DV2
Glasherstellung in der Schule
Durchführung:
[7]1. 2. 3.
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 9
b) V1: Natriumpolyphosphatglas
Tiegel halb gefüllt mit Natriumpolyphosphat
> 10 min warten!
Graphittiegel auf Ceranplatte
Abb. 7: Herstellung von Natriumpolyphosphatglas
Glasherstellung in der Schule
Auswertung:
[7]• Glasbildung durch:
1. Polyphosphat als Netzwerkbildner 2. Natriumoxid als Netzwerkwandler
3. Schmelzpunkt von Natriumpolyphosphat: 628 °C
• Hohe Kühlspannung! Splittergefahr!
• Glas ist wasserlöslich!
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 10
b) V1: Natriumpolyphosphatglas
Abb. 8:
Natriumpolyphosphatglas
Glasstruktur – Natriumpolyphosphatglas
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 11
3D-Netzstruktur
10 % [8]
lineare Polyphosphate
90 % [8]
cyclische +
Oligophosphate
∆
Glasfärbung
a) DV3: mit Metalloxiden [9]
• meist Nebengruppenelementsalze
• im Glas ähnliche Farbe wie in wässriger Lösung
• je nach Konzentration unterschiedlich intensive Farbe
Was ist Glas? / Glasherstellung / Glasfärbung/ Analyse verschiedener Glassorten / Spezialglas 12
Abb. 9: Kupferglas
hohe Kupferkonzentration niedrige Kupferkonzentration Abb. 10: Kobaltglas
Abb. 11: Mangan(II)glas
Abb. 12: Nickelglas
Glasfärbung
b) V2: mit Glastinten [10]
Durchführung:
1. 2. 3.
Was ist Glas? / Glasherstellung / Glasfärbung/ Analyse verschiedener Glassorten / Spezialglas 13
Aktivkohle
Wasserglaslösung Vermischen!
gereinigte Glasplatte
Abb. 13: Herstellung von Glastinte
Glasfärbung
b) V2: mit Glastinten
Auswertung:
+4 -2 +1 -2 +1 +1 +4 -2 +1 -2
[Si
2O
7]
6-(aq)+ 8 Na
+(aq)+ 2 OH
-(aq)2 Na
4SiO
4(s)+ H
2O farbloser Feststoff
• Aktivkohle wird in der Wasserglaslösung eingeschlossen
• Entfernbar durch heißes Wasser oder abschleifen
• ACHTUNG: Kontakt mit Haut, Kleidung oder Oberflächen vermeiden!
Was ist Glas? / Glasherstellung / Glasfärbung/ Analyse verschiedener Glassorten / Spezialglas 14
Abb. 14: Glasstück mit schwarzer Tinte
Glasfärbung
c) als Anlauffärbung: [11]
• Verwendung von Edelmetallsalzen
• Reduktion beim Schmelzvorgang
• Nachträgliches erwärmen kolloidal gelöste Nanokristalle
Was ist Glas? / Glasherstellung / Glasfärbung/ Analyse verschiedener Glassorten / Spezialglas 15
Analytik - Farbspektren
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 16
Abb. 15: Spektrometer Abb. 16: Innenkammer
Analytik - Farbspektren
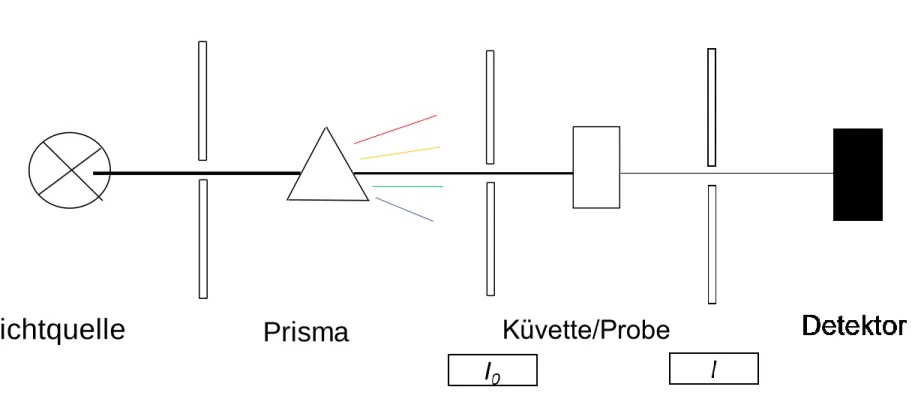
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 17
Lichtquelle
Abb. 17: Aufbau eines Spektrometers
Prisma Küvette/Probe
Analytik – Farbspektren: Berechnung
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 18
Lambert-Beersches-Gesetz:
Transmission in %[13]: 𝑇 = 𝐼 𝐼
0Absorption in %
[12]: 𝐴 = 𝜀 ∗ 𝑑 ∗ 𝑐 Zusammenhang
[13]: 𝐴 = 1 − 𝑇
I: Intensität der Strahlung nach der Probe I
0: Anfangsintensität der Strahlung
T: Transmission bei einer Wellenlänge
A: Absorption bei einer Wellenlänge 𝜀: spezifische Stoffkonstante
d: Schichtdicke
c: Konzentration der absorbierende Substanz
Analytik – DV4: Farbspektren
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 19
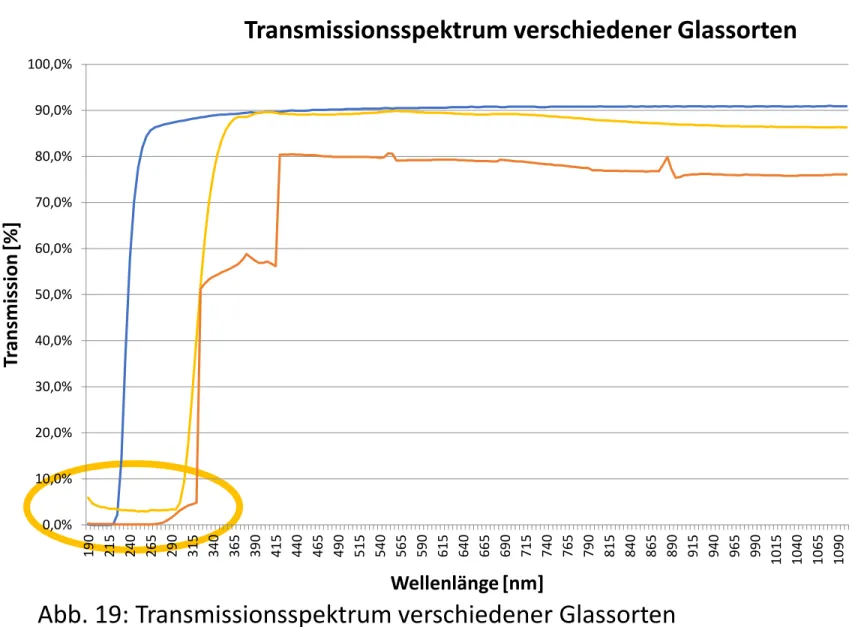
Abb. 19: Transmissionsspektrum verschiedener Glassorten
0,0%
10,0%
20,0%
30,0%
40,0%
50,0%
60,0%
70,0%
80,0%
90,0%
100,0%
190 215 240 265 290 315 340 365 390 415 440 465 490 515 540 565 590 615 640 665 690 715 740 765 790 815 840 865 890 915 940 965 990 1015 1040 1065 1090
Transmission[%]
Wellenlänge [nm]
Transmissionsspektrum verschiedener Glassorten
Quarzglas
Kalk-Natron-Glas Boro-Silikat-Glas
Analytik – DV4: Farbspektren
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 20
Abb. 20: Transmissionsspektrum von Natriumpolyphosphat-Buntglas Abb. 21: Buntglas
0,0%
10,0%
20,0%
30,0%
40,0%
50,0%
60,0%
70,0%
80,0%
90,0%
100,0%
190 215 240 265 290 315 340 365 390 415 440 465 490 515 540 565 590 615 640 665 690 715 740 765 790 815 840 865 890 915 940 965 990 1015 1040 1065 1090
Transmission[%]
Wellenlänge [nm]
Transmissionsspektrum Buntglas
Nickelglas Kupferglas Weißglas Kobaltglas
Kupferglas hohe Cu(II)-Konz.
Analytik – DV4: Farbspektren
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 21
Abb. 23: Strukturformel von Dimethylphthalat
O O
O O
CH3
CH3
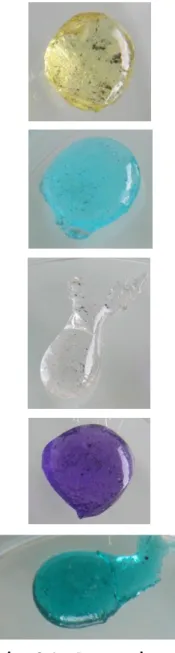
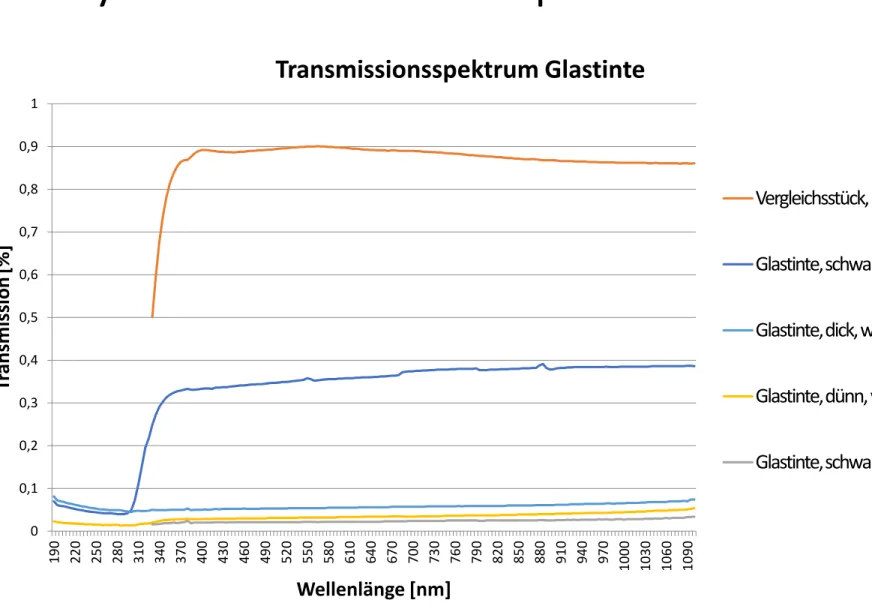
Abb. 22: Transmissionsspektrum von Glastinte auf Kalk-Natron-Glas
Abb. 24: Glasstücke mit Tinte
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1
190 220 250 280 310 340 370 400 430 460 490 520 550 580 610 640 670 700 730 760 790 820 850 880 910 940 970 1000 1030 1060 1090
Transmission[%]
Wellenlänge [nm]
Transmissionsspektrum Glastinte
Vergleichsstück, DMP
Glastinte, schwarz,Luft
Glastinte, dick, weiß, Luft
Glastinte, dünn, weiß, Luft
Glastinte, schwarz, DMP
Analytik - Dichtebestimmung:
a) DV5: Sinkmethode
Küvette mit:
Tetrabromethan und
Bromnaphthalin
nicht schultauglich!
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 22 BrBr
Br H H
Br Br
Abb. 25: Dichteanlage für Sinkmethode
Analytik - Dichtebestimmung
b) V3: Pyknometer-Methode
Dichtebestimmung von Flüssigkeiten
• Durchführung:
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 23
mit Wasser gefüllt
1. Volumenbestimmung:
Leergewicht: m
leer= 57,827 g Masse mit Wasser: m
mW= 157,179 g Messtemperatur: T
VMess= 20 °C
Abb. 26: Pyknometer
Analytik - Dichtebestimmung
b) V3: Pyknometer-Methode
• Durchführung:
2. Bestimmung der Glasdichte
Masse Glasgrieß: m
GlasMasse mit Glasgrieß und Wasser: m
GesamtMesstemperatur: T
GMessWas ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 24
mit Wasser und Glasgrieß gefüllt
Abb. 26: Pyknometer
Analytik - Dichtebestimmung
b) V3: Pyknometer-Methode
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 25
Tab. 3: Dichte 𝜌
W(T) von Wasser in Abhängigkeit zur
Temperatur
[14]T in °C ρ in g/cm
318 0,999
19 0,998
20 0,998
21 0,998
22 0,998
23 0,998
24 0,997
1. Volumenbestimmung:
Leergewicht: m
leer= 57,827 g Masse mit Wasser: m
mW= 157,179 g Messtemperatur: T
VMess= 20 °C
2. Bestimmung der Glasdichte
Masse Glasgrieß: m
GlasGesamtmasse: m
GesamtMesstemperatur: T
GMessAuswertung über: 𝑉 = 𝑚
𝜌
Analytik - Dichtebestimmung
Auswertung:
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 26
Glassorte Dichte mit Sinkmethode Dichte mit Pyknometer- Methode
Boro-Silikat-Glas 2,230 g/cm
32,230 g/cm
3Kalk-Natron-Glas 2,501 g/cm
32,500 g/cm
3Tab. 4: Vergleich der Methoden zur Dichtebestimmung
Analytik – V4: Bestimmung des Protolysegrads
Durchführung:
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 27
1. 2. 3. 4.
1. Blindprobe
2. Kalk-Natron-Glas 3. Boro-Silikat-Glas 4. Wasserglaslösung
Abb. 27: Aufbau zur Bestimmung des Protolysegrads
Analytik – V4: Bestimmung des Protolysegrads
Durchführung:
[15]1. 2.
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 28 1. 2. 3. 4.
entmineralisiertes
1. 2. 3. 4.Wasser 6 Tropfen
Universalindikator
Abb. 28: Durchführung der Bestimmung des Protolysegrads
Analytik – V4: Bestimmung des Protolysegrads
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 29
Beobachtung:
• Alkaliionen-haltige Gläser reagieren alkalisch
Abb. 30: Bestimmung des Protolysegrads
Abb. 29: Skala des Universalindikators
[20]Analytik – V4: Bestimmung des Protolysegrads
Auswertung:
Beispiel Wasserglas
+1 +4 -2 +1 -2 +1 +1 +1 +4 -2 -2 +1
Schulbuch
[15]: Na
4SiO
4(s)+ H
2O Na
+(aq)+ Na
3HSiO
4(aq)+ OH
-(aq)+1 +4 -2 +1 -2 +4 -2 +1 -2 +1
Universität
[11]: 2 Na
4SiO
4(s)+ H
2O [Si
2O
7]
6-(aq)+ 8 Na
+(aq)+ 2 OH
-(aq)Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 30
Ausblick - Spezialglas
• DV6: Milchglas [16]
• Trübungsmittel: Calciumphosphat (Ca 3 (PO 4 ) 2 )
• Ursache: Bildung von unlöslichem Calciummetaphosphat (Ca(PO 3 ) 2 ) scheidet sich in Tröpfchen ab
verändert Lichtbrechung
• funktioniert nicht in Phosphatgläsern
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 31
Abb. 30: Produkt des Versuches
Ausblick - Spezialglas
• DV7: phototropes / solarisierbares Glas [17]
enthält Silberhalogenide selbsttönendes Glas
+1 -1 +1 -1 0 +2 -1
AgCl (solv) + CuCl (solv) Ag (s) + CuCl 2(solv)
Was ist Glas? / Glasherstellung / Glasfärbung / Analyse verschiedener Glassorten / Spezialglas 32
Abb. 31: Schmelze des phototropen Glases
Abb. 32: selbstgemachtes phototropes Glas
Schulrelevanz [18], [19]
33
Versuch Inhaltsfelder im Kerncurriculum
Glasherstellung: DV2, V1 „Der Mix macht‘s“ – Eigenschaften von Stoffgemischen (Sek. 1)
„Schatzkiste der Natur – Chemie in Alltag und Technik“ – Umgang mit Ressourcen (Sek. 1)
Glasfärbung: DV3, V2 Farbstoffe / Farbigkeit (Q4) Farbspektren: DV4 Spektroskopie (Q4)
Dichtebestimmung: DV5, V3 „Welt der Stoffe“ – Nachweis von Stoffeigenschaften (Sek. 1) Protolysegrad: V4 Protolysereaktionen (E)
solarisierbares Glas: DV7 Redoxreaktionen (E)
Tab. 5: Schulrelevanz des Themengebietes Glas
Gefahren in der Schule
• Schnittgefahr an Scherben
• Heißes Glas sieht aus wie kaltes Glas!
• Lackieren von Natriumpolyphosphatglas Konservierung
Einschließung der Schwermetallionen in Farbglas
• besondere Vorsicht beim Umgang mit Wasserglaslösung
34
Abb. 33: Erste-Hilfe-Kasten des
AC-Praktikums
Quellenverzeichnis
[1] URL: https://www.baunetzwissen.de/glas/fachwissen/materialeigenschaften/definition-von-glas-159077, abgerufen am 15.05.2018.
[2] Lange, 1980: Rohstoffe der Glasindustrie. 1. Auflage. Leipzig. S. 14 –16.
[3] Vogel W., 1992: Gals Chemie. 3. Auflage. Berlin Heidelberg. S. 51.
[4] Fröhler, A, 2005: Lexikon für Glas und Glasprodukte. Schorndorf. S. 363.
[5] Frühauf, D.; Tegen, H., 2007: Blickpunkt Chemie. Neubearbeitung. Braunschweig. S. 227.
[6] Lüthje, Gall, Reuber, 1975: Lehrbuch der Chemie, Sekundarstufe 1. 1. Auflage. Diesterweg Salle. S. 15.
[7] Wurm, D.; Woest, V., 2003: Einfache Experimente zum Thema Glas.CHEMKON/10.Jahrg./Nr. 3. Weinheim. S. 131 –134.
[8] Hollemann/Wiberg, 2007: Lehrbuch der anorganischen Chemie. 102.Auflage. Berlin. S. 782 –783.
[9] Vogel W., 1992: Gals Chemie. 3. Auflage. Berlin Heidelberg. S. 255 –304.
[10] Raat, H, 1990:Chemie des Alltags. Ein Lexikon der praktischen Chemie. 27. verbesserte Auflage. Freiburg im Breisgau. S. 243.
[11] Neumüller, B., 2016: Seminar zum AC1-Praktikum für Lehramtsstudierende. Eigene Mitschrift. Marburg. Erste Woche.
[12] Lange, 1980: Rohstoffe der Glasindustrie. 1. Auflage. Leipzig. S. 8.
[13] Atkins, P.; de Paula, J., 2013: Physikalische Chemie. 5. Auflage. Weinheim. S.514 –515.
[14] URL: https://www.internetchemie.info/chemie-lexikon/daten/w/wasser-dichtetabelle.php, abgerufen am 02.06.2018.
[15] Keune, H.; Boeck, H., 1998: Chemische Schulexperimente. 1. Auflage. Berlin. S. 112.
[16] Vogel W., 1992: Gals Chemie. 3. Auflage. Berlin Heidelberg. S. 304 –310.
[17] Vogel W., 1992: Gals Chemie. 3. Auflage. Berlin Heidelberg. S. 437 –444.
[18] Hessisches Kultusministerium, 2016: Bildungsstandards und Inhaltsfelder. Das neue Kerncurriculum für Hessen. Sekundarstufe I –Gymnasium. Chemie.Wiesbaden. S. 22 –27.
[19] Hessisches Kultusministerium, 2016: Kerncurriculum gymnasiale Oberstufe. Chemie.Wiesbaden. S. 25 –42.
[20] Rickelt, E.: AC-Praktikum.
35
Vielen Dank für Ihre Aufmerksamkeit!
Haben Sie noch Fragen oder Anmerkungen?
36