des Chemielehramtsstudiums an der Uni Marburg referiert. Zur besseren
Durchsuchbarkeit wurde zudem eine Texterkennung durchgeführt und hinter das eingescannte Bild gelegt, so dass Copy & Paste möglich ist – aber Vorsicht, die Texterkennung wurde nicht korrigiert und ist gerade bei schlecht leserlichen Dateien mit Fehlern behaftet.
Alle mehr als 700 Protokolle (Anfang 2007) können auf der Seite
http://www.chids.de/veranstaltungen/uebungen_experimentalvortrag.html eingesehen und heruntergeladen werden.
Zudem stehen auf der Seite www.chids.de weitere Versuche, Lernzirkel und Staatsexamensarbeiten bereit.
Dr. Ph. Reiß, im Juli 2007
Philipps-Universität Marburg Fachbereich Chemie
Übungen im Experimentalvortrag
Sommersemester 1998
Protokoll zum Experi mentalvortrag
"Alles Apfel"
vom23. April 1998
vorgelegt von
Wilfried Budde Wehrdaer Weg 9
35037 Marburg
---
/
1. Einleitung: Warum gerade Äpfel?
1.2 Der Apfel aus botanischer Sicht
2. Die Inhaltsstoffe von Äpfeln 3. Der Reifungsprozeß
3.1 Beurteilung von Geschmack und Aussehen 3.2 Veränderungen der Frucht während der Reifung
• VERSUCH 1: Atmung von Äpfeln
• VERSUCH 2: Nachweis von Chlorophyll in der Schale
• VERSUCH 3: Bestimmung des Fruchtsäuregehalts
1 2
4
5 5
6
3.3 Auslösung der Reifung durch Ethen 16
4. Alles Apfel: Überblick über die Produkte 17
5. Die enzymatische Bräunung 19
• VERSUCH 4: L-Ascorbinsäure als Antioxidationsmittel
6. Pektin: Struktur, Vorkommen, Verwendung 23
7. Pektin-spaltende Enzyme 26
• VERSUCH 5a: Saftausbeute aus Apfelmaische
• VERSUCH Sb: Klären von Apfelsaft
8. Eigenschaften von Pektin: Geliermechanismen 33
• VERSUCH 6a: Gelierverhalten niedrigveresterter Pektine
• VERSUCH 6b: Gelierverhalten hochveresterter Pektine
9. Mikrobielle uefährdung von Früchten und Fruchtprodukten 41
• DEMO: Einfluß der Wasseraktivität auf Mikroorganismen
10. Literaturverzeichnis 46 .
1.1 Warum gerade "Apfel" ?
. "
"-.',
~.,~
, ,
( r -, .
I · •
Die Herkunft des Apfels ist noch ungeklärt. Als sicher gilt, daß die Syrer bereits vor 5000 Jahren Äpfel aus Kleinasien nach Ägypten gebracht haben.
Bei den Pharaonen wurde der Apfelbau sehr gefördert. In unseren Breiten waren schon sehr früh mehrere Wildsorten (z.8.
Paradies- und Holzapfel) bekannt, wie Ausgrabungen der 3000 Jahre alten Pfahlbauten am Bodensee bestätigen.
Als Symbol der Liebe und der Schönheit. des Glücks und der Macht erlangte der Apfel mystische, literarische und historisch-symbolische Bedeutung. So war der Reichsapfel der deutschen Kaiser als Symbol für die Welt ein Teil ihrer Reichsinsignien und damit Ausdruck ihrer Macht. In der christlichen Symbolik ist der Apfel Sinnbil·d der Sünde. Der biblischen Überlieferung nach ist der Baum der Erkenntnis ein Apfelbaum. Bei allen germanischen Völkern spielt der Apfel als Fruchtbarkeitssymbol bei Hochzeitsbräuchen eine Rolle. Für die Griechen war der Apfel ein Geschenk des Weingottes Dyonisos. Sie und die Römer verwandten viel Zeit und Mühe auf die Verbesserung und Neuzüchtung von Apfelsorten. Sie waren es auch, die schon damals aus Äpfeln Wein und Säfte kelterten.
Durch Züchtung und Anpassung an die verschiedenen Boden- und Kltmavernättntsse ist der Apfelbaum Malus domestica der wohl am meisten verbreitete Obstbaum überhaupt. Seine Früchte dürften die beliebtesten sein, nicht nur wegen ihrer Form. Farbe und dem Geschmack, sondern vor allem wegen der vielseitigen Verwendbarkeit und dem Gesundheitswert. Die Sortenvielfalt ist beträchtlich. Heute kennt man weltweit rund 20.000 verschiedene Apfelsorten von denen jedoch nur einige Sorten im großen Stiel
vermarktet werden. Der Verbrauch je Kopf an Äpfeln in Deutschland beträgt rund 30 kg pro Jahr; das ist etwa ein Drittel, gemessen am Gesamtverbrauch an Frischobst. Neben den genannten Vorteilen zeichnen sich Äpfel durch eine lange Lagerfähigkeit aus, so daß sich im Gegensatz zu anderen Früchten die Verarbeitung über geraume Zeit hinziehen kann.
In diesem Vortrag möchte ich weniger die Inhaltsstoffe von Obst und dessen Bedeutung für die menschliche Ernährung herausstellen, sondern vielmehr am Beispiel des Apfels einige Möglichkeiten der Obstverarbeitung aufzuzeigen.
Ausgehend vom Reifungsprozeß und den damit verbundenen Veränderungen
,~
in der Frucht, wird anschließend das Phänomen der enzymatischen Bräunung erläutert. In den folgenden Kapitel geht es um das Heteropolysaccharid Pektin, das bei der Verarbeitung von Äpfel eine ganz entscheidende Rolle spielt. Der letzte Teil setzt sich mit der mikrobiologischen Gefährdung der Produkte auseinander.
1.2 Der Apfel aus botanischer Sicht
Ein Apfe/- Lied
In meinem kleinen Apfel, da siehtes lustig aus:
es sind darin fünf StObchen grad wie in einem Haus.
In jedem StObchen wohnen zwei Kemchen schwarz und fein, die liegen drin und
trsumen
vom lieben Sonneschein.Sie trsumen auch noch weiter gar einen ecronen Traum, wie sie einst werden hangen am schonen Weihnachtsbaum.
Der paradiesische Apfel am Baum der Erkenntnis ist botanisch gesehen gar nicht so paradiesisch. Denn bei der Apfelfrucht wird nur das für den Genuß wertlose Kerngehäuse aus den Fruchtblättern gebildet und ist demzufolge gemäß der botanischen Definition die ~,eigentliche" Frucht. Dagegen" geht der genießbare Teil der Apfelrrucnt, das mächtig entwickene "Fruchtfleisch", aus der Blütenachse hervor und ist aus diesem Grund streng genommen keine Frucht.
Abb. 1: Aufbau der Apfelfrucht (Sammelbalgfrucht)
/ /
~. ~p'
c97g~ .
.
I\ / \
\~' ~
II /\ \ "-=...-/ / /
\. /~"'l"'/
.. \ t
sa '''" ..A
~/~~---
rI ..
I' -s: I
f
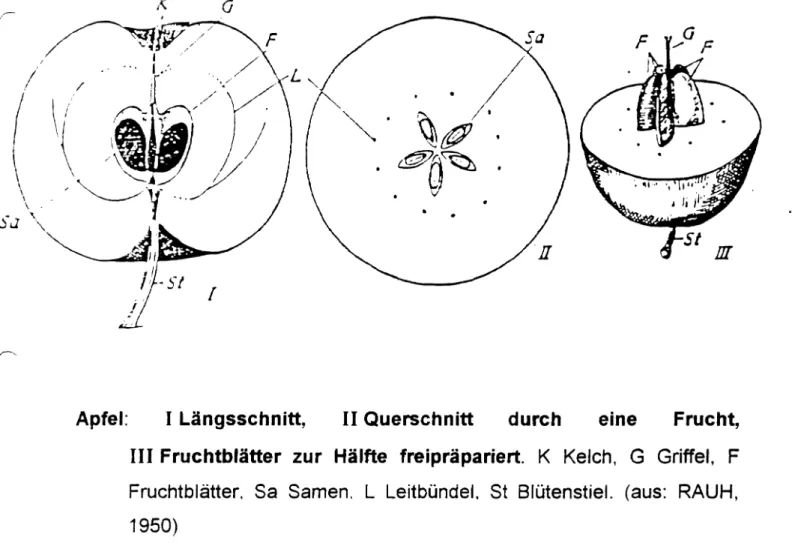
Apfel: I Längsschnitt, 11 Querschnitt durch eine Frucht, III Fruchtblätter zur Hälfte freipräpariert. K Kelch, G Griffel, F Fruchtblätter, Sa Samen~ L Leitbündel. St Blütenstiel. (aus: RAUH, 1950)
2. Die Inhaltsstoffe von Äpfeln
Wie die meisten anderen Obstsorten liefern auch Äpfel Kohlenhydrate, Vitamine und Mineralstoffe in für den Menschen emährungsphysiologisch bedeutsamen Mengen. Der Hauptnährstoff sind die Kohlenhydrate, die in erster Linie der Energieversorgung dienen. Neben den Monosacchariden Glucose und Fructose finden sich Disaccharide (Saccharose) und verschiedene Polysaccharide, vor allem Stärke, Cellulose und Pektine.
Cellulose und Pektine sind unverdaulich und liefern dem Körper keine Energie, sie gehören zu den Ballaststoffen.
Tab. 1: Nährstoffgehalt und Brennwert von Apfel u. Banane im Vergleich
Inhaltsstoffe in 100 9 Apfel, Apfel, Banane, (verzehrbarer Anteil) frisch getrocknet frisch
Brennwert [kJ] 229 1110 337
Wasser [9] 85,3 27,0 74
Kohlenhydrate [g] 12,4 61,1 18,8
Eiweiß [g] 0,34 1,37 1,15
Fett [g] 0,4 1,63 0.18
Kalium [mg] 144 622 393
Magnesium [mg] 6,4 * 36
Eisen [mg] 0,48 1,2 0,55
Calcium [mg] 7,1 30 8,7
Vit. E [mg] 0,5 * 0,27
Vit. 81 (Thiamin) [~g] 35 100 44
Vit. B2 (Riboflavin) [~g] 32 100 57
Vit. 86(Pyridoxin) [tJg] 45 * 370
Niacin [mg] 0,3 0,8 0,65
Vit. C [mg] 12 12 12
Fruchtsäure [g] 0,65 * *
Ballaststoffe [g] 2,3 11,5 2,0
* = Es liegen keine Daten vor.
Vitamine sind essentielle Nahrungsbestandteile, die der Körper nicht selbst aufbauen kann. Vitamin C ist das Obst- und auch Gemüse-Vitamin schlechthin.
Der Vitamin C-Bedarf eines erwachsenen Menschen liegt bei etwa 75 mg
Vitamin C pro Tag. Zum Vitamingehalt des Apfels tragen neben dem Vitamin C auch die Vitamine der B-Gruppe, Vitamin E sowie Carotin (Vorstufe von Vitamin A) bei.
Mineralstoffe haben im Körper eine Vielzahl von Funktionen. Kalium und Natrium beeinflussen den Wasserhaushalt, außerdem wird Kalium zusammen llit Magnesium für die Funktion von Muskel- und Nervenzellen benötigt.
Phosphor und Calcium sind wichtig Bestandteile von Knochen und Zähnen.
Eisen ist Zentralion des Hämoglobins und damit für den Sauerstofftransport unentbehrlich.
Wichtig ist, daß die Zusammensetzung der Inhaltsstoffe in Abhängigkeit von verschiedenen Faktoren variiert. Dazu gehören vor allem die Abhängigkeit von Sorte und Reifezustand, die wiederum von Klima, Boden und Emtetermin beeinflußt werden.
3. Der Reifungsprozeß
3.1 Beurteilung von Geschmack und Aussehen
Die Kaufentscheidung für einen bestimmten Apfel trifft der Verbraucher in der Regel nach dem Geschmack des Apfels. Am Geschmacksempfinden sind der Geschmackssinn (süß, sauer) und der Geruchssinn (Aroma) als chemische Sinne, der Tastsinn (weich, hart) und die Temperaturempfindung beteiligt.
Außerdem tragen auch optische Reize (z.B. bei der Bevorzugung roter oder grüner Äpfel) zum Geschmacksempfinden bei.
Der Geschmack des Apfels ist nicht nur sortentypisch, sondern abhängig vom Reifungszustand und damit auch abhängig vom Besonnungsgrad, dem Erntetermin und der Behandlung nach der Ernte.
Man unterscheidet zwei Reifezeiten: Die Baum- oder Pflückreife und die Genußreife. Früh- und Herbstäpfel können mit Genuß bereits gleich nach der Ernte gegessen werden. Späte Winteräpfel benötigen dagegen eine gewisse
Zeit der Nachreife. Für den Geschmack und damit für Verzehr und Weiterverarbeitung ist, wie bereits erwähnt, der Reifezustand der Frucht ein ganz entscheidendes Kriterium.
3.2 Veränderungen der Frucht während der Reifung
Während ihrer Entwicklung laufen in der Frucht komplizierte biochemische Prozesse ab. Zunächst ist die Fruchtemährungsphysiologisch von der Mutterpflanze abhängig, nach der Abtrennung vom Baum kann sie
r>
stoffwechselphysiologisch selbständig existieren. Später erlöschen langsam die gesteuerten Lebensvorgänge und ein ungesteuertes Wirken der Enzyme führt zum Verderb der Frucht. Die sogenannte Genußreife kennzeichnet den Zeitpunkt, bei dem die Entwicklung der Frucht soweit abgeschlossen ist, daß Ausfärbung, Saftigkeit, Aromagehalt und Säure-Zucker-Verhältnis einen
"harmonischen, fruchttypischen sensorischen Eindruck" machen.
Der bio-riemische Reifungsprozeß bei Äpfeln ist zu beobachten an Veränderungen im Aussehen und Verschiebungen in der Zusammensetzung der Inhaltsstoffe:
-Änderunqder Atmungsaktivität
-Umsatz von rund 200/0 der vorhandenen Kohlenhydrate:
-+
Abbau von Stärke, Hemicellulosen und Pektinen-+
Bildung von Zuckern (Glucose, Fructose, Saccharose) -Vernnqerunq des Fruchtsäurengehalts-Faroänderunq von grün zu andersfarbig (gelb, rot, braun) -Ausbildung des .sortentvplscnen" Aromas
In den folgenden Experimenten wird der Reifungsprozeß von Äpfeln untersucht. Die Versuche sollen zeigen, daß im Apfel während der Reifung und Lagerung eine Fülle von Veränderungen vor sich gehen: der Apfel .lebt" also.
VERSUCH 1: Atmung von Äpfeln
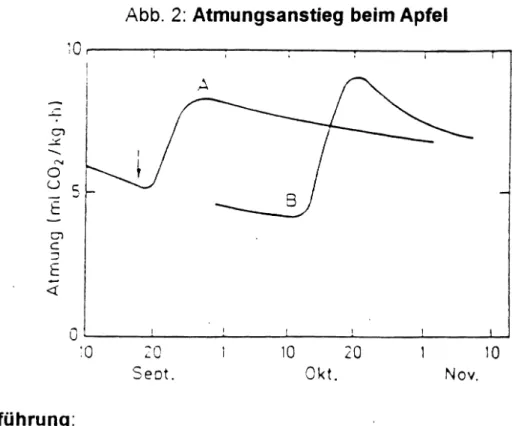
Die Atmungsintensität hängt vom Entwicklungszustand der Frucht ab. Mit zunehmenden Wachstum erfolgt zunächst ein Atmungsanstieg, der dann in einen langsamen AbfaU bis zur Reife übergeht (vgf. Abb. 2). Bei einer Reihe
,~
von Früchten ist das Einsetzen der Reifung mit einem erneuten Anstieg der Atmung verknüpft (sog. Klimakterium). In diesem Klimakterium wird ein Maximum der COrProduktion durchlaufen. das von einem Anstieg der Ethen- Produktion begleitet wird. In diesem Versuch wird die Atmung von Äpfel durch den Nachweis von CO2im entstehenden Gasgemisch gezeigt.
Abb. 2: Atmungsanstieg beim Apfel
;0r---r---~----_....~
-
E<i
10 Nov.
10 20
Okt.
:0 Seot.
O---olo..--~---_-...i_---'----"
~o
Du rchfü h ru ng:
Der Saugtopf wird durch den PVC-Schlauch mit dem Dreiwegehahn und dem Kolbenprober verbunden. In den Saugtopf werden anschließend zwei bis
drei Äpfel gegeben und Deckel und Unterteil gefettet. Die gesamte Apparatur muß dann auf ihre Dichtigkeit hin überprüft werden.
Nach einigen Tagen läßt sich am Kolbenprober eine Gasentwicklung ablesen. Die gebildete Gasmenge variiert stark und ist u.a. abhängig vom Reifezustand der verwendeten Äpfel und der Raumtemperatur.
Ein Teil der entwickelten Gasmenge wird über das Einleitungsrohr in das Demoreagenzglas mit Barytlauge eingeleitet. Als Blindprobe kann die Einleitung von Raumluft in Barytlauge durchgeführt werden, die negativ ausfällt.
Chemikalien: Barytlauge (gesättigte Ba(OH)2-Lsg.)
Materialien: Saugtopf, PVC-Schlauch (0 5mm), Kolbenprober mit Dreiwegehahn, Gummistopfen, Demoreagenzglas, Einleitungsrohr, Stativmaterial
Sonstiges: Äpfel (z.B. Boskoop)
Auswertung:
Die Trübung im Demoreagenzglas wird durch die Fällung von BaC03 hervorgerufen.
Die Ursachen für den Anstieg der CO2-Produktion werden noch nicht voll verstanden. Beteiligt sind chemische und physikalische Faktoren. Für denCOT"
Anstieg werden folgende Gründe diskutiert:
• Decarboxylierung von Malat undPyruvat
• Abnahme der Photosyntheseaktivität in der Frucht
• durch Enzyme katalysierte Abbauprozesse
VERSUCH 2: Nachweis von Chlorophyll in der Schale
An der Farbigkeit der Äpfel sind drei Farbstoffklassen (Pflanzliche Pigmente) beteiligt, die jeweils eine bestimmte Farbe der Schale verursachen. Die Chlorophylle bestimmen den Grün-Wert, außerdem während bzw. nach ihrem Abbau auch den Braun-Wert. Die Carotine und ihre Oxidationsprodukte, die Xanthophylle werden zur Gruppe der Carotinoide zusammengefaßt, sie sind für die gelben und auch roten Farben verantwortlich. Den Rot-Blau-Wert verursachen die Anthocyane, die zu den Flavonoiden gezählt werden.
Die Reifung der Äpfel ist meist mit einer Farbänderung gekoppelt. Der Übergang von grün zu andersfarbig geht zurück auf einen Chlorophyll-Abbau.
Die Carotinoide werden wie in den grünen Blätter von den Chlorophyllen verdeckt und werden erst nach deren Abbau sichtbar. Daneben kommt auch die Neu-Synthese von anderen Farbstoffen (z.B. Anthocyanen) vor. Die Farbe ist allerdings von der jeweiligen Apfelsorte abhängig. Grüne Äpfel sind daher nicht generell unreif.
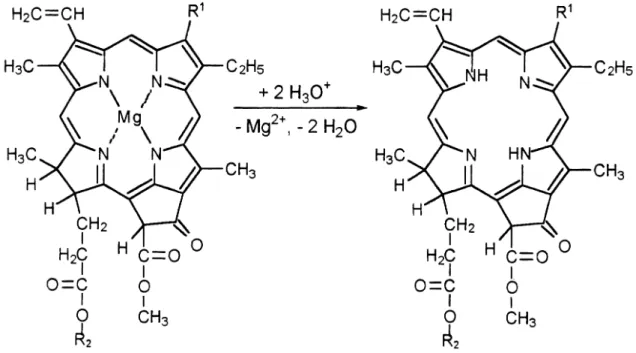
Unter normalen Bedingungen reifen die Äpfel am Baum aus, die Trennung der Frucht vom Baum erfolgt erst recht spät. Chlorophyll gehört chemisch gesehen zur Gruppe der strckstotthaltlqen Pyrrolfarbstoffe. Stickstoff spielt für die Nährstoffversorgung der Pflanze eine große Rolle, so daß Chlorophyll auf einem bisher weitgehend unbekannten Weg abgebaut werden, um den eingebauten Stickstoff zu .recyceln", Der Abbauprozeß wird eingeleitet durch einen Austausch des zentralen Magnesiumatoms gegen zwei Wassersstoffatome, so daß das braungrüne Phäophytin entsteht. Die Protonen stammen von schwachen Säuren (z.B. Kohlensäure, Essigsäure), die im Herbst vermehrt in den Zellen gebildet werden. Danach, so wird vermutet, wird vom Chlorophyllmolekül durch das Enzym Chlorophyllase der Phytolrest hydrolytisch abgespalten. Der Abbau des sogenannten Chlorophyllids, d.h. des Porphyrinringsystems ist dagegen völlig unbekannt. Die Verfärbung der Apfelschale bei reifenden Früchten beruht also auf den gleichen physiologischen Abbauprozeßen wie die herbstliche Blattverfärbung.
Abb. 3: Umwandlung von Chlorophyll in Phaeophytin durch Säuren
Durchführung:
Jeweils 2 Äpfel werden geschält und die Schalen unter Zugabe von methanoJischer Salzsäure-Lösung (1 ml Salzsäure auf 30 ml Methanol) im Küchenmixer zerkleinert. Anschließend werden die Blattschnitzel in den Mörser gegeben. Dazu kommt eine Spatelspitze Calciumcarbonat, das den sauren Zellsaft neutralisiert und etwas Seesand, der dem besseren Aufschluß der Zellen dient. Der Farbstoffextrakt wird gewonnen, indem man schrittweise etwas methanolische Salzsäure-Lösung zusetzt und kräftig im Mörser zerreibt.
Der Farbstoffextrakt wird entweder über einen Papierfilter oder über das Baumwolltuch abflltrlert. Die Extraktion wird solange weitergeführt, bis der Rückstand hell und blaß geworden ist. Die Extrakte werden in braunen Glasflaschen im Kühlschrank aufbewahrt.
20 ml des jeweiligen Farbstoffextrakts werden im Schütteltrichter mit der gleichen Menge Petroleumbenzin oder einem anderen unpolaren Lösungsmittel überschichtet und anschließend mehrere Male kräftig geschüttelt. Nach der Ausbildung der Phasengrenze kann der Versuch ausgewertet werden.
I~
Chemikalien: Methanol, konz. Salzsäure, Calciumcarbonat, Seesand, Petroleumbenzin (oder anderes unpolares Lösungs- mittel)
Materialien: Messer, Schere, Küchenmixer, Gummiwischer, Mörser.
mit Pistill, Spatel, Glastrichter, Baumwolltuch, Filter- papier, 2 braune Glasflaschen (50 ml), 2 Schüttel- trichter mit Stopfen (50 ml), Stativmaterial
Sonstiges: 2 reife und 2 unreife Äpfel (z.B. Golden Dellcious)
Auswertung:
Methanol ist mit Wasser unbegrenzt mischbar. Aber bereits nach kurzem Stehenlassen wird die Phasengrenze sichtbar, die sich zwischen dem hydrohilen wäßrigem Alkohol und dem stark hydrophoben (lipophilen) Petroleumbenzin ausbildet. Die obere unpolare Phase (Petroleumbenzin) enthält das Chlorophyll und ist dadurch deutlich grün gefärbt. Die hydrophoben Eigenschaften des Chlorophyllmoleküls lassen sich hauptsächlich auf den Phytylrest zurückführen. Phytol, d.h. der Phytylrest, ist ein einfach ungesättigter Alkohol, d'er aus einer langen Kohlenwasserstoffkette besteht, die entsprechend hydrophobe Eigenschaften besitzt. Allerdings zeigt das Chlorophyllmolekül auch hydrohile E.igenschaften, die bei der Extraktion mit methanolischer Salzsäure ausgenutzt werden. Hierfür sind die polaren Bereiche des Porphyringsystems verantwortlich, vor allem der Cyclopentanonring mit seiner Methoxycarbonyl-Gruppe.
Neben dem Chlorophyll sind in dieser Phase möglicherweise noch die gelben Carotine und die braunen Phäophytine enthalten, die ähnliche Eigenschaften wie die Chlorophylle besitzen, Carotine sind dagegen lange Wasserstoffketten mit konjugierten Doppelbindungen (Isopren-Einheiten), die ebenfalls nur in lipophilen Stoffen löslich sind.
Daneben gibt es weitere gelbe und rote Farbstoffe, die offenbar hydrophile Eigenschaften besitzen und sich dadurch in der polaren wäßrigen Phase lösen.
Es handelt sich dabei um die Xanthophylle (z.B. Xeaxanthin), die Oxidationsprodukte der Carotine.
In den Schalen der reifen Äpfel läßt sich durch das Ausschütteln mit Petroleumbenzin kein oder deutlich weniger Chlorophyll nachweisen.
Stattdessen treten die Carotinoide und das Phäophytin in den Vordergrund.
Abb. 4: Löslichkeit der pflanzlichen Pigmente
(1)Obere Phase: Petroleumbenzin ~ unpolar (lipophil)
Beispi~'e: Chlorophylle, ß-Caroti·n
(2) Untere Phase: MethanollWasser ~ polar (hydrophil) Beispiel: Zeaxanthin
HO
OH
VERSUCH 3: Titrimetrische Bestimmung des Fruchtsäuregehalts
Ein Merkmal von vielen Äpfel ist, daß sie sowohl süß als auch sauer schmecken. Der saure Geschmack wird hervorgerufen, durch die in den Früchten enthaltenen Fruchtsäuren. Beim Apfel ist wie beim anderen Kern- und
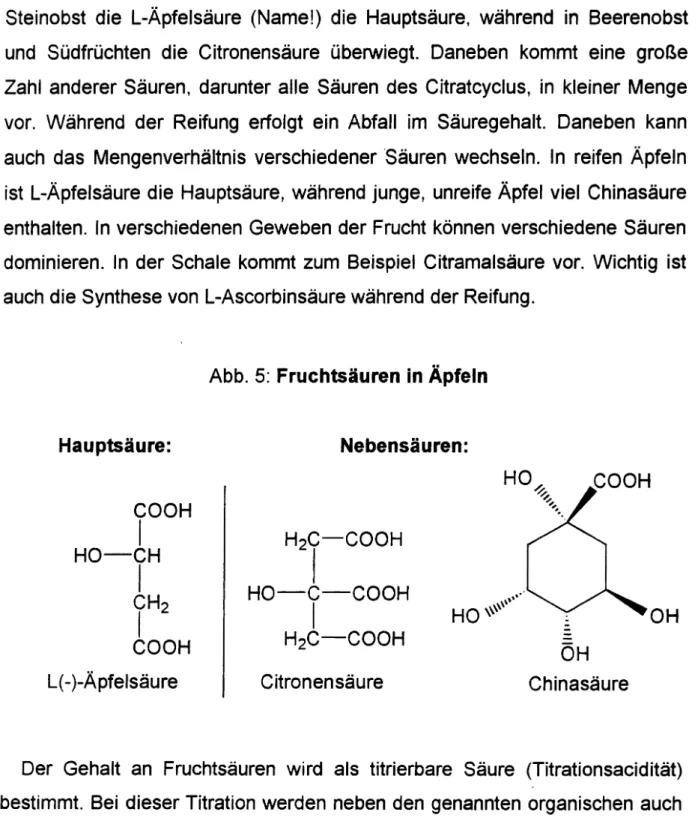
Steinobst die L-Äpfelsäure (Name!) die Hauptsäure, während in Beerenobst und Südfrüchten die Citronensäure überwiegt. Daneben kommt eine große Zahl anderer Säuren, darunter alle Säuren des Citratcyclus, in kleiner Menge vor. Während der Reifung erfolgt ein Abfall im Säuregehalt. Daneben kann auch das Mengenverhältnis verschiedener 'Säuren wechseln. In reifen Äpfeln ist L-Äpfelsäure die Hauptsäure, während junge, unreife Äpfel viel Chinasäure enthalten. In verschiedenen Geweben der Frucht können verschiedene Säuren dominieren. In der Schale kommt zum Beispiel Citramalsäure vor. Wichtig ist auch die Synthese von L-Ascorbinsäure während der Reifung.
Abb. 5: Fruchtsäuren in Äpfeln
Hauptsäure:
COOH
I
HO-CH CH
I
2COOH
I
L(-)-Äpfelsäure
Nebensäuren:
H2C-COOH
HO-C-COOH
I
H2C-COOH
I
Citronensäure
OH
OH
Chinasäure
Der Gehalt an Fruchtsäuren wird als titrierbare Säure (Titrationsacidität) bestimmt. Bei dieser Titration werden neben den genannten organischen auch die anorganischen Säuren erfaßt, die allerdings nur einen sehr niedrigen Anteil am Gesamtsäuregehalt haben.
Durchführung:
Je ein reifer und unreifer Apfel werden gewogen und im Küchenmixer unter Zugabe von wenig desto Wasser gründlich zerkleinert. Die Maische wird in einem 1 I Meßkolben mit desto Wasser bis zur Marke aufgefüllt. Vor der
Titration wird die Proben-Lösung durch ein Teesieb filtriert. 50 ml des Filtrats werden in das Becherglas einpipettiert und bis zum beginnenden Sieden erhitzt, um eventuell vorhandenes C02 auszutrieben. Durch Zusatz von ca.
50 ml desto Wasser (C02-frei) wird die Probe abgekühlt und anschließend die
pH-~lektrode eingesetzt. Die Titration mit Natronlauge erfolgt in 1 ml- bzw. in der Nähe des Äquivalenzpunkts in 0,5 mi-Schritten unter potentiometrischer Kontrolle bis auf pH
=
8,1. Die Änderung des pH-Werts kann auf dem angeschlossenen Meßgerät verfolgt werden. Möglicherweise kann der Endpunkt auch unter Zusatz des Indikators Phenolphthalein ermittelt werden.Aus dem Ergebnis wird anschließend der Gesamtsäuregehalt pro 100 g Apfel berechnet.
Chemikalien: Natronlauge (c(NaOH)
=
0,1 molllMaterialien: pH-Meter, 50 ml Bürette, Magnetrührer mit Rührfisch, Becherglas (250 ml, hohe Form), Vollpipette (50 ml), Messer, Küchenmixer, Teesieb, Meßkolben (1 I), pH- Elektrode, Meßgerät
Sonstiges: 2 Äpfel unterschiedlicher Reife
Auswertung:
HOOC-CH2-CH-COOH(aq) + 2 Na+(aq) + 2 OH-(aq)
OH
I
1l
-OOC-CH2-CH-COO(aq) + · 2 H20 + 2 Na"(aq)
OH
I
Der Endpunkt der Titration liegt im alkalischen Bereich, weil die zu bestimmende Acidität von schwachen Säuren hervorgerufen wird. Äpfelsäure
ist eine schwache zweiprotonige Säure (pKS1 = 3,40, pKS2
=
5,05), ihre Salze heißen Malate. Am Äquivalenzpunkt liegen die Salze dieser schachen Säuren vor. die dann entsprechend eine alkalische Reaktion der Lösung hervorrufen.Die Bestimmung der titrierbaren Säuren erfolgt nach der Bestimmungen der Internationalen Fruchtsaftunion, in denen auch der Endpunkt der Titration mit pH = 8,1 festgelegt ist, um den Säuregehalt verschiedener Fruchtsäfte vergleichen zu können. Die Berechnung des Fruchtsäurengehalts erfolgt vereinfacht als Äpfelsäure, der Hauptsäure in Äpfeln:
r ' Berechnung: Einwaage: 1649 Apfel auf 1000 ml Vorlage: 50 ml Proben-Lösung
ceq(NaOH) Meq(C4HsOs) t
VF
=
0,1 molll= 67,01 g/mol
= 1,0204
= 20
m(C4HsOs) = 5,2 ml * 136,75mg* rnl' =711 mg ::::> m(C4H60 S)/100g
=
430 mg=
0,43 9Fruchtsäurengehalt pro 100 9 Apfel (Golden Delicious)
• Apfel, "unreif' (frisch): 0,43 9
• Apfel, reif: 0,26 g
Der Fruchtsäurengehalt von Äpfel nimmt während der Reifung ab. Eine Ausnahme stellt dabei die Synthese von L-Ascorbinsäure dar, die während dieser Zeit erfolgt. Der Fruchtsäurengehalt von Äpfeln schwankt von Sorte zu
Sorte erheblich. Die Sorte Boskoop hat beispielsweise einen deutlich höheren Säuregehalt als die in diesem Versuch verwendete Sorte Golden Delicious.
Der in der Tabelle 1 genannte Wert von 0,65 g ist demnach als Durchschnittswert aufzufassen.
Die Abnahme des Fruchtsäurengehalts läßt sich auch durch die Messung des pH-Werts während der Reifung verfolgen. Dazu lagert man mehrere Äpfel einer Sorte bei Zimmertemperatur und bestimmt im Abstand von jeweils einer Woche den pH-Wert.
3.3 Auslösung der Reifung durch Ethen
Die natürliche Regulation des Pflanzenwachstums erfolgt durch mehrere Klassen von Phytohormonen. Die Reifung von Früchten ist mit der Biosynthese von Ethen gekoppelt. Die physiologischen Wirkungen des Phytohormons Ethen sind außerordentlich vielfältig. Neben der Beschleunigung der Fruchtreife fördert es den Blattfall und wirkt negativ gravitop. Vermutlich verändert Ethen in der Zelle die Permeabilität der Membranen. Bei vielen fleischigen Früchten so auch beim Apfel steigt der Ethen-Pegel nach dem Abschluß der Wachstumsphase steil an. Hierdurch werden die in Kapitel 3.2 genannten spezifischen Reifungsprozesse induziert.
Äpfel zeichnen sich durch eine vergleichsweise hohe endogene Ethen- Produktion aus. Daher sollten Äpfel nicht zusammen mit anderen Obst- und Gemüsearten gelagert werden. In der Praxis verhindert man durch die Blockierung der Ethen-Bildung durch Hemmstoffe oder durch Entfernung des gebildeten Ethen das Reifen während des Transports und der Lagerung. Zum gewünschten Zeitpunkt führt man die synchrone Reifung durch Ethen- Begasung herbei. Auch bei verschiedenen Citrusfrüchten wird dieses Verfahren angewendet. Beim Steinobst und bei Oliven kann durch Ethen- Begasung der Fruchtfall ausgelöst werden.
r:
Durch die Lagerung in kontrollierter Atmosphäre (CA-Lagerung, vgl. Tab. 2) können einige Apfelsorten bis zur neuen Ernte gehalten werden. Dabei wird die Atmosphäre der Kühlräume, was den OL' N2- und CO2-Gehalt betrifft, optimal auf die Ansprüche der jeweiligen Apfelsorte eingestellt. Durch eine Luftwäsche wird der Feuchtigkeitsgehalt ständig reguliert und außerdem das Ethen entfernt. Durch diese Maßnahmen wird der Stoffwechsel der Früchte erheblich verlangsamt sowie der Alterungs- und Abbauprozeß verzögert.
Mit Hilfe eines Gaschromatographen ist es möglich, den Ethen-Gehalt der Luft aus der in Versuch 1 verwendeten Apparatur zu ermitteln. Eine Messung ergab eine Ethen-Konzentration von 540 ppm. Die physiologische Wirkkonzentration von Ethen liegt im Bereich von 0,01-10 ppm und damit deutlich unterhalb der gemessenen Konzentration. Mit Hilfe dieser Apparatur läßt sich die Reifung der "eingelegten" Äpfel beschleunigen. Möglicherweise können diese Äpfel dann bei den Versuchen 2 und 3 eingesetzt werden.
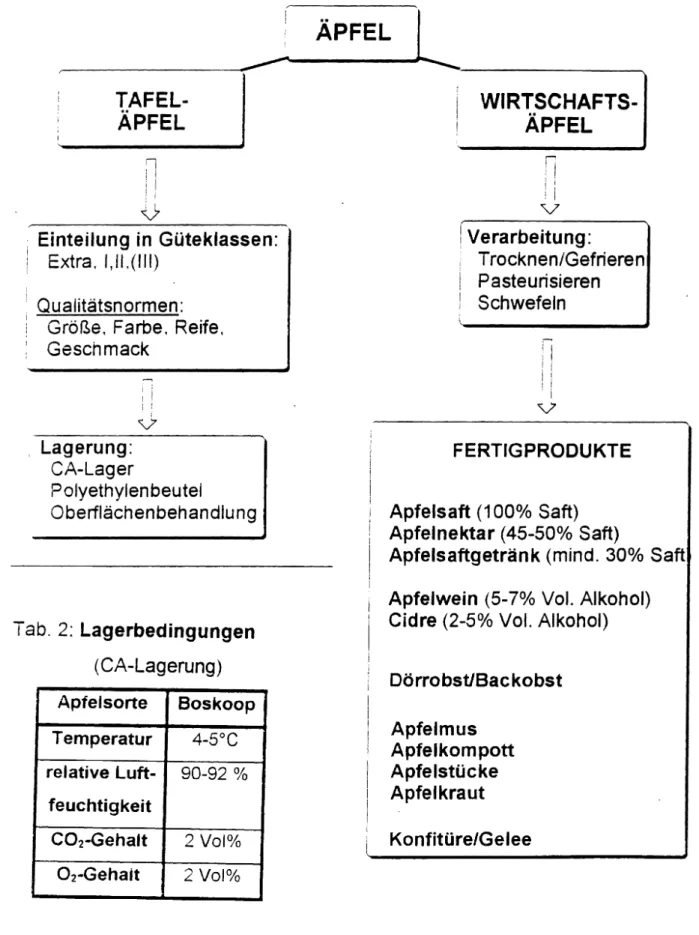
4. Alles aus Apfel - Überblick über die Produkte
In der Abbildung 5 ist eine Auswahl der aus Äpfeln hergestellten Produkte
r>.
gegeben. In der Praxis unterscheidet man zwischen den für den Frischverzehr vorgesehenen Tafeläpfeln und den Wirtschaftsäpfeln, die ausschließlich der Verarbeitung zugeführt werden und damit der Herstellung von verschiedenen Apfel-Produkten dienen.
Abb. 5: Verschiedene Apfelprodukte
,.--.---...-~
TAFEL- ÄPFEL
n
i I
i i
D
Einteilung in Güteklassen:
Extra, I,JI.(III)
i Qualitätsnormen:
Größe, Farbe, Reife, Geschmack
; !
I !
i !
I Lagerung:
CA-Lager
Polyethylen beutet
Oberilächenbehandlung
.r>.
Tab. 2:
Lagerbedingungen
(CA-Lagerung) Apfelsorte Boskoop Temperatur 4-SoC relative Luft- 90-92 %
feuchtigkeit
CO2-Gehatt 2 VoI°;{' Os-Gehalt 2 Voj%
ÄPFEL
l
- - - -
WIRTSCHAFTS·
ÄPFEL
r!I
I ;
i I
<r Verarbeitung:
Trocknen/Gefrieren Pasteurisieren Schwefeln
11i'
!i : !I I
. i V
FERTIGPRODUKTE
Apfelsaft (1000/0 Saft) Apfelnektar (45-50% Saft)
Apfelsaftgetränk (mind. 30% Saft Apfelwein (5-7% Vol. Alkohol) Cidre (2-50/0 Vol. Alkohol)
Dörrobst/Backobst Apfelmus
Apfelkompott Apfelstücke Apfelkraut Konfitüre/Gelee
19
5. Die enzymatische Bräunung
Eine täglich beobachtbare Reaktion bei der Verarbeitung von pflanzlichen Lebensmitteln ist das Braunwerden von Obst- und Gemüsearten, deren Schnittflächen der Luft ausgesetzt werden. Die Intensität der bei der Zerkleinerung auftretenden Farbänderung ist abhängig vom Zerkleinerungsgrad der Lebensmittel und der Einwirkungsdauer von Luftsauerstoff auf die freigelegten Oberflächen. Auch bei der Herstellung von Apfelsaft spielen die als enzymatische Bräunung bezeichneten Vorgänge eine große Rolle.
,,--.
Der Saft der Apfelzelle ist farblos. Erst nach der Zerstörung des Gewebes und damit auch der Zellen färbt sich der Saft bräunlich. An den Reaktionen sind phenolische Verbindungen, das Enzym Polyphenoloxidase (PPO) und der Luftsauerstoff beteiligt. In der intakten Zelle sind die PPO und ihr Substrat, die phenolischen Verbindungen, in unterschiedlichen Kompartimenten untergebracht. Bei der Saftherstellung werden die Zellen zerstört, so daß Enzym und Substrat zusammenkommen und dadurch die Farbänderung bewirken.
Die Gesamtmenge der phenolischen Verbindungen in Äpfel liegt zwischen 0,1 und 1 %. Wichtig sind dabei vor allem Chlorogensäure, Catechin und r>
Epicatechin. Daneben spielen auch Gerbstoffe eine Rolle, die zum astringierend-bitteren Geschmack der Früchte beitragen.
Abb. 6: Phenolische Verbindungen in Äpfeln
Epicatechin (2R, 3R) Catechin (2R, 35)
OH COOH
o
Chlorogensäure HO
HO
,(!f0H
'~OH
OH OH
HO
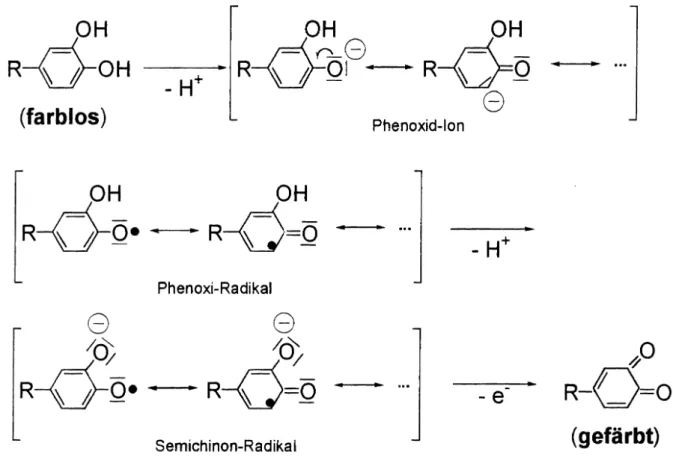
Abb. 7: Mechanismus der enzymatischen Bräunung:
(1) 'PPO oxidiert phenolische Verbindungen durch Übertragung von O2 (Oxidation: formal: + %O2 , - H20 )
OH OH OH
R-i )-OH
..-R - 6 ' - 8
~!J 01 ..
'. R--6=O
•.. . ..
- H+ 8
(farblos) Phenoxid-Ion
~'
OH OH
R-i )-oe .. .. R-Q 0 ..
.,... - H+ ..
Phenoxi-Radikal
8 8
/0) /0'
~OR-i )=oe
• •R-Q/O .
• ...
-e-
•R-< )=0
Semichinon-Radikal (gefärbt)
(2) Reaktionen der prim. Oxidationsprodukte (u. Folgereaktionen) z.B. 1,4-Cycloaddition nach Diels-Alder
--... . ..
o
IO~/
R
Dienophil Dien
~~0°_-. o
R~O Y
~R
Bei der PPO handelt es sich um einen Enzymkomplex, in dem mehrere Metallze.ntren (u.a. Cu) enthalten sind, die genau Struktur und Funktionsweise
ist noch unbekannt. Die PPO übertragt O2, d.h. sie oxidiert das jeweilige Phenol. Außerdem katalysiert die PPO die Hydroxylierung von Monohydroxyphenolen und dann die Oxidation von o-Dihydroxyphenolen zu 0-
Chinonen.
Die primären Oxidationsprodukte, die o-Chinoide sind farbig, Catechinon ist beispielsweise gelb. Die eigentliche Bräunung wird verursacht durch eine Vielzahl von Folgereaktionen, die in der Literatur vereinfacht als
"Polymerisation" bezeichnet werden. In Wirklichkeit ist das Reaktionsgeschehen sehr viel komplizierter. Die o-Chinoide dimerisieren beispielsweise in einer Diels-Alder-Cycloaddition und bilden anschließend komplexe Strukturen, die dann unter Abspaltung von CO2 und nachfolgenden Oxidationen weiter reagieren können. Dieses .Verblndunqsqemisch" ist für die braune Farbe verantwortl ich.
Die beim Mahlen und Auspressen der Äpfel ablaufenden Reaktionen sind zum Teil erwünscht, weil sie zur Farbe des Saftes beitragen. Allerdings dürfen die Oxidationen nicht zu weit fortschreiten, weil sonst der Saft zu dunkel würde.
Daneben kommt es durch Oxidationsvorgänge zur unerwünschten Beeinträchtigung des Aromas.
VERSUCH 4: L-Ascorbinsäure als Antioxidationsmittel
Um die enzymatische Bräunung zu verhindern bzw. einzuschränken, ist es notwendig, die Phenoloxidasen zu inaktivieren oder den Luftsauerstoff während der Verarbeitung und Lagerung auszuschließen. Die Verarbeitung der Lebensmittel wird in einer Stickstoff-Atmosphäre (Schutzgas) durchgeführt, während die Endprodukte durch Vakuumverpackung vor dem Sauerstoff geschützt werden. Die PPO kann durch eine kurzzeitige Hitzebehandlung oder durch eine Erniedrigung des pH-Werts inaktiviert werden. Daneben werden Antioxidationsmittel wie L-Ascorbinsäure verwendet. In der Praxis der Apfelsaftherstellung werden Mengen von 0,5-1 g L-Ascorbinsäure pro Liter Saft
,r---..
entweder direkt beim Mahlungsvorgang oder erst später in die Maische gegeben. Zusätzlich arbeitet man während des gesamten Herstellungsprozesses unter Stickstoff als Schutzgas. Größere Menge an L- Ascorbinsäure können sogenannte enzymatische Bräunungsreaktionen hervorrufen und werden daher vermieden. In diesem Versuch wird die Möglichkeit gezeigt, die Oxidationsvorgänge durch den Einsatz von L- Ascorbinsäure zu steuern oder zu verhindern.
Durchführunq.
Chemikalien: L-Ascorbinsäure
Materialien: Küchenreibe, Plastikschale, Baumwolltuch, Glas- trichter, 3 Demoreagenzgläser, Spatel
Sonstiges: 3 Äpfel (bzw. frisch gepreßter Apfelsaft)
Die Äpfel werden mit Hilfe der Küchenreibe zerkleinert und aus der Maische der Saft über ein Baumwolltuch ausgepreßt. In die Demoreagenzgläser gibt man etwa 50 ml Saft und in eines zusätzlich eine Spatelspitze L-Ascorbinsäure und schüttelt gut durch. Nach 10-15 Minuten gibt man zu einer weiteren Probe eine Spatelspitze L-Ascorbinsäure und mischt gut durch.
Auswertung:
Der Apfelsaft ohne L-Ascorbinsäure wird innerhalb von wenigen Minuten braun während die entsprechende Gegenprobe sich kaum verfärbt. Die Bräunung läßt sich außerdem mehr oder weniger rückgängig machen, wie der Zusatz von L-Ascorbinsäure zu einer weiteren Probe zeigt. Bereits nach einer Minute hellt sich der so behandelte Saft deutlich auf.
L-Ascorbinsäure reduziert die farbigen primären Oxidationsprodukte zu den farblosen phenolischen Verbindungen. Diese reduzierende Wirkung der L- Ascorbinsäure hält solange an, bis sie vollständig zur Dehydro-L- ascorbinsäure oxidiert worden ist.
Abb.8: Redoxgleichgewicht (vereinfacht)
OH
I 0
HO-C H
2-C H --q0
HO OH
L-Ascorbinsäure
Bei fortgeschrittener enzymatischer Bräunung können die rasch entstehenden komplexen Folgeprodukte nur noch eingeschränkt aufgehellt werden. Neben der reduzierenden Wirkung auf die phenolischen Inhaltsstoffe hemmt L- Ascorbinsäure wahrscheinlich auch die PPO.
Abb.9: Reduktion der primären Oxidationsprodukte
~O
R-< )=0
(gefärbt)
o
OHR -(-yO ;=\
+ 2
H - - "
R - VOHHO OH
(farblos)
...
6. Pektin: Vorkommen, Struktur, Gewinnung
Pektinstoffe oder kurz Pektine (von griechisch pectos = geronnen, erstarrt) sind hochpolymere Heteropolysaccharide, die in der Zellwand und MitteIlamelIe höherer Pflanzen vorkommen. Der Begriff .Pektinstoffe" ist eine Sammelbezeichnung für diese Gruppe. Hauptbestandteil ist Polygalacturonsäure, die aus a-1,4-glykosidisch verknüpften 0- Galacturonsäure-Bausteinen besteht. Die Galacturonsäure-Monomere sind innerhalb der Kette zickzackförmig gegeneinander verdreht (Faltblattstruktur).
Der Polymerisationsgrad variert. die Kettenlänge liegt zwischen 100 bis über 1000 Bausteinen.
Abb. 10:Struktur von Pektin
6
H~O
COOH4
' '\L./~
13 12 OH
OH
a-D-Galacturonsäure
OH
COOCH:3
0 -
Polygalacturonsäure-Kette (partiell mit Methanol verestert)
Die reine Polygalacturonsäure wird auch als Pektinsäure bezeichnet. In der Natur ist die Pektinsäure, die Salze heißen Pektate. unterschiedlich stark mit Methanol verestert. Man spricht dann von Pektin.
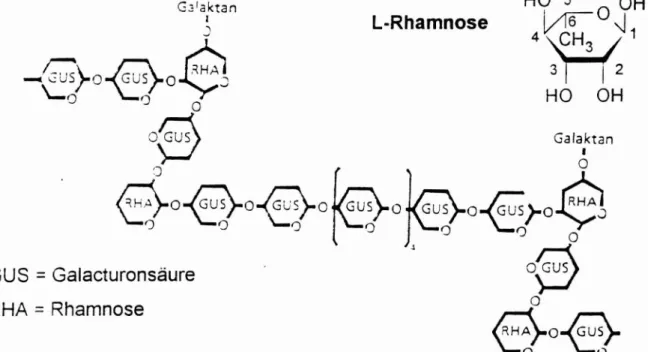
Abb. 11: Hauptkette mit eingelagerten Rhamnose-Molekülen HO 5 0 OH
4~ ~1
~
HO OH L-RhamnoseG3'aktan
I
J
e s\.-
-6- ' ' S $:\HA
- '-.:u /"0 "u 0 ;J
'-0
'J oO~GUS>
Gala,ktan6-
'J0 -8-
'J0 -6-
'J0 6 ~~ ~Y" JQ o~ro ~ \:; Y'
GUS =Galacturonsäure' '
O~Gus>
0
o-0-
RHA = Rhamnose
-
. "
In die lineare Hauptkette aus Polygalacturonsäure sind a-1,2-glykosidisch verknüpfte Rhamnose-Moleküle eingelagert. Die Verteilung der Rhamnose- Moleküle über das Pektinmolekül ist ungleichmäßig. An die Rhamnose- Moleküle sind weitere Neutralzucker, entweder als Monomer (Galactose, Arabinose) oder als längere Seitenkette (Galactan, Araban) geknüpft. Die homogene Struktur wird durch Rhamnose und die Neutralzucker-Seitenketten gestört. Rhamnose-Moleküle bewirken jeweils einen Knick in der Kette.
Pektin ist neben Cellulose und Hemicellulosen am Aufbau der pflanzlichen Zellwand beteiligt. Dabei kommt Pektin in seiner wasserunlöslichen Form als Protopektin in der MitteIlamelIe in weitaus höheren Konzentrationen vor als in den Sekundärwänden. Es fungiert dabei als Gerüst- und Kittsubstanz und bewirkt den Zusammenhalt der Zellen im Zellverband. Der Blattfall im Herbst und das "Mehligwerden" von Äpfeln und anderen Früchten ist auf den enzymatischen Pektinabbau zurückzuführen. Die Zellwände benachbarter Zellen sind in diesem Zustand gegeneinander verschiebbar und die Struktur des Gewebes geht somit verloren.
Der Pektingehalt von Pflanzen schwankt ganz erheblich, nur wenige sind daher für die technische Pektingewinnung geeignet.
Tab. 3: Pektingehalte verschiedener Pflanzenmaterialien Pflanzenmaterial Pektin-Gehalt [%]
(Frischgewicht)
Apfel 0,5-1,6
Tomaten 0,2-0 ,5
Grapefruit 1,6-4,5 Johannis-Beeren 0,9-1.5
Rohstoff Pektin-Gehalt [%]
(Trockenmasse)
Apfeltrester 15
Zuckerrübenschnitzel 20
Zitronenschalen 30
Pektine werden heute aus Trockentrestern von Äpfeln und Citrusfrüchten hergestellt. Die Trester fallen in der Regel als Nebenprodukt bei der Saftpressung an und enthalten einen relativ hohen Anteil an Pektin. Das Rohmaterial. wird dabei in getrockneter Form verarbeitet, um Gärprozesse zu vermeiden und die Trester dadurch länger lagerfähig zu machen. Bei der industriellen Pektinherstellung wird durch saure Extraktion mit verdünnten Mineralsäuren ein Pektinextrakt gewonnen, der nach Trennung und Reinigung mit Alkohol aus der Lösung gefällt wird. Nach Trocknung und Mahlung wird das Rein-Pektin homogenisiert. Der Veresterungsgrad kann (grob) durch den Extraktionsprozeß beeinflußt werden.
Pektin spielt als Zusatzstoff (E 440) in der Lebensmitteltechnologie eine große Rolle. Die Hauptverwendung besteht in seiner Funktion als Geliermittel.
Neben Konfitüren, Marmeladen und Gelees werden Pektine auch zur Herstellung von Süßwaren und in Fruchtzubereitungen in Milch- und Backwaren eingesetzt. Daneben dienen Pektine zur StabiJisierung von Fruchtgetränken und zur Herstellung von Emulsionen und Suspensionen in der Pharmazie.
Als Ballaststoffe spielen Pektine im Rahmen der Ernährung eine wichtige Rolle. Ballaststoffe können im Dünndarm des Menschen nicht verdaut werden und gelangen mit anderen unverdaulichen Nahrungsbestandteilen in den Dickdarm. Hier binden sie Wasser, quellen und vergrößern dadurch die Darmfüllung, was die Darmtätigkeit anregt und Verstopfungen verhindert.
7. Pektin-spaltende Enzyme
Pektin-spaltende Enzyme werden auch als pekt(in)olytische Enzyme bezeichnet. Daneben findet man den Begriff .Pektinasen" als allgemeine Sammelbezeichung für Pektin-spaltende Enzyme.
Pektinolytische Enzyme findet man in fast allen höheren Pflanzen, aber auch in Schimmelpilzen, Hefen und pflanzenpathogenen Mikroorganismen. Diese Fermente spielen im Stoffwechsel von grünen Pflanzen, besonders bei der Keimung der Samen und beim Reifen der Früchte, eine wichtige Rolle.
Zur Produktion von Pektin-spaltenden Enzymen im industriellen Maßstab eignen sich am besten Kulturen des Schimmelpilzes Aspergillus niger. Aus den Pilzkulturen werden die Enzyme extrahiert und gereinigt, um unerwünschte Wirkungen anderer Enzyme des Pilzes auszuschließen.
Nach ihrer Wirkungsweise lassen sich zwei Gruppen von pektinolytischen Enzymen unterscheiden. Pektinesterasen katalysieren die Abspaltung der Methoxyl-Gruppen des Pektins. Dabei entstehen unter Anlagerung von Wasser die freien Carboxyl-Gruppen, und Methanol wird freigesetzt. Die zweite Gruppe umfaßt Pektinhydrolasen und Pektinlyasen, wobei alle Enzyme dieser Gruppe die Polygalacturonsäure-Hauptkette spalten und damit allgemeiner als Depolymerasen zusammengefaßt werden können. Zu den Pektinhydrolasen gehört die Polygalacturonase, welche die a-1,4-glykosidische Bindung hydrolytisch spaltet. Im Gegensatz dazu spalten die Pektinlyasen die Hauptkette in einer ß-Eliminierungsreaktion. Die verschiedenen Enzyme unterscheiden sich nicht nur in ihrem jeweiligen Substrat, sondern auch in ihrem Angriffsort am Substrat. Man spricht in diesem Zusammenhang von endo- und exo- Enzymen.
Pektinolytische Enzyme spielen bei der Verarbeitung von Obst und Gemüse eine entscheidende Rolle, wobei sowohl positive als auch negative Einflüsse zu verzeichnen sind. Vor allem Beerenobst hat einen hohen Gehalt an wasserlöslichem Pektin (vgl. Tab. 3). Die vermahlenen Beeren bilden eine feste Galerte, die nur wenig Saft abtropfen läßt~ Erst durch den Pektinabbau wird eine vernünftige Saftausbeute (vgl. Versuch 5a) ermöglicht. Neben der Verflüssigung von Maischen werden pektinolytische Enzyme bei der Fermentation von Kaffee- und Kakaobohnen und zur Trubstabilisierung in naturtrüben Obst- und Gemüsesäften (vgl. Versuch 5b) eingesetzt. Der Anwendungsbereich der verschiedenen pektinolytischen Enzyme ist ziemlich
vielfältig und wird sich zukünftig im Rahmen der Lebensmitteltechnologie noch weiter ausweiten.
VERSUCH 5a: Saftausbeute aus Apfelmaische
Als Geliermittel sind Pektine bei der Produktion verschiedener Fruchtzubereitungen (vgl. Versuch 6) unerläßlich. Auf die Saftgewinnung aus Früchten wirken sich Pektine dagegen störend aus. Der Fruchtsaft wird dabei mechanisch aus den Früchten gepreßt. Wegen' ihres
r:-.
Wasserbindungsvermögens halten Pektine dabei viel Saft im Apfeltrester zurück und mit diesem auch Farbstoffe, Aromastoffe und Zucker. Zusätzlich löst sich ein Teil der Pektine im Saft und verhindert dadurch weitgehend das Absetzen von Trübstoffen.
Die in der Fruchtsaftindustrie hergestellten Säfte werden durch Erhitzen haltbargemacht und aus Kostengründen häufig in Form von Konzentraten transportiert und gelagert. Vor der. Abfüllung und dem Verkauf wird das Fruchtsaftkonzentrat mit Wasser rückverdünnt. Fruchtsäfte mit hohem Pektingehalt können jedoch nicht konzentriert werden. Sie beginnen frühzeitig zu gelieren und verstopfen dabei zum Beispiel die Abfüllmaschinen. Um das
«<.
Gelieren zu verhindern und um die Fruchtpreßsäfte von Trübstoffen zu befreien werden in der Industrie Pektin-spaltende Enzyme eingesetzt.
In diesem Versuch wird die Erhöhung der Saftausbeute und die Klärung von frisch gepreßtem Apfelsaft durch den Einsatz pektinolytischer Enzyme gezeigt.
Durchführung:
Der ungeschälte Apfel (etwa 250 g) wird auf der Küchenreibe über einer Plastikschale gerieben. Die Apfelmaische wird zu gleichen Teilen in zwei Bechergläser eingewogen. Zu der ersten Maischeprobe gibt man 2 ml der Enzymlösung (Mengen vorher ausprobieren) und 8 ml Wasser und zur zweiten Maischeprobe pipettiert man entsprechend 10 ml Wasser. Die Maischen
werden mit einem Glasstab regelmäßig umgerührt und nach etwa 15 min aus den Bechergläsern in je ein Teesieb geschüttet. Dabei dürfen die Maischen nicht in das Teesieb hineingedrückt werden. Über den Trichter kann der Saft in einen Meßzylinder ablaufen. Nach einigen Minuten kann die Saftmenge in den Meßzylindern abgelesen werden.
Chemikalien: pektinolytisches Enzymgemisch (z.B."Kitzinger Antigel"
oder Enzympräparat der Fa. Novo Nordisk. Mainz) Materialien: Küchenreibe,Plastikschale, 2 Bechergläser (100 ml),2
Gummiwischer, 2 Glasstäbe, Stativmaterial, 2 Meß- zylinder (10mi),2 Meßzylinder (50 ml),2 Teesiebe, 2 Glastrichter,
Sonstiges: Apfel
Auswertung:
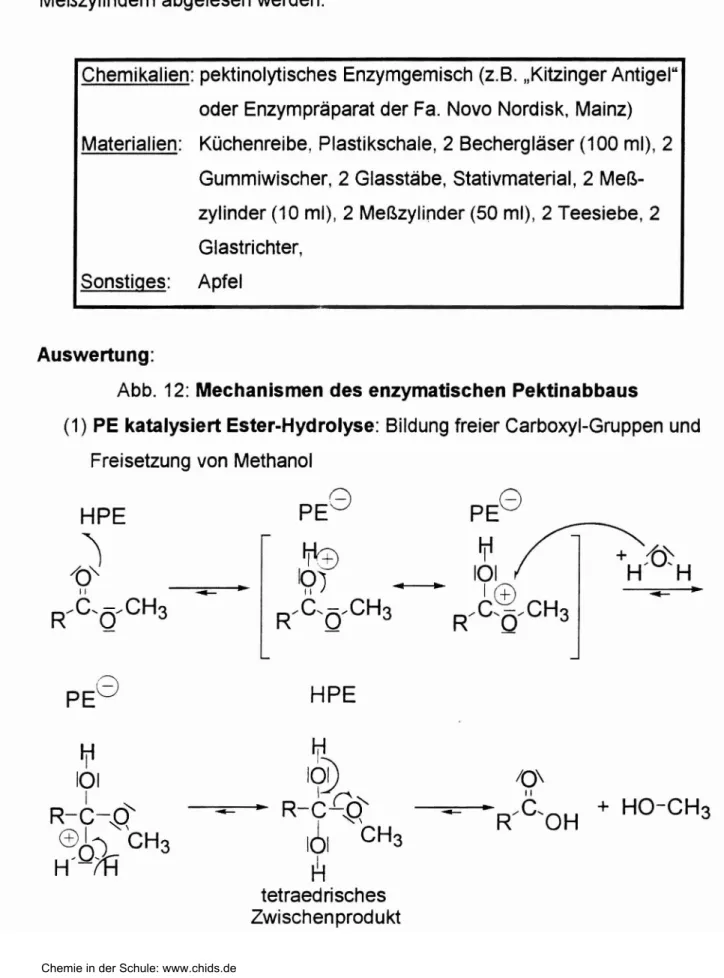
Abb. 12:Mechanismen des enzymatischen Pektinabbaus
(1) PE katalysiert Ester-Hydrolyse: Bildung freier Carboxyl-Gruppen und Freisetzung von Methanol
PE 9
19')
®
R"C'Ö"CH3
HPE
10]) ~
-- • R-C ~o'
16\ ~'cH3
tetraedrisches
~
Zwischenprodukt
(2) PG katalysiert Hydrolyse deru-1,4-glykosidischen Bindung
OOH OH
0
O~HH OH
I I
H
+H+c,,/C~
~..
o 0
OH COOH
Kettenende
OOH OH
O~HI
H
IOH - C sH
1007C
0 C OH
..- ~C;O~
.r> I
0
OH H COOH
Kettenende
... 0
.. ..
OH OH
H
OOH
O~~ C~
/O'-H
OH
HOOH
~-O H
OH
neues Kettenende
Aus der mit der Enzymlösung behandelten Maische läuft deutlich mehr Saft ab, der außerdem heller bleibt als der aus der unbehandelten Maische. Durch die sogenannte Maische-Enzymierung wird die Saftausbeute deutlich erhöht.
Das pflanzliche Pektin wird abgebaut und kann daher kaum noch Wasser und andere Inhaltsstoffe im Gewebe zurückhalten.
Als Beispiele für den enzymatischen Pektinabbau werden die katalytische Wirkung der Pektinesterase (PE) und die einer Polyqatacturonase (PG) beschrieben. Die PE spaltet unter Anlagerung von Wasser die Methoxyl- Gruppen des Pektins ab. Je nach Ausmaß der Esterhydrolyse entstehen dabei niedriger veresterte Pektine oder sogar Pektinsäure. Erst danach wird die Polygalacturonase aktiv und spaltet hydrolytisch Mono- oder Di- Galacturonsäure-Einhiten von der Hauptkette ab. Die beteiligten Mechanismen sind insofern vereinfacht dargestellt, weil die genaue Funktionsweise bzw.
katalytische Wirkung der Enzyme noch' nicht in allen Einzelheiten bekannt ist.
VERSUCH 5b: Klären von Apfelsaft
Frisch gepreßte Fruchtsäfte sind oft trüb und lassen sich schlecht filtrieren.
Zu den Trübstoffen gehören Fruchtfleischreste, Proteine, oxidierte und kondensierte Polyphenole, mehrwertige Metallionen (teilweise komplexiert) und Kohlenhydrate. Die meisten Trübstoffe liegen im Saft kolloidal gelöst vor.
Dabei fungiert das negativ geladene Pektin als Schutzkolloid, (vgl. Abb. 13) daß beispielsweise die positiv geladenen Proteinkerne (pH-Wert unterhalb des isoelektrischen Punkts) als Schutzhülle umgibt und auf diese Weise die
r>.
Teilchen stabilisiert.
Bei der Herstellung von naturtrüben Apfelsäften ist diese sogenannte .Trubstabtüetenmq" erwünscht. Durch den kombinierten Einsatz von PE und PG werden Galakturonsäure-Oligomere gebildet, "die bei einen Polymerisationsgrad von 8-15 Galacturonsäure-Einheiten eine kolloid- stabilisierende Wirkung besitzen. Die vollständige Entesterung und Spaltung der Kette muß dann allerdings durch rasche Pasteurisation und die damit verbundene Inaktivierung der Enzyme verhindert werden.
Unerwünscht und hinderlich ist die Schutzkolloidwirkung des Pektins bei der Herstellung von klaren Fruchtsäften. Durch den Einsatz von Pektin-spaltenden
Enzymen über einen längeren Zeitraum kann die sogenannte .F ruchtsattsch önunq"oder das "Klären" erzielt werden.
Durchführung:
Chemikalien: Ethanol, pektinolytisches Enzymgemisch (s.o.) Materialien: Küchenreibe, Plastikschale, Glastrichter, Baumwoll-
tuch, Becherglas (250 ml), 3 Demoreagenzgläser, 3 Stopfen, Glasstab
Sonstiges: Äpfel
Die Äpfel werden mit Hilfe der Küchenreibe zerkleinert und aus der so erhaltenen Maische der Saft über ein Baumwolltuch ausgepreßt. In die Demoreagenzgläser gibt man jeweils etwa 50 ml Saft und in eines zusätzlich 1 ml des Enzymgemisches und verrührt mit einem Glasstab. Nach etwa 10 Minuten gibt man in zwei der Demoreagenzgläser je 50 ml Ethanol, während man eine Probe des unbehandelten Saftes ohne Ethanol beläßt. Die Demoreagenzgläser werden mit einem Stopfen verschlossen, zweimal vorsichtig geschüttelt und dann ruhig stehen gelassen.
Auswertung:
Bereits nach kurzer Zeit ist das Ergebnis ablesbar. In dem Versuchsansatz ohne Pektin-spaltende Enzyme bildet sich ein Gelpfropfen, der an der Oberfläche bleibt,während sich in dem anderen Versuchsansatz die Trübstoffe allmählich absetzen. Das Pektin wird durch die pektinolytischen Enzyme abgebaut und kann daher nicht mehr als Sctiutzkolloid für die Trübstoffe fungieren. Die Trubteilchen aggregieren aufgrund der Ladungsunterschiede zu größeren Klastem, die leicht sedimentieren. In der Lebensmitteltechnologie schließt sich an die Ausflockung eine Filtration über Cellulose oder Kieselgur an.
~-...
,~
In der wäßrigen Lösung sind die Pektinmoleküle stark hydratisiert. Nach der Zugabe von Ethanol konkurrieren die Ethanol-Moleküle mit den Pektin- Molekülen um die Wasserhülle. Die Ethanol-Moleküle beanspruchen einen Teil des Wassers für ihre eigene Hydrathülle, so daß letztendlich das Pektin-Sol in ein Pektin-Gel überführt wird. Das Pektin-Gel ist spezifisch leichter als das Wasser und bildet einen Pfropfen an der Oberfläche. Die Bildung eines Pektin- Gels durch Zugabe von Alkohol wird bei der technischen Herstellung von Pektin ausgenutzt (Pektin-Fällung).
8.
Eigenschaften von Pektin: GeliermechanismenPektin ist wasserlöslich. wobei die Löslichkeit wiederum von verschiedenen Faktoren (Temperatur. Trockensubstanzgehalt, pH-Wert. u.a.) abhängt. Unter geeigneten Bedingungen lassen sich 2-10 %ige Lösungen herstellen. Dabei ist zu beachten. daß Pektin-Lösungen zudem noch viskos sind und unter bestimmten Bedingungen Gele bilden. Dieser Eigenschaft, d.h. der Fähigkeit zu gelieren. verdankt Pektin seine große Bedeutung. Bei der Herstellung von
Pektin-Lösungen muß man entweder mit sehr schnell rührenden Rührwerken in 60-80
oe
heißem Wasser arbeiten oder das Pektin in rund 20 % der Trockenmass.e (Zucker) trocken vormischen und erst dann in das heiße Wasser einrühren.Viele Faktoren nehmen Einfluß auf die Stabilität von Pektin-Lösungen, pH- Wert und Temperatur sind dabei die wichtigsten. Im allgemeinen sind Pektin- Lösungen bei pH 3-4 und Raumtemperatur stabil. Bei niedrigerem pH-Wert und einer mäßig erhöhten Temperatur erfolgt zunächst die Abspaltung der Ester-Gruppen, bei noch höherer Temperatur tritt zusätzlich der Kettenabbau ein. Pektin-Lösungen sollten daher nicht über längere Zeit gelagert werden, da Pektin außerdem noch leicht enzymatisch abgebaut werden kann.
Die Haupt-Eigenschaft des Pektins besteht in seiner Gelierfähigkeit. Die modemen Geltheorien gehen davon aus, daß es zwischen den Molekülketten zur Ausbildung begrenzter Haftzonen kommt. Unregelmäßigkeiten im Molekül in der Anordnung der Ester-Gruppen oder die Einlagerung von Rhamnose- Molekülen oder eine Seitenkette aus Neutralzuckem sorgen dafür, daß solche Haftzonen nur kurz sind und daneben freie Kettenstücke vorhanden sind. Durch die Ausbildung der Haftzonen entsteht ein dreidimensionales Netzwerk (Pektin- Gei), in dem Wasser, Zucker und andere lösliche Stoffe gehalten werden können.
Die GelbUdung wird auch wieder durch eine Vielzahl von Faktoren beeinflußt, die wichtigsten davon sind:
• Pektintyp
• Trockensubstanzgehalt (Zucker, Fruchtanteil)
• mehrwertige Ionen (z.B. Ca2+)
• pH-Wert (Säuregehalt)
• Temperatur
In ihrem Gelierverhalten unterscheiden sich die niedrigveresterten Pektine (NV-Pektine) von den hochveresterten Pektinen (HV-Pektine). Der
Veresterungsgrad von NV-Pektinen liegt unter 50 %. der von HV-Pektinen entsprechend über 50 %. Als Veresterungsgrad wird dabei das statistische Verhältnis der veresterten zu den gesamten Galakturonsäure-Gruppen bezeichnet. Der hat Einfluß auf die Löslichkeit und eben auch auf die Geliereigenschaften des Pektins. Die Handelspektine haben je nach Pektintype einen Veresterungsgrad zwischen 25 und 75%.
Abb. 14:Modell des molekularen Netzwerks eines Pektin-Gels
-Haftzonen
/ /
/
'/ /
VERSUCH 6a: Gelierverhalten niedrigveresterter Pektine
Der Geliermechanismus von NV-Pektinen hängt stark von dem Vorhandensein von mehrwertigen Kationen in der Lösung ab. Insbesondere mit Ca2+-lonen bilden Pektine sogenannte heteropolare Hauptvalenzgele. Den zugrunde liegenden Geliervorgang bezeichnet man daher auch als Ca2+- Mechanismus. Die Haftzonen zwischen zwei nebeneinander liegenden Kettenmolekülen werden dadurch gebildet. daß Ca2+-lonen enge Bindungen mit den Carboxyl- und Hydroxyl-Gruppen eingehen, In Abhängigkeit vom pH- Wert sind die die Carboxyl-Gruppen zudem noch teilweise deprotoniert. so daß
die resultierenden Bindungen einen hohen heteropolaren Anteil haben. Wichtig dabei ist. daß sich die beteiligten Ketten zick-ackförmig gegenüber liegen. Man spricht daher auch von einer .Elerschachtelstruktur" mit den Ca2+-lonen als Eiern.
Abb. 15: Haftzonen bei NV-Pektinen durch Ca2+-lonen-Bindung
Für das Zustandekommen dieser Bindungen sind Zucker und Säure nicht so wichtig. Die Gelierfähigkeit von NV-Pektinen ist daher relativ unabhängig von bestimmten pH-Werten. Sie können in einem pH-Bereich von 2.5-7 bei jeder Zuckerkonzentration bis zu etwa 85 % Trockensubstanz Gele bilden. Es muß aber eine ausreichende Menge an Ca2+-lonen zu Verfügung stehen.
Durchführung:
2 g Pektin wird etwa mit der Hälfte des Zuckers (insgesamt 40 g) trocken vermischt. Anschließend rührt man die Mischung portionsweise in das etwa 80°C heiße Wasser (120 ml) ein. bis das Pektin vollständig gelöst ist. Erst danach wird die Restzuckermenge zugesetzt. Die Temperatur sollte während
dieser Zeit nicht wesentlich unter 80°C abfallen. Mir der Citronensäure (ca.
2 ml) wird anschließend ein pH-Wert von etwa 3,5 eingestellt.
Ungefähr die Hälfte des Modellgelees gießt man in die bereitgestellte Petrischale und in ein Sturzglas. Danach gibt man 1 ml der Calciumchlorid- Lösung zu, rührt kräftig durch und füllt den Modellgelee ebenfalls aus. Die Zugabe und Dosierung der Citronensäure und der Calciumchlorid-Lösung kann recht gut mit Einwegspritzen erfolgen. Mit Hilfe von Lebensmittelfarben (z.B.
Ostereierfarben) können die Modellgelees eingefärbt werden.
Chemikalien: NV-Pektin (z.B. Pektintyp .Classic AF 703" der Fa.
Herbstreith& Fox KG, Neuenbürg), Zucker, Citronensäure(w = 0,5), Calciumchlorid-Lsg.
(60 mg/mi), Stativmaterial
Materialien: Magnetrührer mit Kontaktthermometer, Rührfisch, Becherglas (250mi), Spatel, 2 Uhrgläser oder 2 Petri- schalen, 2 Sturzgläser, Einwegspritzen
Auswertung:
Nach dem Ausgießen der Geleeproben dauert es einige Minuten, bis die vollständige Gelierung einsetzt. Der Gelierprozeß ist temperaturabhängig.
Beim Abkühlen nimmt die Eigenbewegung der Moleküle ab, wodurch ihre Neigung steigt, sich zu einem Gelnetzwerk zu vereinigen. Während der Abkühlphase wird die kritische Temperatur erreicht, bei aer die Gelierung einsetzt.
Der Ansatz ohne Ca2+-lonen ist lediglich hochviskos und geliert auch nach längerer Zeit nicht. Man kann das leicht demonstrieren, in dem man die beiden Uhrgläser senkrecht hält.
Bei einem Überschuß oder hohen Konzentrationen von Ca2+-lonen und relativ hohen pH-Werten kann es zu Ausflockung von Ca-Pektinat kommen.
Um das zu vermeiden können Puffersalze (Citrat, Tatrat) zugesetzt werden,
weiche die Ca2+-lonen nur relativ langsam freisetzen und auf diese Weise das Zusammenwirken von Pektin und Ca2+-lonen steuern.
Abb. 16: Geliermechanismus von NV-Pektinen
~~~~.~'-./ ~
~---
V~ • • v~ • •
VERSUCH 6b: Gelierverhalten hochveresterter Pektine
Im Unterschied zu den NV-Pektinen bilden die HV-Pektine sogenannte Nebenvalenzgele. bei denen die Bindung· in den Haftzonen durch Wasserstoffbrücken erfolgt. In diesem System ist der Zusatz von Wasser und Säure notwendig. Daher spricht man bei der Gelierung von HV-Pektinen von einem Zucker-Säure-Mechanismus.
Abb. 17:Gelnetz aus HV-Pektin (Kettenassoziation durch H-Brücken)
0°0°0°-
6 0I CHI'0 0 - HI0°0°6
0 -Neigung zu Polymer-Wasser Bindungen kleiner und die Neigung zu Polymer-
....--....,
Polymer Bindungen entsprechend größer wird. Neben dem Zucker bewirken auch andere lösliche Substanzen eine Dehydratisierung der in Lösung befindlichen Pektinmoleküle. Bei Fruchtzubereitungen trägt maßgeblich auch der Fruchtanteil zum Trockensubstanzgehalt der Lösung bei. Die zugesetzte Säure drängt die Dissoziation der freien Carboxyl-Gruppen zurück und vermindert dadurch die elektrostatische Abstoßung der Ketten.
Allerdings gibt es für jede Zuckerkonzentration und Pektintype nur einen begrenzten pH-Bereich. bei dem die Gelierung optimal verläuft. Jede Abweichung vom erforderlichen Wert hat einen negativen EinflUß auf Festigkeit. Konsistenz und Syneräseneigung. Unter Synärese versteht man das
Ausbluten eines Gelees bei unzureichender Gelierung beispielsweise bei zu niedrigem pH-Wert.
Zu Einstellung eines für den jeweiligen Pektintype optimalen pH-Bereichs verwendet man in der Lebensmitteltechnologie Genußsäuren (Citronensäure, Essigsäure, u.a.).
Durchführung:
Chemikalien: HV-Pektin (z.B. Pektintyp .Classlc CF 201" der Fa.
Herbstreith &Fox KG, Neuenbürg), Zucker, Citronensäure (w = 0,5), Stativmaterial
Materialien: Magnetrührer mit Kontaktthermometer, Rührfisch, Becherglas (250mi), Spatel, Uhrglas oder Petrischale, Sturzglasr, Einwegspritze
Sonstiges: Apfelsaft (klar)
Die Zubereitung des Modellgelees erfolgt wie in Versuch 6a. Statt Wasser verwendet man bei diesem Ansatz käuflichen Apfelsaft, 150 g Zucker und 2 9 Pektin. Für die Einstellung des pH-Werts auf 3 benötigt man in Abhängigkeit vom jeweiligen Apfelsaft rund 8 ml Citronensäure. Außerdem sollte der Modellgelee vor dem Ausfüllen kurz aufgekocht werden.
Auswertung:
Bei" dem verwendeten HV-Pektin erfolgt die Gelierung im Gegensatz zu dem verwendeten NV-Pektin bereits nach wenigen Augenblicken. Für den Geliervorgang nach dem Zucker-Säure-Mechanismus sind keine Ca2+-lonen notwendig. In gewissen Grenzen können sich Zucker und Säure ersetzen.
Geringere Zuckergehalte erfordern tiefere pH-Werte; höhere pH-Werte sind möglich bei höherem Zuckergehalt. Die in der Versuchsvorschrift genannten Zucker- und Säuremengen können deshalb in engen Grenzen variiert werden.

![Tab. 3: Pektingehalte verschiedener Pflanzenmaterialien Pflanzenmaterial Pektin-Gehalt [%] (Frischgewicht) Apfel 0,5-1,6 Tomaten 0,2-0 ,5 Grapefru it 1,6-4 ,5 Johannis-Beeren 0 ,9-1 .5 Rohstoff Pektin-Gehalt [%] (Trockenmasse) Apfeltrester 15 Zuckerrübensc](https://thumb-eu.123doks.com/thumbv2/1library_info/3941414.1533360/28.892.125.790.763.1157/pektingehalte-verschiedener-pflanzenmaterialien-pflanzenmaterial-frischgewicht-trockenmasse-apfeltrester-zuckerrübensc.webp)