Physikalisches Anf¨ angerpraktikum der Universit¨ at Heidelberg - APL II Versuch 252 Aktivierung von Indium und Silber
Versuch 252
Aktivierung von Indium und von Silber mit thermischen Neutronen
Abbildung 1: Oben: Versuchsaufbau. Unten: Neutronenquelle.
I Messaufbau
• Geiger-M¨ uller Z¨ahlrohr mit Betriebsger¨at
• Externer Impulsz¨ahler
• PC mit Drucker
• Neutronenquelle
• Pr¨aparatehalterung
• Indium- und Silberbleche
II Vorbereitung
Bereiten Sie sich auf die Beantwortung von Fragen zu folgenden Themen vor:
Radioaktiver Zerfall, Zerfallsarten, Nuklide, Geiger-M¨ uller-Z¨ahlrohr.
Verst¨andnisfragen:
1. Was ist ein Neutron?
2. Was passiert, wenn ein Atomkern ein langsames Neutron einf¨angt?
3. Wie ist der Zusammenhang zwischen Aktivierung und Zerfall?
4. Was ist die Halbwertszeit, wie kann man sie messen?
5. Wie sieht das Spektrum eines β-Strahlers aus? Warum handelt es sich um ein kontinuierliches Spektrum?
III Aufgaben
1. Bestimmung der Halbwertszeit von
116In.
2. Bestimmung der Halbwertszeiten von
108Ag und
110Ag
c Dr. J.Wagner - Physikalisches Anf¨angerpraktikum - V. 1.0 Stand 01/2010
1
Physikalisches Anf¨ angerpraktikum der Universit¨ at Heidelberg - APL II Versuch 252 Aktivierung von Indium und Silber
IV Grundlagen
Zur Herstellung einer radioaktiven Quelle werden stabile Isotope durch Kern- reaktionen aktiviert. Besonders geeignet hierf¨ ur sind Neutronen, da diese nicht der Coulomb-Wechselwirkung ausgesetzt sind und daher vom Kern leicht einge- fangen werden k¨onnen. In diesem Versuch werden die Isotope
115In bzw.
107Ag /
109Ag mit Hilfe thermischer Neutronen aktiviert.
Die Neutronenquelle besteht aus einem Pr¨aparat, das Berylliumsp¨ane und einen α-Strahler (
241Am) enth¨alt. Durch die Kernreaktion
9
Be + α →
12C + n
entstehen Neutronen mit einer Energie von 1 - 10 MeV. Diese schnellen Neutro- nen werden in dem die Neutronenquelle umgebenden Paraffinblock durch ela- stische St¨oße mit den Wasserstoffkernen abgebremst, bis sie nahezu thermische Energie erreicht haben. St¨oße gegen die Kohlenstoffkerne bremsen die Neutro- nen nur wenig ab. Bei einem elastischen Stoß gegen eine gleich schwere Masse (n¨amlich gegen ein Proton) verliert dagegen das Neutron im Mittel die H¨alfte der Energie. Viele Atomkerne haben einen großen Wirkungsquerschnitt f¨ ur den Einfang langsamer Neutronen. Dabei entsteht ein Isotop des bestrahlten Ele- ments mit einer um eins erh¨ohten Massenzahl. Wenn dieser Kern radioaktiv ist, stellt die Aktivierung durch langsame Neutronen die bequemste M¨oglichkeit zur Erzeugung dieses radioaktiven Isotops dar. Bei Bestrahlung von Indium wird aus dem stabilen Isotop
115In der β-Strahler
116In gebildet. Allerdings werden dabei zwei sogenannte Isomere erzeugt. Dabei handelt es sich um Nuklide, die jeweils die gleiche Anzahl von Neutronen und Protonen besitzen, sich aber in ei- nem unterschiedlichen Energiezustand befinden. Zum einen wird
116In gebildet welches sich im Grundzustand befindet, zum anderen der metastabile Zustand
116m
In. Beide Nuklide sind β
−-Strahler die mit unterschiedlichen Halbwerts- zeiten in das stabile Isotop
116Sn zerfallen. Die Halbwertszeiten finden Sie in der Nuklidkarte im Anhang.
Bei der Aktivierung wird pro Sekunde eine bestimmte Zahl von radioaktiven Kernen erzeugt. Die Zahl der pro Sekunde zerfallenden Kerne ist aber der An- zahl der jeweils vorhandenen radioaktiven Kerne proportional (Zerfallsgesetz).
Daher nimmt die Aktivit¨at A (d.h. die Zahl der Zerf¨alle pro Sekunde) als Funk- tion der Bestrahlungsdauer t nach dem Gesetz
A(t) = A
∞(1 − exp{−λt}) (1)
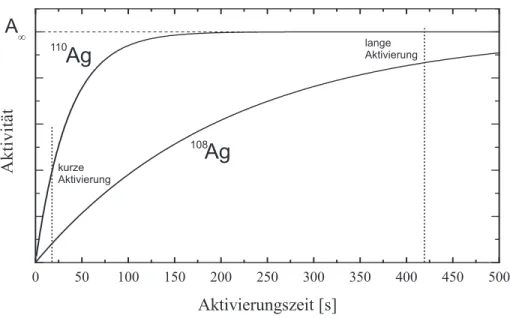
kurze Aktivierung
lange Aktivierung 110
Ag
108
Ag
Abbildung 2: Aktivit¨at von
108Ag und
110Ag bei unterschiedlichen Aktivierungs- zeiten. Es wurde angenommen, dass der Wirkungsquerschnitt bei beiden Isoto- pen identisch ist.
zu, bis ein Gleichgewicht eintritt, bei dem pro Sekunde gleichviel Kerne des ra- dioaktiven Isotops neu gebildet werden wie pro Sekunde zerfallen. Nach Ende der Aktivierung tritt dann nur noch der Zerfall nach dem radioaktiven Zerfalls- gesetz
A(t) = A
0exp (−λt) (2)
auf. F¨ ur die Halbwertszeit gilt
T
1/2= ln 2
λ . (3)
Da nat¨urliches Silber aus 51%
107Ag und 49%
109Ag besteht, werden bei der Aktivierung zwei unterschiedliche Isotope erzeugt. Es entstehen die radioakti- ven Silberisotope
108Ag und
110Ag. Sie zerfallen durch β-Zerfall in
108Cd und
110
Cd. Da die Halbwertszeiten dieser Silber-Isotope sich um etwa einen Fak- tor 6 unterscheiden, kann durch unterschiedlich lange Aktivierungszeiten das Isotopenverh¨altnis variiert werden. Wird nur kurz aktiviert (20 s), entsteht vor c Dr. J.Wagner - Physikalisches Anf¨angerpraktikum - V. 1.0 Stand 01/2010
2
Physikalisches Anf¨ angerpraktikum der Universit¨ at Heidelberg - APL II Versuch 252 Aktivierung von Indium und Silber
allem
110Ag. Mit zunehmender Aktivierungszeit wird vermehrt
108Ag erzeugt w¨ahrend
110Ag in S¨attigung geht (Abbildung 2).
V Durchf¨ uhrung des Versuchs
1. Halbwertszeit von Silber
Stellen Sie am Betriebsger¨at die Z¨ahlrohrspannung zwischen 500 V bis 550 V ein. Bestimmen Sie zun¨achst den Untergrund. Entfernen Sie alle Quellen aus dem Raum. Stellen Sie im Messprogramm zerfall.exe die Torzeit des Z¨ahlers auf 10 Sekunden und messen Sie ¨ uber einen Zeitraum von 100 s den Untergrund. Speichern Sie die Messdaten unter einem ge- eigneten Namen, z.B. UntergrundAgxx.dat wobei Sie f¨ ur xx Ihre Initialen w¨ahlen.
F¨ ur die Silbermessung wird wieder eine Torzeit von 10 Sekunden einge- stellt. Lassen Sie sich vom Assistenten zeigen, wie man die Tr¨ager mit den Silberblechen (blaues Tr¨agermaterial) in die Neutronenquelle einlegt.
Das Silberblech wird mindestens 7 Minuten lang aktiviert und dann so schnell wie m¨ oglich vor das Z¨ahlrohr gebracht. Stecken Sie das Pr¨apa- rat mit der Silberseite zum Z¨ahlrohr hin in die vorgesehene Aussparung und fixieren Sie es mit dem Aluminiumblech. Starten Sie sofort das Mes- sprogramm durch einen Mausklick auf den Pfeil im linken oberen Bereich des Programmfensters. Die gesamte Messzeit sollte 400 Sekunden betra- gen. Nachdem das Silberbleche noch ca. 5 Minuten nach Ende der Mes- szeit außerhalb der Quelle war, d.h. die Aktivit¨at abgeklungen ist, wird die Messung dreimal wiederholt. Speichern Sie jedes Mal die Messdaten und drucken Sie das Protokoll aus.
2. Halbwertszeit von Indium
Messen Sie ¨uber einen Zeitraum von zweimal 4 Minuten ohne Pr¨aparat den Nulleffekt. Sie k¨onnen dazu die Start- Stopp- Automatik des Betriebs- ger¨ates des Z¨ahlrohrs verwenden. Achten Sie wieder darauf, dass sich keine radioaktiven Quellen im Raum befinden. Speichern Sie die Daten unter ei- nem geeigneten Namen. Stellen Sie anschließend im Messprogramm das Messintervall auf 120 s und stecken Sie das aktivierte Indium- Pr¨aparat (gr¨ unes Tr¨agermaterial) in die Halterung. Die Messung sollte ¨ uber einen
Zeitraum von 120 Minuten gehen. Speichern Sie am Ende der Messung die Daten und drucken Sie das Protokoll aus. W¨ahrend die Indiummessung l¨auft, k¨onnen Sie bereits mit der Auswertung der Silbermessung beginnen.
VI Auswertung
F¨ uhren Sie die Auswertung gem¨aß der separat am Praktikumsplatz ausliegen- den Anleitung durch.
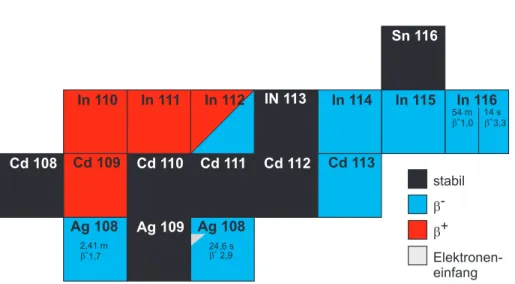
VII Anhang
In 116
54 mb-1,0 14 s b- 3,3
Sn 116
In 115 In 114
IN 113 In 111
In 110
Cd 109 Cd 110 Cd 111 Cd 112 Cd 113
Ag 108
2,41 m b-1,7
Ag 108
24,6 s b- 2,9