28.11.12 Robbin Schnieders
Abb.1: Siedediagramm einer Flüssigkeit mit Siedepunktsmaximum
Azeotrope Mischungen
Definition:
- Als Azeotrope bezeichnet man Stoffgemische, welche sich durch Destillation nicht weiter auftrennen lassen
verhalten sich in der Hinsicht wie Reinstoffe
- Man unterscheidet zwischen Homogenen Azeotropen (Komponenten sind
mischbar) und Heterogenen Azeotropen (Komponenten sind nicht immer mischbar)
Azeotropentypen:
1. mit Siedepunktsmaximum:
- Die intermolekularen Wechselwirkungen zwischen zwei fremdartigen Teilchen A-B ist größer als in den Reinstoffen A-A oder B-B.
Dampfdruckerniedrigung und Siedepunkterhöhung - Die Mischungsenthalpie ΔMH ist kleiner null
- Es kommt oft zu Volumenkontraktion.
- Beispiel: Chloroform/Aceton
Liegt ein Stoffgemisch der Zusammensetzung x1 vor, welches zum Sieden erhitzt wird, so besitzt der Dampf die Zusammensetzung x1‘. Es befindet sich im Dampf also wesentlich mehr
Stoff Y als Stoff X (imVergleich mit x1).
Die zurückbleibende Flüssigkeit weist eine Abnahme von Stoff Y auf und hat nun die
Zusammensetzung x2. So näher man sich immer weiter dem Höhepunkt der
Kurve, dem azeotropenPunkt, an. Hier haben Flüssigkeits- und Dampfphase die selbe Zusammensetzung, wodurch keine weitere Stofftrennung auf diesem Wege erfolgen kann.
2. mit Siedepunktsminimum:
- Die intermolekularen Wechselwirkungen zwischen A und B sind kleiner als die der Reinstoffe A-A oder B-B.
Dampfdruckerhöhung und Siedepunkterniedrigung - ΔMH > 0
- oft Vergrößerung des Volumens - Beispiel: Dioxan/Wasser
28.11.12 Robbin Schnieders
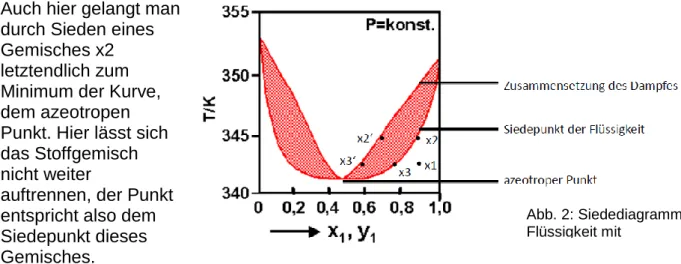
Auch hier gelangt man durch Sieden eines Gemisches x2 letztendlich zum Minimum der Kurve, dem azeotropen Punkt. Hier lässt sich das Stoffgemisch nicht weiter
auftrennen, der Punkt entspricht also dem Siedepunkt dieses Gemisches.
Trennung von Azeotropen:
Azeotrope lassen sich aufgrund oft unterschiedlicher physikalischer Eigenschaften vielseitig voneinander trennen.
So lassen sie sich oft durch Auskristallisieren einer Komponente, Dampfpermeation bzw. Pervaporation (Trennung des Dampfes bzw. der Flüssigkeit durch Membran) auftrennen. Bei Azeotropen, die Wasser als Komponente aufweisen, können verschiedene Trocknungsmittel eingesetzt werden.
Anwendung von Azeotropen Mischungen:
Azeotrope können als Schleppmittel bei der Stofftrennung eingesetzt werden. Dies wird oft bei Azeotropen mit Wasser angewendet.
Bsp.: Trennung von Essigsäure/Wassergemischen:
Hierbei handelt es sich nicht um ein Azeotrop, allerdings wäre die Auftrennung durch Destillation, aufgrund ähnlicher Siedepunkte (118°C/100°C), nicht sehr effektiv.
Durch Zugabe von Ethylacetat wird die Trennung erleichtert, da Ethylacetat mit Wasser ein niedrigsiedendes Azeotrop bildet (70°C). So kann das Gemisch sehr viel leichter durch Destillation getrennt werden.
Abb. 2: Siedediagramm einer Flüssigkeit mit
Siedepunktminimum