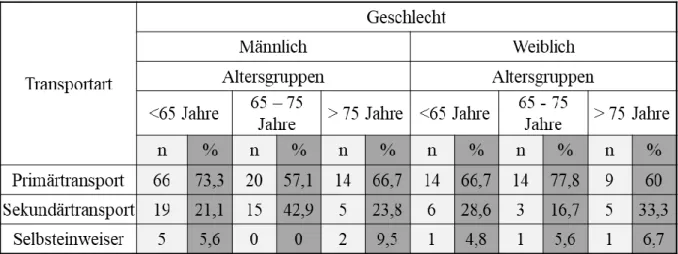
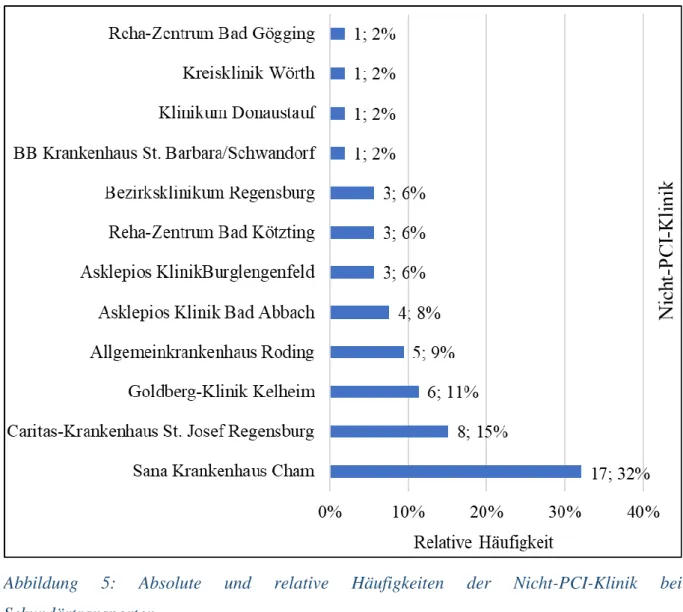
Ischaemic Time bei Patienten mit ST-Hebungsmyokardinfarkt: Eine Analyse der Regensburger STEMI-Datenbank
Volltext
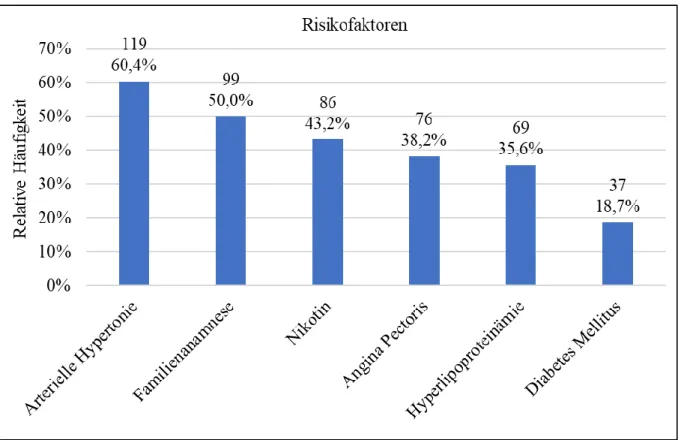
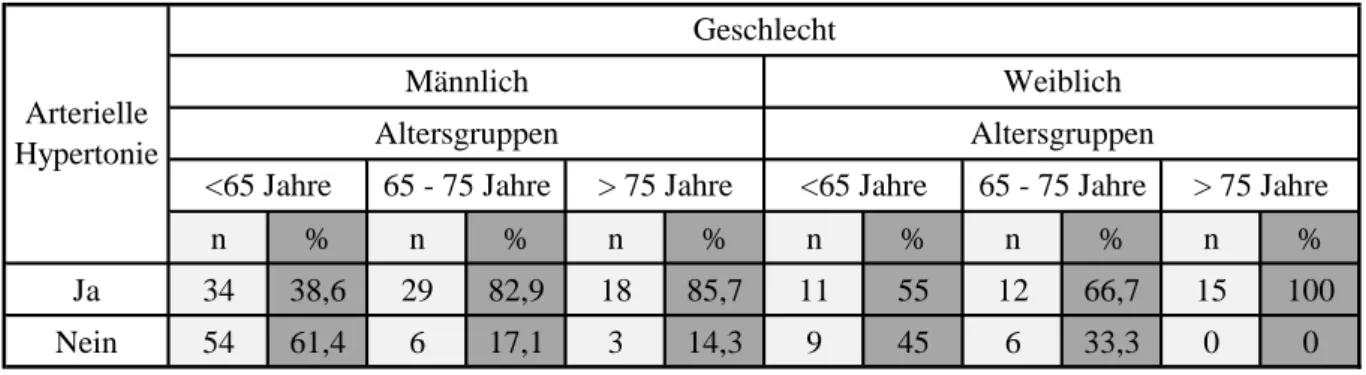
Abbildung
ÄHNLICHE DOKUMENTE
Später stellte sich heraus, dass auf der Inten- sivstation bereits mit dem Patienten über eine mögliche Reanimation ge - sprochen wurde und dieser ausschließ- lich eine
IMC: intermediate care unit; HDU: high dependency unit; TAA: Tachyarrhythmia absoluta; * MAC- Score: Major adverse events and complications score: 1 Punkt für jede der
Zwischen der dynamischen Leberfunktion und der Beatmungsdauer einerseits sowie dem neurologischen Outcome andererseits zeigt sich keine statistisch signifikante
Dabei sollte die Frage beantwortet werden, ob ältere, multimorbide Patienten mit Urosepsis bei Urolithiasis von einer Steintherapie profitieren und somit die
Wie verändert sich die körperliche Belastbarkeit (PeakVO2) und die Lebensqualität (Short- Form-Health-Survey, SF-36) nach 3 Monaten körperlichem Training bei Patienten
(2012) fest, dass Patienten, die eine ischämische Cholangiopathie mit sekundär sklerosierender Cholangitis während des Intensivaufenthaltes entwickelten signifikant
Wie bereits im Absatz oberhalb erwähnt werden auch in dieser Studie zur Lebensqualität nach Operation an der Aorta ascendens Patienten mit verschiedenen
konnten in ihrer, erst kürzlich erschienen, prospektiven Studie an 1235 Patienten deutlich machen, dass eine eingeschränkte Nierenfunktion mit einer geringen eGFR sowie