Versuch 34 Spektralfotometrie
Photoelement
KMnO - Küvetten4 Spektrallampe
Glühlampe
Amperemeter
Abbildung 1:Aufbau des Versuchs Spektralfotometrie.
I Messaufbau
• Spektralfotometrische Messanordnung auf einer Grundplatte, bestehend aus: Lichtquelle mit asph¨arischer Kondensorlinse, K¨uvettenbank, Hg- Cd-Spektrallampe mit Netzteil und Einblendspiegel, Monochromator in Littrow-Anordnung mit verschiebbarem Austrittsspalt und Fotoelement Typ BPY 64 in einem Geh¨ause, beleuchtetes Ableselineal mit mm-Teilung, Sehschlitz zur visuellen Beobachtung des Spektrums
• Picoamperemeter zur Fotostrommessung
• Netzversorgung f¨ur die Lampen
S2
L1
Sp1
L3 Pr S
Sp2 S0
Abbildung 2: Strahlengang im Spektrometer. Die Bezeichnungen sind Im Ka- pitel
”Grundlagen“ erl¨autert.
• Je Versuchsaufbau:
1 Satz (5 St¨uck) K¨uvetten mit 0,00005-molaren Kaliumpermanganat- l¨osung (KMnO4), Schichtdicken:l1=1,5 cm,l2=3 cm,l3=6 cm,l4=12 cm, l5=24 cm.
F¨ur alle 5 Aufbauten gemeinsam: Eine 25 ml-B¨urette mit 1/10 ml-Teilung und 2 l Vorratsgef¨aß (VE-Wasser), eine 10 ml-B¨urette mit 1/20 ml-Teilung und 2 l Vorratsgef¨aß (0,001-molare w¨assrige KMnO4-L¨osung)
• Eine offene K¨uvette (rechteckig),l=1,5 cm
• Zur Auswertung einfachlogarithmisches Papier mit 4 Dekaden
II Literatur
• W. Walcher,Praktikum der Physik, B.G.Teubner Stuttgart,
• Standardwerke der Physik: Gerthsen, Bergmann-Sch¨afer, Tipler.
• Homepage des Praktikums:
http://www.physi.uni-heidelberg.de/Einrichtungen/AP/
III Vorbereitung
Bereiten Sie sich auf die Beantwortung von Fragen zu folgenden Themen vor:
Aufbau eines Prismenspektralapparates, Absorption (Extinktion) von Strah-
lung, Lambert-Beersches Gesetz, Absorptionsspektren (Absorption in L¨osun- gen), Fotometrie, Spektralfotometrie, Spektrum eines Temperaturstrahlers, Planck’sches Strahlungsgesetz. Beantworten Sie bei Ihrer Vorbereitung folgen- de Fragen zum Versuch:
1. Was passiert bei der Absorption von Licht durch die KMnO4-Molek¨ule der verwendeten Probel¨osung?
2. Wie weist man Licht m¨oglichst empfindlich nach?
3. Wie h¨angt die Absorption von L¨ange und Konzentration der durchstrahl- ten L¨osung ab. Wie kommt man zu den entsprechenden Formeln?
4. Wie sieht das Spektrum eines Planck’schen Temperaturstrahlers aus? Wie
¨andert sich das Spektrum bei ¨Anderung der Temperatur?
5. Was genau wird auf den Achsen dargestellt, wenn man ein
”Spek- trum“ zeichnet? Nach
”oben“...? Nach
”rechts“...?
IV Aufgabe
• Die Apparatur wird mit Spektrallinien bekannter Wellenl¨ange geeicht.
Zusatzaufgabe:Die
”Apparatebreite“ des Spektrografen wird bestimmt.
• Durch Messung der Absorption von Licht der Wellenl¨ange λ=525 nm als Funktion der Schichtdicke bzw. der Konzentration einer KMnO4-L¨osungen wird der molare Extinktionskoeffizientǫf¨urλ= 525 nm ermittelt.
• Das Absorptionsspektrum von KMnO4 wird im Bereich vonλ= 630 nm bis 490 nm (von gelb bis blau) gemessen.
• Das Emissionsspektrum einer Gl¨uhlampe wird bestimmt unter Verwen- dung der bekannten Empfindlichkeit des Fotoelements.
V Grundlagen
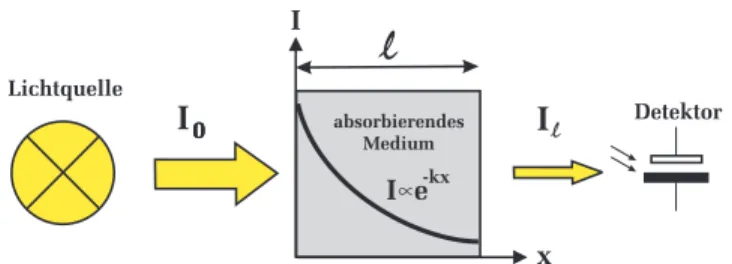
Als Fotometrie bezeichnet man die Konzentrationsbestimmung einer Substanz durch Absorption (bzw. durch Streuung oder Fluoreszenz). Das Prinzip be- ruht auf der Messung der Abschw¨achung der Intensit¨at eines einfallenden Lichtb¨undels durch die in der Messzelle enthaltene Substanz. Das Absorpti-
0
x I
0 I
0 l
l
absorbierendes Medium
I e%
-kx
I
Lichtquelle
Detektor
Abbildung 3:Verdeutlichung des Lambertschen Absorptionsgesetz.
onsgesetz f¨ur Licht lautet in der differentiellen Schreibweise:
dI
I =−kdl. (1) Anschaulich bedeutet dies, dass die relative Intensit¨atsabnahmedI/I bei klei- nen Wegstrecken, der Dicke dl proportional ist. Durch Integration von Glei- chung (1) erh¨alt man die Intensit¨atIdes Lichts nach Durchlaufen der Strecke l im absorbierenden Medium (Lambertsches Absorptionsgesetz):
I=I0e−kl. (2)
Dabei bezeichnetI0die in das Medium eindringende Intensit¨at,ldie L¨ange des Lichtweges im absorbierenden Medium und k die Absorptionskonstante (bzw.
”Extinktionskonstante“, die beiden Bezeichnungen werden in der Literatur ne- beneinander verwendet und sind identisch).
Zur Auswertung von Messungen empfiehlt sich die logarithmische Schreibweise:
ln I I0
=−kl bzw. lnI=−kl+ const mit const = lnI0. (3) Tr¨agt man I gegenl auf halblogarithmischem Papier auf, so ergibt sich eine Gerade. In der Praxis verwendet man dekadische Logarithmen. Gleichung (3) hat dann die Gestalt
logI=−k′l+ const′ mit k′ = log ek= 0,434k. (4) k′ heißt”dekadischer oder Bunsenscher Absorptionskoeffizient“.
F¨ur verd¨unnte L¨osungen gilt im allgemeinen, dass die Absorptionskonstantek′ der Konzentrationc proportional ist (Beersches Gesetz):
k′ =ǫc. (5) Man nennt ǫden molaren Extinktionskoeffizienten oder kurz Molarextinktion, wobeicin mol/l oder mol/cm3anzugeben ist. Nach dem Beerschen Gesetz istǫ von der Konzentrationcder L¨osung unabh¨angig, d.h.ǫist eine Stoffkonstante.
Bei hohen Konzentrationen k¨onnen Abweichungen vom Beerschen Gesetz auf- treten. Ein Beispiel bietet die CuCl2-L¨osung, bei der beim ¨Ubergang von verd¨unnter zu konzentrierter L¨osung eine Gleichgewichtsverschiebung bei der Komplexbildung auftritt, gem¨aß
verd¨unnte L¨osung konzentrierte L¨osung Cu H2O
4
++
+ 2Cl− ⇔ 1
2
Cu+++
CuCl4−−
+ 4H2O.
Eine Erh¨ohung der Konzentration bedeutet also in diesem Fall nicht einfach eine Vergr¨oßerung der Zahl der an der Absorption beteiligten Ionen (wie im G¨ultigkeitsbereich des Beerschen Gesetzes), sondern Neubildung von Ionen an- derer Art, die i.a. auch ein anderes Absorptionsverhalten zeigen.
Die Konzentrationsabh¨angigkeit der Absorption bietet auch eine einfache M¨oglichkeit, den zeitlichen Verlauf von chemischen Reaktionen (Auftauchen bzw. Verschwinden von Ionen) zu verfolgen.
k′ bzw. ǫ h¨angen von der Wellenl¨ange ab. Die Funktionen k′(λ) bzw. ǫ(λ) beschreiben das Absorptionsspektrum der L¨osung. Unter einem Spektrum ver- steht man ein Diagramm, in dem die Intensit¨at eines Strahlers bzw. eine ihr proportionale Gr¨oße (hier der Fotostrom) ¨uber der Wellenl¨ange aufgetragen ist. Die Stellen maximaler Absorption sind die Schwerpunkte von sog. Absorp- tionsbanden, die f¨ur jedes Ion charakteristisch sind und zu dessen Nachweis dienen k¨onnen. Zusammenfassend l¨asst sich mit den eingef¨uhrten Gr¨oßen das Absorptionsgesetz folgendermaßen schreiben:
I=I010−k′l=I010−ǫcl (6)
Es gibt zwei Methoden k′ undǫzu messen:
1. Man misst die Intensit¨at des austretenden Lichts als Funktion der L¨ange der durchstrahlten Fl¨ussigkeit bei konstant gehaltener Konzentration. Auf- tragung von logIgegenlergibtk′. Bei bekannter Konzentration errechnet sich darausǫ.
2. Man h¨alt die Schichtdicke l konstant und variiert die Konzentrationc in definierter Weise. Auftragen von logIgegencergibt zun¨achst das Produkt ǫlund damit bei bekannteml wiederǫ.
L5
L2 L3
Pr S2
Sp1
L1
Sp2
S L
D
Abbildung 4:Strahlengang des Spektralfotometers.
Zum Aufbau der Apparatur: Der Aufbau des Spektrographen gleicht im Prinzip dem des Prismenspektrometers (Versuch 33). Jedoch ist er diesem ge- gen¨uber in zweierlei Hinsicht vollkommener. Einmal wird durch einen Spiegel hinter dem Prisma daf¨ur gesorgt, dass dieses vom Licht zweimal durchlaufen wird, wodurch die Aufl¨osung verdoppelt wird. Zum Zweiten erreicht man durch Einf¨ugen einer weiteren Linse (Feldlinse L2 in Abbildung 3 und 4) in den Strah- lengang, dass von dem den Spalt Sp1 durchtretenden Licht nichts verloren geht, was große Intensit¨aten am Bildort bzw. auf der Fotoelement bedeutet. (Inten- sit¨at = Energiezufuhr pro Zeit und Fl¨ache, hier also proportional der Zahl der pro Zeit und Fl¨ache einfallenden Photonen.) Das ist f¨ur die Absorptionsmessun- gen wichtig, weil die Absorption (R¨uckgang des Fotostromes) umso deutlicher wird, je gr¨oßer die Prim¨arintensit¨at ist.
Der Strahlengang der Apperatur ist in den Abbildungen 4 und 5 dargestellt.
Ein genaues Verst¨andnis wird nicht verlangt. Wichtig ist aber, dass Sie den Aufbau des gew¨ohnlichen Spektralapparates (Versuch 33) verstanden haben.
L2
Sp1
L1
L3
Pr1
L5
S0
Sp2
Pr1
L‘3
‘
Abbildung 5:Vereinfachte Darstellung des Strahlengangs.
Den tats¨achlichen Strahlengang in der verwendeten Apparatur zeigt Abbil- dung 4. Um ihn ¨ubersichtlicher zu machen, wurde in Abbildung 5 die in Wirk- lichkeit auftretende 90◦-Abwinkelung des Strahlengangs an dem Prisma S2 nicht gezeichnet und die Spiegelung am Littrow-Spiegel S3 zur¨uck ¨uber das Prisma Pr1 etc. ersetzt durch den durchlaufenden Strahlengang ¨uber Pr2 etc.
Die Linse L′3 (= Spiegelbild der Kollimatorlinse L3) entspricht dem Fernrohr- objektiv beim Spektrometer. Die Absorptionsk¨uvetten werden zwischen L1 und Sp1 gebracht. Die Linsen L2 und L5 werden ebenso wie die Spalte Sp1 und Sp2 durch die Linsenkombination L3 und L4 ineinander abgebildet; Sie beeinflussen den Abbildungsstrahlengang Sp1 Sp2 nicht. (L2 und L5 liegen ja in der Ebene von Sp1 und Sp2, also von”Gegenstand“ und”Bild“). L2 bildet L1 in S (bzw.
Pr1) ab und L5 bildet S (bzw. Pr′1) auf das Fotoelement So ab. Insgesamt wird
also L1 auf So abgebildet.
Die eingezeichneten Strahlen k¨onnen entweder als Grenzen eines vom Mittel- punkt von L1 ausgehenden Lichtb¨undels aufgefasst werden, dessen Achse mit der optischen Achse der Anordnung zusammenf¨allt oder aber als die Achsen zweier vom oberen bzw. unteren Ende der Gl¨uhwendel L ausgehenden B¨undel.
Das Licht der zur Eichung des Monochromators dienenden Spektrallampe wird uber einen in Abbildung 3 nicht eingezeichneten Spiegel S1 zwischen L1 und¨ Sp1 in den Strahlengang eingeblendet.
Jeder Spektralapparat hat eine
”Apparatebreite“. Sie charakterisiert die F¨ahig- keit des Spektrometers, zwei Linien verschiedener Wellenl¨angen voneinander zu trennen (noch
”aufzul¨osen“) und ist im wesentlichen durch die Spaltbreite Sp1 gegeben. Aus Abbildung 5 ist ersichtlich, dass mit L3 und L′3 gerade eine 1:1 - Abbildung des Spaltes Sp1 auf sein Bild Sp2 erreicht wird. Das heißt aber, dass die Wellenl¨angendifferenz zweier benachbarter Linien umso kleiner sein darf, je schmaler der Spalt ist. Gleichzeitig geht mit Verkleinerung der Spaltbreite die Lichtintensit¨at zur¨uck. Eine hohe Aufl¨osung geht also stets auf Kosten der hinter dem Spektralapparat zur Verf¨ugung stehenden Intensit¨at.
Die prinzipielle Grenze der Aufl¨osung wird durch Beugungserscheinungen gesetzt. Dies wird im Versuch 31 und 33 diskutiert.
Technische Daten: f(L1)= 4,1 cm, f(L2)= 20 cm, f(L3)= f(L′3)= 60 cm, f(L5)= 10 cm; Prisma: Flintglas F2; Breite des Eintrittsspalts und der Pro- jektion des Austrittsspalts: 0,6 mm.
VI Durchf¨uhrung des Versuchs
Schauen Sie w¨ahrend der Durchf¨uhrung zu jeder Versuchsaufgabe auch im Ka- pitel Auswertung nach. Einige Diagramme sind sofort w¨ahrend der Messung zu zeichnen. Daf¨ur brauchen Sie drei Blatt gew¨ohnliches Millimeterpapier und ein Blatt einfach logarithmisches Papier (Ordinatenbereich vier Zehnerpotenzen).
1. Skizzieren Sie den Versuchsaufbau.
2. Wellenl¨angen-Eichung
Hierzu wird die Hg-Cd-Spektrallampe verwendet, das Gr¨unfilter ist aus dem Strahlengang zu klappen. Schalten Sie die Lampe ein und stecken Sie den Einblendspiegel auf. (Nach etwa 5 bis 10 Minuten gibt die Lampe die volle Intensit¨at ab.) Sie sehen das Spektrum durch einen Schlitz im
Monochromatorkasten. Mit den st¨arksten Linien wird die Eichkurve des Monochromators aufgenommen und sofort gezeichnet (Bereich 400 nm - 1100 nm). Die Wellenl¨ange entnehmen Sie der Tabelle. Um die Extrapo- lation ins Infrarote zu erleichtern, soll in der Eichkurve die Spaltstellung uber 1/λ¨ aufgetragen werden (statt ¨uber λ). Sie k¨onnen sich auf die rote Linie und 6 bis 7 der
”stromstarken“ Linien beschr¨anken. Der Fotostrom ist in der letzten Spalte der Tabelle eingetragen (Iph). Die Grobeinstel- lung des Spalts auf die Linien erfolgt visuell, die Feineinstellung mittels des Fotostrom-Maximums. Notieren Sie auch die Str¨ome. Versuchen Sie, die (unsichtbaren) Linien bei 690,7 nm , 708,2 nm und 1014,0 nm mit dem Detektor zu finden. (1/λ= 1,448µm−1, 1,41µm−1, 0,986µm−1). Zeich- nen Sie zun¨achst, um einen Anhaltspunkt zu haben, mit den sichtbaren Linien eine vorl¨aufige Eichkurve.
λ[nm] Element λ−1 [µm−1] Farbe Intensit¨at Iph[b.E.]
643,8 Cd 1,553 rot schwach 10
578 Hg 1,73 gelb stark 20
546,1 Hg 1,831 gelbgr¨un stark 40
508,6 Cd 1,966 gr¨un mittel 15
491,6 Hg 2,034 blaugr¨un sehr schwach 0.3
480 Cd 2,083 blau mittel 10
467,8 Cd 2,138 blau schwach 5
435,84 Hg 2,294 blauviolett stark 13
407,8 Hg 2,452 (violett) unsichtbar 0.3
404,7 Hg 2,471 (violett) unsichtbar 3.0
3. Zusatzaufgabe f¨ur Physiker: Bestimmen sie an einer starken Linie das Ap- parateprofil (Linienbreite). W¨ahlen Sie f¨ur die Schrittweite 0,5 mm. Tragen Sie Ihre Messwerte sofort in ein Diagramm ein. Die Apparatebreite ist in nm anzugeben (Umrechnung mit Hilfe der Eichkurve).
Achtung: Bitte schalten Sie nach vollendeter Eichung bzw. nach Be- stimmung des Apparateprofils die Spektrallampe aus. (Vor erneutem Einschalten muss die Lampe etwa 5 Minuten abk¨uhlen, sonst z¨undet sie nicht.)
Um den Einfluss von Streulicht zu unterdr¨ucken, wird bei den Messungen VI.4, VI.5 und VI.6 ein Gr¨unfilter eingeschwenkt.
Damit keine unn¨otigen Wartezeiten an den B¨uretten entstehen, kann die Rei- henfolge der Messungen VI.4 und VI.5 vertauscht werden.
Uberzeugen Sie sich vor Beginn der Messungen, dass die Gl¨¨ uhlampenwendel so scharf wie m¨oglich auf den Eintrittsspalt abgebildet ist. Pr¨ufen Sie mit ei- nem weißen Papier nach, ob das nahe der Kollimatorlinse entstehende Bild der Kondensor¨offnung gleichm¨aßig weiß ist. (Hierzu ist der Deckel des Monochro- matorkastens zu ¨offnen.) Die Gl¨uhlampe l¨asst sich mit den drei Stellschrauben am Geh¨ause justieren.
4. Absorption einer KMnO4- L¨osung als Funktion der Schichtdicke:
Lambertsches Absorptionsgesetz.
Als Lichtquelle benutzen Sie die Gl¨uhlampe. Stellen Sie den Austrittspalt fest auf die Wellenl¨angeλ=525 nm ein und nehmen Sie die durchgelassene Intensit¨at als Funktion der K¨uvettenl¨ange vonl1=1,5 cm bisl5=24 cm auf.
Die Messwerte sind sofort auf halblogarithmischem Papier einzuzeichnen.
Dunkelstrom: An dieser Stelle kann der
”Dunkelstrom“ den ein Foto- element auch ohne Lichteinfall liefert, wichtig werden. Bestimmen Sie ihn durch Abdecken des Eintrittsspalts und ziehen Sie ihn bei intensit¨atsschwa- chen Messungen vom gesamten Fotostrom ab. Wiederholen Sie noch im weiteren Verlauf gelegentlich die Dunkelstrommessung, insbesondere am Schluss des Versuchs.
5. Absorption einer KMnO4- L¨osung als Funktion der Konzentra- tion: Beersches Gesetz.
Einstellung auf λ=525 nm wie unter VI.4. Bei konstanter Schichtdicke l wird die Konzentration c schrittweise erh¨oht (z.B. jeweils um den Fak- tor 2) und tr¨agt die durchgelassene Intensit¨at logarithmisch gegen c auf.
Als erstes wird eine sogenannte Nullmessung mit reinem VE-Wasser1ge- macht. Geht man von einem abgemessenen Volumen V0 reinen Wassers aus und gibt nach und nach die VoluminaV1, V2, ...einer KMnO4-L¨osung bekannter Konzentration ˜c zu (in der B¨urette betr¨agt die Konzentration
1VE-Wasser: Voll Entsalzenes Wasser.
˜
c=10−3mol/l), so erh¨alt man die Konzentrationen c0= ˜c 0
V0
= 0, c1= ˜c V1
V0+V1
, c2= ˜c V1+V2
V0+V1+V2
,
c3= ˜c V1+V2+V3
V0+V1+V2+V3
, c4= ˜c V1+V2+V3+V4
V0+V1+V2+V3+V4
. Aus den oben angegebenen Gleichungen ergibt sich f¨ur V0=21 ml, V1=1,4 ml,V2=1,6 ml,V3=4,0 ml undV4=14,0 ml (V1+V2+V3+V4=V0) die gew¨unschte 1:2-Abstufung, n¨amlich
10−3 16 : 10−3
8 : 10−3 4 : 10−3
2
!mol l
Die Rechteck-K¨uvette zun¨achst nicht ausleeren. Die L¨osung mit der Konzentrationc4 wird in Aufgabe VI.6 noch ben¨otigt.
Freiwillige Zusatzaufgaben:
6. Absorptionsbanden des MnO−4 Ions.
Um das Streulicht zu unterdr¨ucken, wird auch bei diesem Versuch das Gr¨unfilter eingeschwenkt. Die Rechteckk¨uvette und die darin verbliebene 5×10−4-molare KMnO4-L¨osung aus Versuch VI.5 wird vor dem Eintritts- spalt positioniert. Messen Sie das Absorptionsspektrum, in dem Sie den Intensit¨atsverlauf zwischen gelb und blau in Schritten von ca. 2 mm (in den Banden auch kleiner) durchfahren.
7. Spektrum einer Gl¨uhlampe (”Temperaturstrahler“):
Der Gr¨unfilter wird wieder entfernt. In Schritten von ca. 1,0 cm wird der Spektralbereich von violett bis an das infrarote Ende des Spektrometers durchgefahren. Messen Sie den Fotostrom IP h und tragen Sie direkt IP h
¨
uber 1/λauf.
VII Auswertung
1. zu VI.4 und VI.5: Die gemessenen Fotostr¨ome werden sofort in ein gemein- sames halblogarithmisches Diagramm mit zwei (linearen) Abszissenskalen
f¨ur l und f¨ur c eingezeichnet. Punkte die offenbar aus der Geraden her- ausfallen, nochmals nachmessen. Zu Hause berechnen Sie aus der Steigung der”Lambert-Geraden
”(mitc= 5×10−5mol/l) den dekadischen Absorp- tionskoeffizientenk′und hieraus dann die Molarextinktionǫgem¨aßǫ=k′/c.
(Ber¨ucksichtigen Sie dazu, dass eine Intensit¨atsabnahme um den Faktor 10 gerade eine ¨Anderung des dekadischen Logarithmus um 1.0 bedeutet: die hierzu erforderliche Absorptionsl¨angel′ entnehmen Sie der Zeichnung. k′ ist dann gegeben durchk′ = 1/l). Sch¨atzen Sie die Fehler ab. Analog ver- fahren Sie bei der
”Beer-Geraden“. Geben Sie die Molarextinktion sowohl in liter/(mol cm) als auch in cm2/mol an. Wie gut stimmen die Werte aus der Lambert- und aus der Beer-Geraden ¨uberein?
2. zu VI.6: Tragen Sie den Fotostrom als Funktion der Spaltstellung direkt auf Millimeterpapier auf. Bestimmen Sie die Minima und geben Sie mit Hilfe der Eichkurve die Lage der Permanganatbanden in nm an. Eine Fehler- rechnung ist hier sinnlos, da die Banden mehrere nm breit. sind. Sch¨atzen Sie die Bandenbreite ab.
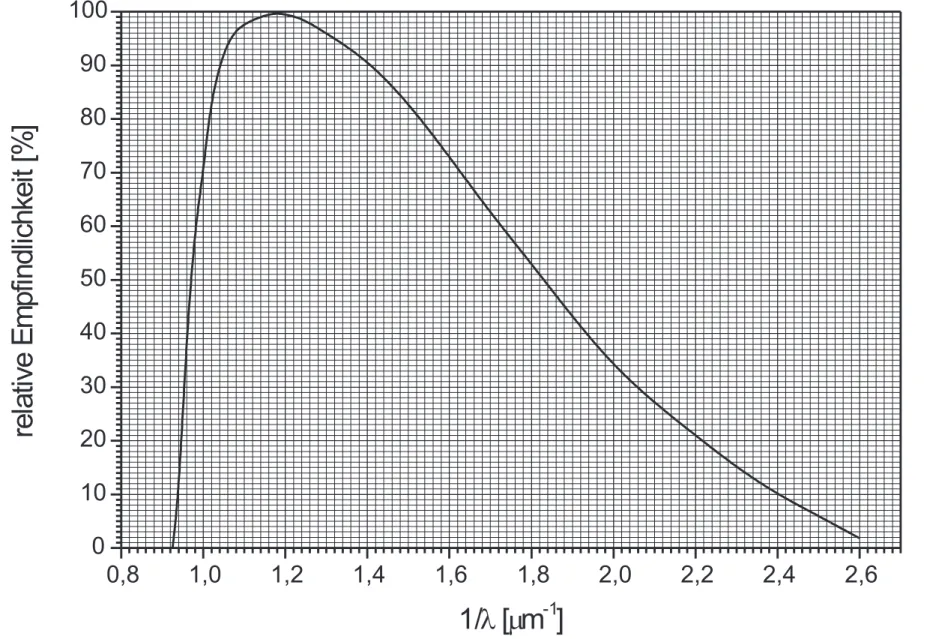
3. zu VI.7: Mit Hilfe der relativen spektralen Empfindlichkeitskurve des Fo- toelementes tragen Sie in das Diagramm die umgerechneten Werte ein, die sich aus den gemessenen Fotostr¨omen ergeben, wenn sie auf konstante Empfindlichkeit korrigieren. Fehlerbalken an einigen Punkten anbringen!
Die so erhaltene Kurve entspricht dem Planck’schen Strahlungsgesetz f¨ur die Temperaturstrahlung. Mit der Apparatur kann man jedoch nur den kurzwelligen Ast der Gesamtkurve messen. Das Maximum der spektralen Intensit¨atsverteilung liegt entsprechend der Temperatur des Gl¨uhfadens von ≈2500◦C bei ca. 1,2 µm, also außerhalb der Empfindlichkeit unseres Detektors. Falls Sie m¨ochten, k¨onnen Sie das auf die Empfindlichkeit des Detektors korrigierte Gl¨uhlampenspektrum auf halblogarithmischem Pa- pier aufragen. Die Intensit¨at bei den hohen Frequenzen (= violetter Ast der Planckkurve) verl¨auft nach der Funktion
I(ν)∝ν3e−(hν/kT)dν (Wiensches Strahlungsgesetz). (7) Da der Exponent bei dem im Praktikum vorliegenden Bedingungen (T,ν) zwischen ca. -5 und -12 liegt, dominiert die Exponentialfunktion. Es ergibt sich somit nur eine schwach gekr¨ummte Kurve.
0,8 1,0 1,2 1,4 1,6 1,8 2,0 2,2 2,4 2,6 0
10 20 30 40 50 60 70 80 90 100
re la tiv e E m p fin d lic h ke it [% ]
1/ l [ m m
-1]
Abbildung 6:Relative spektrale Empfindlichkeit f¨ur das Fotoelement BPY64.