Research Collection
Doctoral Thesis
Über die Nitration des β-Methylanthrachinons
Author(s):
Bütler, Robert Publication Date:
1921
Permanent Link:
https://doi.org/10.3929/ethz-a-000107676
Rights / License:
In Copyright - Non-Commercial Use Permitted
This page was generated automatically upon download from the ETH Zurich Research Collection. For more information please consult the Terms of use.
ETH Library
Dis
s.ETH
'•WO £
Über die Nitration des
jö-Methylanthrachinons
Von der
Eidgenössischen Technischen Hochschule in Zürich
zur
Erlangung
derWürde eines Doktors der technischen Wissenschaften
genehmigte
Nr. 280
Promotionsarbeit
vorgelegt von
Robert Butler, dipl. Chemiker
aus Cham
Referent: Herr Prof. Dr. R. Eder Korreferent: Herr Prof. Dr. H. E. Fierz
Zürich 1921
Druck von Thomas & Hubert, Weida i. Thür.
SpezialdruckereifürDissertationen
Leer
-Vide
-Empty
Vorliegende
Arbeit wurde impharmazeutischen
Institutder
Eidgenössischen
Technischen Hochschuleausgeführt.
Ich möchte an dieser Stelle meinem verehrten Lehrer und
geschätzten Freunde,
Herrn Prof. Dr. R.
Eder,
meinen Dank
aussprechen
für das regeInteresse,
das ermeiner Arbeit
entgegenbrachte.
Leer
-Vide
-Empty
Inhalts-Übersicht.
Seite
Einleitung 7
Theoretischer Teil 10
A.
Mononitrokörper
des/J-Methylantrachinons
10Konstitutionsbeweis für das bei direkter Nitration als
Hauptprodukt
erhaltene
Mononitro-^-methylanthrachinon
24B.
Dinitrokörper
desj3-Methylanthrachinons
26Konstitutionsbeweise für die beiden wichtigsten dinitrierten Derivate
des
/3-Methylanthrachinons
31I.
Dinitro-0-methylanthrachinon
vomFp. 329/331°
32II.
Dinitro-^-methylantbrachinon
vom Fp.293/295°
34C. VersuchezurDarstellungvonTrinitro-oder höher nitrierten
/3-Methyl-
anthrachinonen 36
D. Übersicht über die Produkte der direkten Nitrierung des jS-Methyl-
anthrachinons 38
E.
Urawandlungsprodukte
derNitro-/3-methylanthrachinone,
die zwecks Konstitutionsbestimmungen der letzteren dargestellt wurden.... 39Experimenteller Teil 41
A. Studium der Nitration des
^-Methylanthrachinons
41I.
l-Nitro-2-methylanthrachinon
421. Versuch 42
a) Alkohollöslicher Teil 43
b) Alkoholunlöslicher bezw. alkoholschwerlöslicher Teil... 43
2. Versuch 44
3. Versuch 44
a) Alkohollöslicher Teil 45
b) Alkoholunlöslicher Teil 45
4. Versuch 46
a) Alkohollöslicher Teil 46
Verhalten vonreinem
Mononitro-0-methylanthrachinon
gegenverdünntes Alkali 46
b) Alkoholunlöslicher Teil 46
Untersuchung der Benzolmutterlauge 47
Zusammenfassung
der Versuche 1—4 48Weitere Versuche 50
IL
Dinitro-jS-methylanthrachinone
51Einleitung
511. Versuch: Nitration nach D.R.P. 131873 51
a) Alkohollöslicher Teil 53
Aceton-Behandlung
54b) Alkoholunlöslicher Teil 55
l,5-Dinitro-2-methylanthrachinon
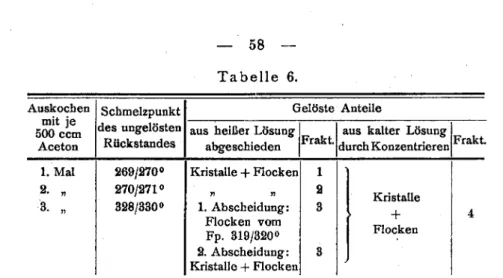
56Untersuchung der
Eisessig-Auszüge
57Aceton-Behandlung
57l,8-Dinitro-2-raethylanthrachinon
60Seite 2.Versuch: Nitration nach Schaarschmidt und Stahlschmidt 61
a) Alkohollöslicher Teil , . 62
b)
Alkoholunlöslicher Teil 633. Versuch: Nitration von
l-Nitro-2-methylanthrachinon
... 64III. Versuche zur Darstellung von Trinitro- oder höher nitrierten
/3-Methylanthrachinonen
65Einleitung 65
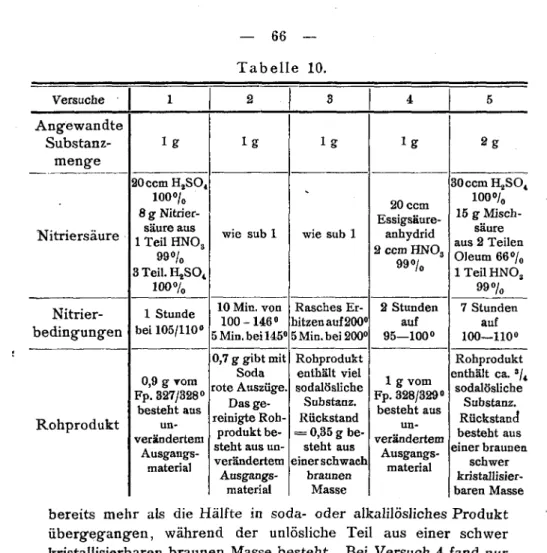
a) Versuche mit l,5-Dinitro-2-methylanthrachinon 65 b) Versuche mit
l,8-Dinitro-2-methylanthrachinon
67B.
Umwandlungsprodukte
derNitro-/J-methylanthrachinone,
die zwecks Konstitutionsbestimmung der letzteren dargestellt wurden .... 67I. Umwandlung des
Mononitro-/?-methylanthrachinons
in 1-Amino-2-methylanthrachinon
und inOxy-2-methylanthrachinon
... 67Einleitung 67
1.
l-Amino-2-methylanthrachinon ausl-Nitro-2-methylanthrachinon
672.
1-Oxy-2-methylanthrachinon
. . 68a) Aus
1-Amino-2-methylanthrachinon
durch Diazoreaktion . 68 b) DurchKondensation vonPhthalsäureanhydrid
und o-Kresol 68 II.Oxydation
vonNitro-/f-methylanthrachinonen
zu Carbonsäuren . 69Einleitung 69
Versuche mit Nitroschwefelsäure nach D.R.P. 273341 .... 72 Versuche mit
CrOa
in salpetersaurer Lösung 73 1. l-Nitroanthrachinon-2-carbonsäure und deren Ca-Salz ausl-Nitro-2-Methylanthrachinon 73
2. 1,5-Dinitroanthrachinon-2-carbonsäurenndderen Ag-Salzaus
l,5-Dinitro-2-methylanthrachinon
743. 1,8-Dinitroanthrachinon-2-carbonsäureundderen Ag-Salz aus 1,8-Dinitro-2-methylanthrachinon 75 III. Reduktion von
Nitroanthrachinon-^-
carbonsäuren 76Einleitung 76
1. 1-Aminoanthrachinon-2-carbonsäure und deren Ag-Salz aus
1-Nitroanthrachinon-2-carbonsäure 77
2. l,5-Diaminoanthrachinon-2-carbonsäure aus 1,5-Dinitroanthra¬
chinon-2-carbonsäure 78
IV. Umwandlung von
Nitroanthrachinon-^-carbonsäuren
in Nitro-,Amino- und
Oxyanthrachinone
80Einleitung 80
1. Versuch zur Darstellung von «-Nitroanthrachinon aus dem Ca-Salz der 1-Nitroanthrachinon-2-carbonsäure 82
2. a-Aminoanthrachinon 82
a) Aus demAg-Salz der 1-Aminoanthrachinon-2-carbonsäure 82 b) Aus der 1-Aminoanthrachinon-ö-carbonsäure durch Kochen
mit Zinnoxydulkali 82
3. 1,5-Dinitroanthrachinon ausdemAg-Salzder 1,5-Dinitroanthra-
chinon-2-carbonsäure 83
4. 1,8-Dinitroanthrachinon 85
a) AusdemAg-Salzder l,8-Dinitroanthrachinon-2-carbonsäure 85
b) Aus Anthrachinon durch Nitration 85
5. 1,5-Diaminoanthrachinon aus 1,5-Dinitroanthrachinon .... 87 6.
1,5-Dioxyanthrachinon
(Anthrarufin) aus 1,5-Diaminoanthra¬chinon durch Diazoreaktion 89
Einleitung.
Das
/?-Methylanthrachinon
ist sowohl vom wissenschaftlichen als auch vom technischenStandpunkte
aus ein sehrwichtiger Körper.
Es ist die Grundsubstanz einer Reihewichtiger
in derNatur vorkommender
Verbindungen,
die als wirksame Bestand¬teile einer ganzen
Gruppe
vonArzneidrogen (Oxymethylanthra- chinondrogen)
seitlanger
ZeitBedeutung haben,
und bildet außerdem dasAusgangsmaterial
zurDarstellung
einer ganzenGruppe
von Anthrachinonfarbstoffen.Das
/?-Methylanthrachinon
ist schon oftGegenstand
chemischer
Untersuchungen
gewesen und wurde zuerst vonO.
Fischer1)
ausMethylanthrazen dargestellt
und in seinenEigenschaften
beschrieben. Wiespätere Untersuchungen
von C. Wachendorff und Ph.Zincke')
und E.Börnstein3)
fest¬stellten,
muß das Produkt von Fischer nicht rein gewesensein;
wahrscheinlich handelte es sich um ein Gemisch der beiden Isomeren. Das
ß- Methylanthrazen
ist im Steinkohlenteer einBegleiter
des Anthrazens und ist von diesem nurschwierig
zutrennen. Bei der
Oxydation
des technischen Anthrazens zuAnthrachinon erhältmandieses
vermengt
mitMethylanthrachinon
und die Derivate beider
Körper
können auf demWege
zurFarbstoff
bildung
durch den ganzen Prozeß derZwischenprodukten¬
bildung
hindurchvereinigt
bleiben. Da dieFarbstoffabkömmlinge
des
Methylanthrachinons
anders nuanciert sind als die des Anthra-chinons,
so muß ein variablerMethylanthrachinongehalt
des Aus¬gangsmaterials,
des technischenAnthrachinons,
Variationen in der Nuance der resultierenden Farbstoffeergeben.
Wie mit derJ) B. 8, 675 (1875).
») B. 10, 1485
(1877).
•)
B.15,
1820(1882).
großen Entwicklung-
der künstlichen Farbstoffe dieAnsprüche
an
Qualität überhaupt gesteigert wurden,
so war man auchbestrebt,
inbezug
auf Reinheit und Konstanz der Nuance denAnforderungen
der Kundschaftgerecht
zu werden. Esgelang,
den
Reinheitsgrad
desAusgangsmaterials,
des Anthrazens zu er¬höhen,
wobei dasMethylanthrazen abgeschieden
wurde und alsNebenprodukt
auftrat. Mit dem Anhäufen dieses Materials be¬gannen dann auch
Bestrebungen,
dasselbe nutzbar zu machen.Es wurde die
Beobachtung gemacht [vergl.
D.R.P. 131873 derB.A.S.F.
(1900)],
daß verschiedeneFarbstoffabkömmlinge
desMethylanthrachinons
in ihrenEchtheitseigenschaften
den Farb¬stoffen ausdemAnthrachinon nichtnur
ebenbürtig
waren, sondern dieselben an Schönheit der Nuance noch überboten.Die Farbstoffe dieser
Gruppe
haben abererst anBedeutung
gewonnen, als die
synthetische Darstellung
des/?-Methylanthra¬
chinons
gelungen war1).
DieserKörper
entsteht durch zweifache Kondensation ausPhthalsäureanhydrid
und Toluol. In der erstenPhase entsteht die
p-Toluyl-o-benzoesäure,
die vor weitererKondensation isoliert wird. Die
zweite,
leichter zu bewerk- stellendeOperation
wirdausgeführt,
indem dieserKörper
einfachmit konzentrierter Schwefelsäure erhitzt wird. Heute werden beträchtliche
Mengen /?-Methylanthrachinon synthetisch
dar¬gestellt.
Das als technisches/?-Methylanthrachinon
bezeichnete Produkt ist einKörper
von hellschwefelgelbem
Aussehen. Ichfand den
Schmelzpunkt
bei dem von mir alsAusgangsmaterial
benützten technischen
yî-Methylanthrachinon,
das aus einem Gemischvon lockerem Pulver und Knollenbestand,
bei171/172°,
während dem reinen Produkte der
Fp.
176° zukommt.Die
Bedeutung
desß-Methylanthrachinons liegt
einerseitsdarin,
daß die von demselben direktabgeleiteten
Farbstoffe alsHomologe
der Farbstoffe des Anthrachinons die vorerwähnte Gütebesitzen,
anderseits abererlangt
das^-Methylanthrachinon
durch
Oxydation
derMethylgruppe
zurCarboxylgruppe
eine sehrerweiterte
Reaktionsfähigkeit.
DieAuffindung
der technischausführbaren
Oxydation
des einfach nitrierten/?-Methylanthra-
•) Friedel und Crafts, A. eh.
[6],
14, 446;Limpricht,
A. 299, 300;Limpricht
undWiegand,
A. 311, 181; Heller und Schiüke, B. 41, 3627;Elbs, J.pr.
[2],
41, 4.chinons ist
allerdings
erst neueren Datums(vergl.
D.R.P. 229394 der B.A.S.F. 1909 undTerres,
B.46, 1638),
und dieEntwicklung
dieser Farbstoffe istzur
gegenwärtigen
Zeit noch in bestemGange.
Neben dieser
Bedeutung
als Grundsubstanz einer Farbstoff- gruppe hat das/J-Methylanthrachinon
auch Interesse als Mutter¬substanz einer Anzahl in der Natur vorkommender
Verbindungen,
welche wirksame Bestandteile von
Arzneidrogen
bilden. Seitlanger
Zeit kennen wir dieChrysophansäure,
welche ein1,8-Dioxy- 3-methylanthrachinon
darstellt. Sie findet sich in verschiedenenAbführdrogen,
zumBeispiel
imRhabarber,
imKreuzdorn,
in der Faulbaumrinde neben demFrangula-Emodin,
einem1, 6, 8-Trioxy- 3-methylanthrachinon.
In der Aloë und in den Sennesblättern ist Aloë-Emodinenthalten,
welches ebenfalls als einTrioxy- /?-methylanthrachinon
erkanntwurde,
in welchem aber zumUnterschied von
Frangula-Emodin
eineHydroxylgruppe
in derSeitenkette sitzt
(l,8-Dioxy-3-oxymethylanthrachinon).
Das beiHautkrankheiten verwendete
Chrysarobin
enthält als wirksameStoffe
Reduktionsprodukte
solcherOxymethylanthrachinone,
be¬sonders das
Chrysophansäureanthranol.
Alle dieseKörper
wurdenin neuerer Zeit
eifrig
untersucht.Ich habe mir in der
vorliegenden
Arbeit das Studium derSalpetersäureeinwirkung
auf das/8-Methylanthrachinon
zurAuf¬gabe gemacht,
da eine genaue Durchsicht der Literatur und eine Anzahl Vorversucheergaben,
daß dieNitroverbindungen
nur inbescheidenem
Umfange
bekannt und die vorhandenenAngaben
in mancher Hinsicht unkorrekt sind und der
Nachprüfung
be¬dürfen.
Theoretischer Teil.
A. Mononitrokörper des /5-Methylanthrachinons.
Von den sieben
möglichen
isomerenMononitrokörpern
des/?-Methylanthrachinons
ist nur einerbekannt,
der zuerst vonH. Römer und W.
Link1) dargestellt
und beschrieben wurde(Fp. 269/270°)
undder,
wie wirspäter
ausführenwerden,
als1-Nitro-2-methylanthrachinon
zu betrachten ist. DieAngaben
über die
Darstellung
lassen sich wiefolgt
resümieren:Einwirkung-
von
Salpetersäure
oder besser Kaliumnitrat auf in konzentrierterH,S04 gelöstes /?-Methylanthrachinon
beiInnehaltung
vonniedriger Temperatur.
BeiBehandlung
desRohproduktes
mit Alkoholgeht
nach Römer und Link eine zweite bei derNitrierung gebildete
Substanz mit roter Farbe inLösung,
die ingrößerer Menge auftritt,
wenn bei derNitrierung
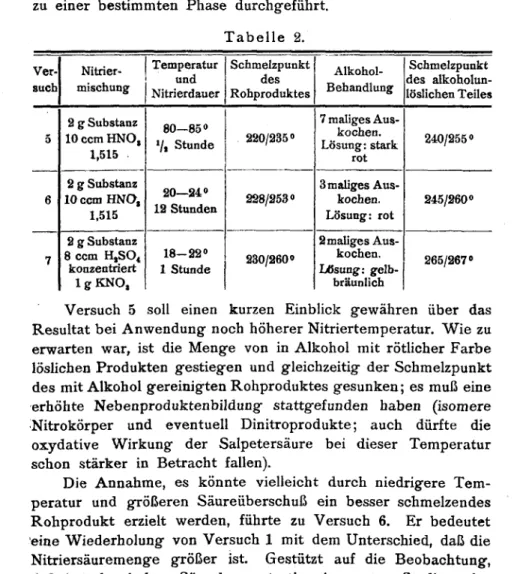
nicht starke Schwefelsäure verwendet wird. Wird bei erhöhterTemperatur gearbeitet,
so entstehen andereNebenprodukte.
Esmußte nun von Interesse
sein,
diese Reaktion etwas näherzu studieren und zu
untersuchen,
ob die in Alkohollöslichen An¬teile des
Reaktionsproduktes
identifiziert und durchgeeignete
Variation derVersuchsbedingungen
auch andere isomereMononitro-/?-methylanthrachinone
in namhafterMenge
erhaltenwerden könnten.
Die
Untersuchungen zeigten aber,
daß auch unter anderenNitrierungsbedingungen
ausschließlich das1-Nitro-2-methyl¬
anthrachinon in
überwiegender Menge gebildet
wird. Unter allenVersuchsbedingungen,
bei denen derNitrierungsprozeß praktisch vollständig
verlaufen war, wurde dieBildung
alkohol¬löslicher
Nebenprodukte
der Nitration beobachtet. Diese Produkte erschweren dieReindarstellung
desl-Nitro-2-methylanthrachinons
J) B. 16, 696 (1883).
bedeutend. Die
Untersuchung
der alkohollöslichenKörper
bietetgroße Schwierigkeiten.
Während beiniedriger Nitrierungs- temperatur
die alkohollöslichen Bestandteilehauptsächlich
ausunverändertem
Ausgangsmaterial bestehen,
verschwindetletzteres,
wenn die Reaktion bei höherer
Temperatur
vorgenommenwird,
nahezuvollständig; gleichzeitig
wird aber dieBildung
der mitroter Farbe in Alkohol löslichen
Körper begünstigt.
Esgelang- nicht,
aus diesem Gemisch neueKörper
in reiner Form zuisolieren,
da dievorlieg-enden
Substanzenaugenscheinlich
sehrähnliche Löslichkeitsverhältnisse besitzen und äußerst leicht zusammenkristallisieren. Ich vermute, daß in diesen Neben¬
produkten
der Nitration enthalten sein können:a) Geringe Mengen
von Isomeren des 1-Nitro-2-methylanthra- chinons,
b)
eventuellgeringe Mengen
vonDinitrokörpern,
c) geringe Mengen
vonOxykörpern
und eventuellOxycarbon- säuren,
die dadurch charakterisiertsind,
daß sie sich in Soda oder Alkalien mit roter Farbe lösen.Bezüglich
dieserEinzelheiten,
sowie der weiterenErgebnisse
sei auf den
speziellen
Teil verwiesen.Von den verschiedenen von mir
geprüften Mononitrierungs-
methoden des
/J-Methylanthrachinons
hat sich als beste Dar¬stellungsweise
für dasl-Nitro-2-methylanthrachinon
das Arbeiten nach Römer und Link erwiesen und zwarvornehmlich bei Inne¬haltung-
einermöglichst niedrigen Temperatur.
Die
Frage
nach derStellung
derNitrogruppe
in demeinzigen
bisher bekanntenMononitro-/3-methylanthra-
chinon
(Fp. 269/270°) gestaltet
sich ziemlichkompliziert;
sie seiim
folgenden eingehend
erläutert.Es kommen hinsichtlich der
Stellung
einerNitrogruppe
im/J-Methylanthrachinon folgende Möglichkeiten
in Betracht:A. Eintritt der
N02-Gruppe
in denBenzolkern,
der dieCH3-Gruppe trägt.
Drei Isomere sind
möglich:
•
ü$r
*coo-:
»oDr
B, Eintritt der
N02-Gruppe
in den nicht substituiertenBenzolkern.
Dabei sind vier Isomere
möglich.
Der Fall Bkommt,
wiewir
später
sehenwerden,
beimMononitro-/?-methylanthrachinon
nicht in Betracht.
Was bis heute über die
Konstitution,
resp. über dieStellung
der
Nitrogruppe
im erwähntenKörper
bekanntist,
sei imfolgenden
kurz referiert.Römer und Link versuchen die
Stellung-
derN02-Gruppe
in ihrem
Mononitro-/?-methyIanthrachinon
durchÜberführung
indas
entsprechende Oxymethylanthrachinon (Fp. 178°)
wahrschein¬lich zu machen. Die beiden bekannten
Monooxyanthrachinone,
das
o-Oxy-
oderErythrooxyanthrachinon
oder wie wir es heute nennen, das1-Oxyanthrachinon (ct-Oxyanthrachinon)
und das2-Oxyanthrachinon (/?-Oxyanthrachinon),
werden von Römerund Link in
bezug
aufLöslichkeit, Schmelzpunkt
usw. mit demvorliegenden Oxymethylanthrachinon verglichen,
und es wird der Schluß gezogen, daß letzteres in seinenEigenschaften
sich mehrdem
ct-Oxy-
als dem/?-Oxyanthrachinon
nähere. Ob aber einl-Nitro-2-methylanthrachinon
oder einl-Nitro-3-methylanthra-
chinon
vorliegt,
wird von Römer und Link nicht entschieden.K. Holder
mann1)
hat bei seinenUntersuchungen
über denkatalytischen
Einfluß vonQuecksilbersalzen
bei derSulfurierung
und
Nitrierung
durcheinstündiges
Kochen von/3-Methylanthra-
chinon mit der zehnfachen
Menge HN03
vomspezifischen
Gewicht
1,4
unter Zusatz von0,3
TeilenHg(N03)2
ebenfalls einNitro-/?-methylanthrachinon dargestellt,
das nach Holdermannganz mit dem
„l-Nitro-2-methylanthrachinon
von Römer undLink" übereinstimmen soll. Holdermann ist also über die
ungeklärte Lage
in derStellung
derN02-Gruppe
beimKörper
vonRömer undLink
hinweggegangen
und nimmt ohne weiteres an, daß es sich um dasl-Nitro-2-methylanthrachinon
handle.Diese
Auffassung
ist in die Literaturübergegangen
und bis 1907stillschweigend
als feststehend erachtet worden.Dann aber haben W. H.
Bentley,
H. Gardner und Ch.Weizmann8)
nun bei ihrerUntersuchung
überOxymethyl-
») B.
39,
1257 (1906).•)
Soc.91,
1626 (1907).13
anthrachinone durch Kondensation von
Phthalsäureanhydrid
mitm-Kresol und Borsäure ein
l-Oxy-3-methylanthrachinon
vomFp.
178°erhalten,
während ihrl-Oxy-2-methylanthrachinon,
erhalten durch Kondensationvon
Phthalsäureanhydrid
mito-Kresol,
den
Fp. 185/186°
besitzt. Da nun dasOxymethylanthrachinon
von Römer und Link nach
Angaben
dieser Autoren ebenfallsbei 178°
schmilzt,
so nehmenBentley, Gard
ner undWeizmann an,daß dasselbe mit ihreml-Oxy-3-methylanthrachinon
identischsei. Diese Annahme ist nun auch in Richters Kohlenstoff- Lexikon
eingedrungen.
Nach derselben würde also dem Mono-nitro-/?-methylanthrachinon
von Römer und Link die Kon¬stitution eines
l-Nitro-3-methylanthrachinons
zuzuschreiben sein.Eder und
Widmer1)
haben nun für dasOxymethylanthra¬
chinon von Römer und Link den
Fp.
181° erhalten und habengefunden,
daß das nachBentley,
Gardner undWeizmann
durch Kondensation vonPhthalsäureanhydrid
und m-Kresol mitBorsäure als Kondensationsmittel erhaltene
Oxymethylanthra¬
chinon vom
Fp. 178/179°
mit dem von Römer und Link nichtidentisch ist. Der
Mischschmelzpunkt
der beiden Produktezeigt,
daß dieselben verschiedener Natur
sind; desgleichen
haben dieAcetylderivate
stark verschiedeneSchmelzpunkte: Acetylderivat
des Produktes von Römer und LinkFp. 180/181°, Acetyl¬
derivat des Produktes von
Bentley,
Gardner und WeizmannFp. 156/157°.
In einer neueren
Abhandlung
von Fritz Ulimann und WalterSchmidt*)
über die Kondensation von Phthalsäure¬anhydrid
mit Aluminiumchlorid wird dasl-Oxy-3-methylanthra-
chinon
beschrieben, dargestellt
durchEliminierung
von Chlorausl-Oxy-3-methyl-4-chloranthrachinon.
Die Konstitution letztererVerbindung
isteindeutig,
bewiesen durch ihreBildungsweise
ausPhthalsäureanhydrid
undp-Chlor-m-kresol.
Für das1-Oxy- 3-methylanthrachinon,
dessen Konstitution nun aucheindeutig
bewiesen
ist,
fanden Ulimann undSchmidt inÜbereinstimmung
mit
Bentley,
Gardner und Weizmann und mit Eder und Widmer ebenfalls denFp.
178°.')
Nach mündlichenMitteilungen.
2) B. 52, 2098 (1919).
Zur
Konstitutionsaufklärung
desMononitro-/?-methylanthra-
chinons könnten
herbeigezogen
werden:die
Monooxymonomethylanthrachinone,
dieAntbra-chinondiamine und die aus ihnen durch Konden¬
sation mit o-Diketonen erhaltenen
Azinfarbstoffe,
die
Monoaminoanthrachinonmonocarbonsäuren
und dieMonooxyanthrachinonmonocarbonsäuren.
Im
nachfolgenden
soll eineZusammenfassung dessen,
was bisjetzt
über diese Anthrachinonderivate bekanntist, gegeben
undinsbesondere kritisch beleuchtet
werden,
inwieweit die Kon¬stitution dieser
Körper
sicher erwiesen undzu derbeabsichtigten endgültigen Konstitutionsaufklärung
desMononitro-/?-methyl-
anthrachinons verwendbar ist.
a) Monooxymonomethylanthrachinone.
Monooxymonomethylanthrachinone
mitStellung
der beidenSubstituenten an verschiedenen Benzolkernen des Anthrachinon- moleküls sind bis
jetzt
nicht bekannt. Den sechsmöglichen
isomeren
Monooxymonomethylanthrachinonen,
bei denen dieSubstituenten sich im
gleichen
Benzolkernebefinden,
kommen die nachstehenden Formeln zu:OH OH
CH,
/Vco\A /\/COV^ /\/C(Vvoh
L
U JJ-CH,
co'v v Nco' Y x/XC0'/\/C(X
4.
/\/c°y\_
rr 5.rrcoYV°H *.fYcY)
\AcoÀÀOH
*
U\c0À/
'U\coAy
OH
-CH,
Diese
Verbindungen
sind zur Zeit alle mehr oderweniger gut
bekannt.1.
l-Oxy-S-methylanthrachinoii ist,
wie imvorangehenden
schonerwähnt,
erhalten worden einerseits vonBentley,
Gardnerund Weizmann und von Eder und
Widmer,
anderseits von15
Ulimann und Schmidt. Die Konstitution dieses bei 178°
schmelzenden
Körpers kann,
wie ebenfalls bereitsangeführt wurde, jetzt
als sicherfestgestellt
betrachtet werden.2.
l-Oxy-4-methylanthrachinon
entsteht bei der Kondensation vonPhthalsäureanhydrid
undp-Kresol;
die.Reaktion
isteindeutig.
Der
Körper
schmilzt bei 175°(korr.).
3.
3-Oxy-l-methylanthrachinon.
DieserKörper
ist von.Bistrzycki
und Yssel de
Schepper1)
aus dementsprechenden
Anthranoldargestellt
und beschrieben worden. Siegeben
für denselben denFp. 299/300°
an.Bistrzycki
und Yssel deSchepper
stützen ihre
Konstitutionserklärung
auf eine Reaktion vonNourrisson2).
Letzterer weistnach,
daß durch Kondensationvon
Phthalsäureanhydrid
und Anisol mit Aluminiumchlorid als Kondensationsmittel eineBenzoylbenzoesäure
IVentsteht,
"•
Oc-0- OCH,
in welcher der Anisolkern in
p-Stellung
zurOCHg-Gruppe
anden Phthalsäurerest
gebunden
wird. Nourrissonbehauptet,
daß beim Erhitzen der
Anisolphthaloylsäure
mit KOH auf280—290" als
Spaltungsprodukte
Benzoesäure undp-Oxybenzoe-
säure entstehen und
gibt
an, daß dieseAnisolphthaloylsäure
beimErhitzen mit konzentrierter
H2S04
auf 150° einOxyanthrachinon ergebe,
das bei 290° noch nicht schmelze und in seinenEigen¬
schaften mit dem
/?-Oxyanthrachinon
übereinstimme. Bei der Reduktiongibt
dieseAnisolphthaloylsäure
IV nachBistrzycki
und Yssel de
Schepper
das der Formel Ventsprechende Methoxyphenylphthalid
(
V \_ rVocH,
v
UCH^U
Dieses
gleiche
Produkt erhieltenBistrzycki
und Ysselde
Schepper,
auchausgehend
vom Phenol undPhthalaldehyd- ')
B.31,
2790(1898).
«)
B.19, 2103(1886).
säure mit
73°/0iger H2S04
alsKondensationsmittel, gemäß
nach¬stehendem Schema:
COOH "
OH ArnwvCOH \/
Damit ist nach
Bistrzycki
undYssel deSchepper bewiesen,
daß auch Phenol bei der Kondensation mit
Phthalaldehydsäure
in
p-Stellung
zurOH-Gruppe angegriffen
wird. InAnalogie
zurReaktionsweise des Phenols
glauben Bistrzycki
undYsselde
Schepper
nun annehmen zudürfen,
daß auch m-Kresolbei der Kondensation mit
Phthalaldehydsäure
inp-Stellung
zurOH-Gruppe reagiere
unddaß das ausdementstehendenm-Kresyl- phthalid
VI erhaltene Anthrachinonderivat vomFp. 299/300°
das3-Oxy-l-methylanthrachinon
VII sein müsse:virYcNn-°H->vii/YCOYx'°H CLHr
VVnA/CO CH,Die
Richtigkeit
der Annahme vonBistrzycki
und Ysselde
Schepper,
daß das zurDarstellung
des3-Oxy-l-methyl-
anthrachinons verwendete
m-Kresylphthalid
nach dergleichen
Reaktionsweise durch
Phtalaldehydsäure-Kondensation
wie dasPhenylphthalid gebildet werde,
ist zwar von dengenannten
Autoren nicht
streng
wissenschaftlichbewiesen,
hat aberjetzt
durch dieArbeiten vonUlimann und Schmidt eine
Bestätigung
erfahren. Bei der Kondensation von m-Kresol mit Phthalsäure-
anhydrid
können nur zweiOxymethylanthrachinone
entstehenentsprechend
den FormelnVIEL
i ! I I
IX.'
Da das
l-Oxy-3-methylanthrachinon
von Ulimann undSchmidtdargestellt
und seine Konstitution einwandsfrei erwiesenwurde,
dieser
Körper
aber mit dem vonBistrzycki
und Ysselde
Schepper dargestellten
nichtübereinstimmt,
so bleibt fürden letzteren nur die von
Bistrzycki
und Yssel deSchepper
angenommene Konstitution
übrig.
Gegen
die Art derBeweisführung
vonBistrzycki
und Yssel deSchepper,
welche die Reaktion vonNourrisson benützt, könnten, gestützt
auf die Arbeit von Ullmann undSchmidt,
Einwände erhoben werden. DieseAutoren,
welche die Kondensationsreaktion vonPhthalsäureanhydrid
mitPhenolen bei
Anwendung
vonA1C13
etwaseingehender
studiert
haben,
kommen zu demResultate,
daß Phenole mitPhthalsäureanhydrid
undA1C13 Kondensationsprodukte liefern,
beidenen der
Eingriff
derCarbonylgruppe
des Phthalsäure-anhydrids gleichzeitig
in verschiedenerStellung
zurOH-Gruppe
der Phenoleerfolgt,
zumgrößten
Teile aberin
O-Stellung
zuderselben,
OH
*•
n-°°-fi '-^J-COOH 'x/'CH,
In
untergeordneter Menge
entstehen dabei auch noch andereKörper.
DurchAnwendung
vonAcetylentetrachlorid
als Ver¬dünnungsmittel
bei derKondensationsreaktion soll die Ausbeuteam
Hauptprodukt
der Kondensation erhöht werden. Dieser Befund von Ulimann und Schmidt stehtgewissermaßen
imWiderspruch
zur Reaktion vonNourrisson,
nach welcher derEingriff
der Phthalsäure bei Phenolen undA1C13
alsKondensationsmittelin
p-Stellung
zurOH-Gruppe erfolgt.
Ulimann und Schmidthaben bei der Kondensation von Phenol mit
Phthalsäureanhydrid
undA1C13
dasp-Phenylphthalid
nur inuntergeordneter Menge
erhalten. Weil dasselbe aber doch neben dem o-Derivatentsteht,
so istanzunehmen,
daß vielleichtgering¬
fügige Abänderungen
derReaktionsbedingungen,
wie Ver¬wendung
des Phenoläthers statt des freien Phenols oder vonPhthalaldehydsäure
stattPhthalsäureanhydrid,
andereTempera¬
turen,
längere
oder kürzereEinwirkungsdauer,
leicht eine Ver¬schiebung
der Ausbeutezugunsten
des einen oder des anderen Isomeren bewirken können.Was die
Beweisführung
von Nourrissonanbetrifft,
so istin
derselben
insofern eine schwacheSeite
zuerkennen,
alsButler. 2
Nourrisson die
p-Oxybenzoesäure
unter denSpaltungs¬
produkten
derAnisolphthaloylsäure angibt.
Wirwissen, daß
dieo-Oxybenzoesäure
bei erhöhterTemperatur
leicht in diep-Oxy-
benzoesäure
umgelagert
wird. Esfolgt daraus,
daß in der vor¬liegenden Anisolphthaloylsäure
dieOCH8-Gruppe ebensogut
inortho- als in
para-Stellung
zurCarboxylgruppe
stehen könnte.Doch
spricht
dieBildung
von/?-Oxyanthrachinon
bei der Be¬handlung
derAnisolphthaloylsäure
Nourrissons mitH2S04
fürdie
para-Ständigkeit
derOCH3-Gruppe
imKörper
vonNourrisson. Die Konstitution des
Körpers
vonBistrzycki
und Yssel de
Schepper
vomFp. 299/300°
kann somit alserwiesen betrachtet werden.
4.
S-Oxy-2-methylanthraclnnon
entsteht nachFraude1)
bei derKondensation von
Phthalsäureanhydrid
mit o-Kresol. Dieses Produkt wurde inMethylalizarin übergeführt,
wodurch seine Konstitution alsfestgestellt
erscheint. Nach denAngaben
vonFraudeschmilzt das
2-Oxy-3-methylanthrachinon bei260—262°,
nachdem es bei 182° bereits zu erweichen
beginnt.
Die Tat¬sache macht es
wahrscheinlich,
daß derKörper
von Fraudenicht ganz rein war,
infolgedessen
dieÜberführung
in einMethylalizarin
auch nicht alsunzweideutig festgestellt
betrachtet werden kann.6.
2-Oxy-l-methylaiitIirachIuon
und 6.l-Oxy-2-methyIanthrachinon.
Diese
Körper
wurden vonBentley,
Gardnerund Weizmanndurch
Synthese dargestellt.
1.Bei derKondensation von
Phthalsäureanhydrid
mit o-Kresolerhielten sie
je
nach demKondensationsmitteJ
mit Borsäure ein Produkt vom
Fp. 185/186°,
mit
A1C1,
. ein Produkt vomFp.
über 300°.Es bestehen drei
Möglichkeiten entsprechend
den Formeln:*
cCrc-
*ao?
<ccôv
») A.
202,163 (1880).
Formel 4 ist bekannt
(Produkt
vonFraude);
es besteht dem¬nach noch die
Möglichkeit
zwischen 5 und 6.Bentley,
Gardner und Weizmann nehmen an, daß in
Analogie
zurReaktion von Nourrisson
(siehe
S.15)
beiVerwendung
vonAlClg
als Kondensationsmittel wahrscheinlich durchAngriff
des Kresols inp-Stellung-
zurOH-Gruppe
zunächst das Produktnachfolgender
Formel entstehe:xi. ' ï-c°-
'X/J-COOH kyOH
CH,
Durch weitere Kondensation können entstehen die
Körper,
dieden
obigen
Formeln 4 und 5entsprechen.
Da aber 4 bekannt ist(Produkt
vonFraude),
so muß dem Produkt vom Schmelz¬punkt
über 300° wahrscheinlich die Formel 5 zukommen. Ful¬das bei der Kondensation mit Borsäure erhaltene Produkt vom
Fp. 185/186°
verbleibt demnach nur noch die Formel 6.Diese
Beweisführung
wäre nun nach dem unter3-Oxy- 1-methylanthrachinon Gesagten
nicht ohne weitereshinzunehmen,
da
ja
Ulimann und Schmidt auch bei der Kondensation vono-Kresol und
A1CI8
inüberwiegender Menge
dieo-Oxysäure
erhalten haben „_ OH
Tr-,
XII.
I
ihre
gleichzeitig
alsNebenprodukt
erhaltenep-Oxysäure
XL
-CO/N/
-CO /N
'-COOH WOH 'Hg
liefert aber bei weiterer Kondensation das von
Bentley,
Gardner undWeizmann beschriebene2-Oxy-l-methylanthra-
chinon.
Gleichzeitig
wird auch von Ullmann und Schmidt be¬stätigt,
daß die vonBentley,
Gardner und Weizmann alsZwischenphase
zuml-Oxy-2-methylanthrachinon
mit Borsäureerhaltene
2'-Oxy-3'-methyl-2-benzoyl-benzoesäure
mit ihrero-Oxysäure,
die bei weiterer Kondensationl-Oxy-2-methyl-
anthrachinon
liefert,
identisch ist. Demnach kann also dieKonstitution
für diese beidenOxymethylanthrachinone
doch alssicher
gestellt gelten.
2*
Untersucht man, inwieweitdie im vorstehenden
dargelegten
Konstitutionsbeweise der
Monooxymonomethylanthrachinon- körper
zurAufklärung
der Konstitution unseres Mononitro-/Nmethylanthrachinons
benützt werdenkönnen,
soergibt
sichfolgendes:
Vorausgesetzt,
daß imMononitro-/?-methylanthrachinon
diebeiden Substituenten am
gleichen
Benzolkernsitzen,
so würdenvon den sechs
möglichen
isomerenMononitromonomethylanthra-
chinonen
jene
drei in Betrachtkommen,
bei denen dieCHa- Gruppe
sich in/?-Stellung
befindet. Römer und Link habenihr
Nitro-/?-methylanthrachinon
in einOxyderivat überführt,
dessen
Schmelzpunkt
sie bei 178° fanden. DieSchmelzpunkte
der drei isomeren
Monooxy-/?-methylanthrachinone
mitStellung
der Substituenten am
gleichen
Benzolkerne sind:3-Oxy-2 -methylanthrachinon (= 2-Oxy-3-methylanthra- chinon), Schmelzpunkt
nach Fraude260/262°.
ï-Oxy-3-methylanthrachinon, Schmelzpunkt
nachBentley,
Gardner und
Weizmann,
Ulimann undSchmidt,
Eder und Widmer 178°.l-Oxy-2-methylanthrachinon, Schmelzpunkt
nachBentley,
Gardner und Weizmann
185/186°.
Von diesen
Körpern
dürfte dererstgenannte
wegen seines hohenSchmelzpunktes
außer Betracht fallen für eineÜberein¬
stimmung
mit demOxy-Körper
von Römer undLink,
wennauch,
wie bereitsausgeführt,
hinsichtlich der Reinheit desKörpers
von Fraude nocheinige
Zweifel bestehen.Hinsichtlich des
l-Oxy-3-methylanthrachinons
haben Ederund Widmer
nachgewiesen,
daß dieserKörper entgegen
denAngaben
vonBentley,
Gardnerund Weizmann nicht überein¬stimmt mit dem
Oxy-Körper
von Römer undLink.
Die letzt¬genannten
Autorengeben
für ihrenKörper
zwar ebenfalls denFp.
178°an, Eder undWidmer konstatiertenaber,
beiWieder¬holung
desVersuches von Römer undLink,
daß diesemOxy- Körper,
wenn er reinvorliegt,
ein höhererSchmelzpunkt,
nämlich
180/181°
zukommt. Diese letztere Tatsache macht es nunwahrscheinlich,
daß derOxy-Körper
von Römer undLinkmit dem
obigen l-Oxy-2-methylanthrachinon
übereinstimmt.21
Immerhin ist noch im
Auge
zubehalten,
daß die beiden Sub- stituenten OH undCH3
auch an verschiedenen Benzolkernen des Anthrachinonmoleküls stehen können. Eineendgültige Abklärung
der Konstitution des
Mononitro-/?-methylanthrachmons
läßt sich als bei demgegenwärtigen
Stande unserer Kenntnisse derMono-oxymonomethylanthrachinone
noch nicht ohne weiteresfolgern.
b)Die
Anthrächinondiamine und die ausihnen durchKon¬densation mit o-Diketonen erhaltenen Azinfarbstoffe.
Terres*) nimmt,
wohlgestützt
aufHoldermann,
ebenfalls an, daß sich imMononitro-/?-methylanthrachinon
dieN02-Gruppe
in
1-,
dieCH8-Gruppe
in2-Stellung
befinde. Er erhält durchOxydation
desNitro-/5-methylanthrachinons
eine Nitroanthra-chinon-/S-carbonsäure,
die er durch Hoffmannsehen Abbau und Reduktion in einDiaminverwandelt,
welches er als1,2-Diamino-
anthrachinon bezeichnet. Dieses Produkt soll identisch sein mit einem
Diamin,
das man nach den D. R.P. 167410Bayer (1904)
und D.R.P. 170562
Bayer (1904)
erhält. Im D.R.P. 167410wird der Beweis
geleistet,
daß beim Nitrieren von*/?-Amino-
urethananthrachinon nur
o-Substitutionsprodukte
auftreten. Dienach
Abspaltung
des Urethanrestes erhalteneno-Nitroamino-
anthrachinone lassen sich lautD.R.P. 170562 leicht in o-Diamine überführen. Die in der Patentschrift für die beiden DiamineCO ""« CO
UcoJU
'ULcoJUnh!
angegebenen Kriterien,
wieLösungsfarbe
in konzentrierterH2S04
undeinigen
anderenLösungsmitteln,
lassen nicht einenstreng
wissenschaftlichen Schluß zu, ob der eine dieserKörper (das 1,2-Diamin)
wirklich identisch ist mit dem Diamin vonTerres. Es
ergibt
sich daher aus diesen beschriebenen Diaminen noch kein sicherer Konstitutionsbeweis für das vonTerres benützte
Ausgangsprodukt,
d. h. dasMononitro-/S-methyl-
anthrachinon.
l)
B.46,1634 (1913).
Terres verwandelt seinAnthrachinondiaminin einen blauen
Azinfarbstoff,
dasIndanthren,
von der FormelXO.
^Xic/V V
yCO.!/NH.
sTr T)
UJU
Das
gleiche
Indanthren entsteht bei der Kondensation von1,2-Diaminoanthrachinon
mitAlizarin,
während das2,3-Diamino-
anthrachinon mit demselben
Körper
einen braunenAzinfarbstoff liefert. Dasgleiche
Verhaltenzeigen
diese zweiDiaminkörper
auch bei der Kondensationen mit
einigen
o-Diketonen. Soviel über die Konstitution dieser Azinfarbstoffe bekanntist,
müssendie zu ihrer
Darstellung
verwendeten o-Diamine die beidenNH2-Gruppen
imgleichen
Kern und zwar ino-Stellung
zueinander enthalten. Aus dem Vorstehenden
ergibt sich,
daß imMononitro-/?-methylanthrachinon
wegen dessenÜberführbarkeit
ineinenblauen
Indanthrenfarbstoff, dieN02-Gruppe
wahrscheinlich in1-,
dieCH8-Gruppe
in2-Stellung
sichbefindet,
wenn auch nachdem
vorliegenden
Tatsachenmaterial der Beweis für diese Formeln noch nicht alsstreng
wissenschaftlichgeleistet gelten
darf. Als ziemlich sicher kann aber nach Vorstehendem wohl betrachtetwerden,
daß die beiden Substituenten imNitro-/?-methylanthrachinon
sich imgleichen
Benzol¬kern des Anthrachinonmoleküls befinden.
c) Die Monoaminoanthrachinonmonocärbonsäuren.
Terres erhält durch Reduktion seiner Nitroanthrachinon- carbonsäure
(siehe b)
mitNaaS
eine Aminoanthrachinoncarbon- säure vomFp. 286°,
die erentsprechend
dem von ihm alsl-Nitro-2-methylanthrachinon
bezeichnetenAusgangsmaterial
alsl-Aminoanthrachinon-2-carbonsäure bezeichnet. Vermutlich ist diese Säure identisch mit der Aminocarbonsäure vom
Fp.
ca.280°,
welche nach D.R.P. 247411 B.A.S.F.(1911)
aus 1-Chloranthra- chinon-2-carbonsäure durch Behandeln mit Ammoniak erhaltenwird. Da aber für die Konstitution der
angewandten
Chlor-anthrachinoncarbonsäure in
bezug
auf dieStellung-
des Chlors inderPatentschrift kein Beweis
vorliegt,
so kann daraus die Kon¬stitution des
Mononitro-/?-methylanthrachinons
ebenfalls noch nicht als erwiesen betrachtetwerden,
wenn auch wiederum einegroße
Wahrscheinlichkeit für die Formel(vergl.
FormelI,
S.11) spricht.
RolandScholl erhielt aus dem
Mononitro-/?-methylanthra-
chinon
(Körper
von Römer undLink)
ebenfalls eine Amino-anthrachinon-2-carbonsäure,
indem er die Reaktion nachAnalogie
des
Überganges
von o-Nitrotoluol in Anthranilsäure ausführtegemäß
demSchema:
C% C„,
^ ^COOK
^AN02 ^NOOH N^NO ^y \ANO,
Nach Terres soll diese Aminoanthrachinonsäure von Scholl mit der
seinigen
identisch sein. Aus dieserReaktion von Schollfolgt vornehmlich,
daß dieMöglichkeit
einerStellung
derN02-Gruppe
im nichtsubstituiertenKern beim
Mononitro-/?-methylanthrachinon
ziemlich
ausgeschlossen ist,
denn es istwenig wahrscheinlich,
daß derMechanismus dieserAnthranilsäuredarstellung
auf die Anthra- chinonreiheübertragen
werdenkönnte,
wenn dieN02-Gruppe
und die
CH8-Gruppe
nicht imgleichen
Benzolkern sitzenwürden,
in
gleicher
Weise wie bei der Anthranilsäure.d)
DieMonooxyanthrachinonmonocarbonsäuren.
Hammerschlag1)
hat sicheingehender
mit einer Mono-oxyanthrachinonmonocarbonsäure
befaßt. Die von ihm an¬gegebenen
Daten weichen aber von denen anderer Autoren etwasab,
sodaß man nicht erkennenkann,
ob er alsAusgangs¬
material a- oder
/3-Methylanthrachinon
in Händenhatte;
sehrwahrscheinlich handelte es sich um ein Gemisch der beiden.
Auch von anderen Autoren
liegen
für die isomerenOxyanthra-
chinoncarbonsäuren zum Teil recht unsichere
Angaben
vor. Es!)
B.11,
83(1878).
können aus denselben keine Beweise für die Konstitution des
Mononitro-/?-methylanthrachinons geschöpft
werden.Konstitutionsbeweis für das bei direkter Nitration als
Haupt¬
produkt
erhalteneMononitro-/?-methylanthrachinon.
Aus dem
jetzigen
Stande unserer Kentnisse der Anthra- chinonchemieergibt sich,
wie im vorstehendendargelegt,
nochkein wissenschaftlich
befriedigender,
einwandsfreier Beweis für die Konstitution desMononitro-/?-methylanthrachinons,
wennauch die Annahme als wahrscheinlichste
erscheint,
daß dieN02-Gruppe
im selben Kerne sich befindet wie dieCHg-Gruppe,
und zwar in
o-Stellung
zu dieser. Am wahrscheinlichsten ist die Formel:CO
NO«
(/ycoYycH8
k/\coA/
Auch die
Tatsache,
daß das Anthrachinon durch Nitration in a-Nitroanthrachinonübergeht
und daß dieCH3-Gruppe
ino-Stellung dirigiert,
macht diese Formel sehr wahrscheinlich.Die
Stellung: 1-Nitro-3-Methyl
ist sicherausgeschlossen,
dieStellung:
3-Nitro-2-Methyl
eventuell nochmöglich,
wenn auchnicht sehr wahrscheinlich.
Unter
Berücksichtigung
dieserErgebnisse
habe ich nunversucht,
aufmöglichst
einfache Weise für dieStellung
derN02-Gruppe
im/?-Methylanthrachinon
einenvollgültigen
Kon¬stitutionsbeweis zu liefern.
Zum
endgültigen
Konstitutionsbeweis für das Mononitro-/?-methylanthrachinon
sind nochfolgende
zweiFragen
einwand¬frei zu beantworten:
I. Ist die
Stellung
derN02-Gruppe
a- oder/?-?
II. Findet sich die
N02-Gruppe
im selben Kerne wie dieCHj-Gruppe?
Frage
I wurde infolgender
Weisegelöst:
Durch
Eliminierung
derGH3-Gruppe
imMononitro-/?-methyl-
anthrachinon können zwei Fälle eintreten:
25
1. Fall: es entsteht a-Nitroanthrachinon.
Bei
a-ständiger Nitrogruppe
kommen für das Mononitro-ß-methylanthrachinon folgende
Konstitutionen in Betracht:a) b) c)
CO ^ * CO
Y^iCH, /V VVch, Nitrogruppe
ina-Stellung
,coX) UscoA/
im zweiten Kern-CU LU
no^
Mög-lichkeit
b istausgeschlossen (vergl.
S.20).
2. Fall: es entsteht
/?-Nitroanthrachinon.
Bei
/J-ständiger Nitrogruppe
kommen für das Mononitro-/?-methylanthrachinon folgende
Konstitutionen in Betracht:a) b)
/\/COV'\rw Nitrogruppe
in/}-Stellung-
im zweiten Kern.
I I 1
*/^co^
Die
Entfernung"
derCH8-Gruppe
wurde dadurchbewerkstelligt,
daß das
Nitro-/J-methylanthrachinon
durch Chromsäure in sal¬petersaurer
Lösung
zurCarbonsäureoxydiert
wurde. EinVersuch,
durch Erhitzen des Kalksalzes derNitroanthrachinoncarbonsäure direkt das
entsprechende
Nitroanthrachinon zuerhalten,
führtenicht zum
Ziele.
Durch Reduktion mitZinnoxydulkali
entstehteine
Aminoanthrachiuon-/S-carbonsäure.
Aus demAg-Salz
der¬selben kann man nun in
analoger Weise,
wie dasWillgerodt
und
Maffezoli1)
bei der 2-Aminoanthrachinon-3-carbonsäureausgeführt haben,
durch Erhitzen leichtC02 abspalten.
DieC02-Abspaltung
in derAminoanthrachinon-/?-carbonsäure erfolgt,
wie ich
gefunden habe, quantitativ
auch schon leicht beilängerem
Erhitzen derNitroanthrachinon-/3-carbonsäure
mitüberschüssiger Zinnoxydulkalilösung.
Man erhält so dasentsprechende
Mono-amin. Dasselbe erwies sich in unserem Falle als a-Aminoanthra- chinon. Die
NOs-Gruppe
desMononitro-/?-methylanthra-
chinons befindet sich also in
a-Stellung.
») J.
pr.[2], 82,
205(1910).
Frage
II wurde wiefolgt gelöst:
DasNitro-^-methylanthrachinon wurde
in denentsprechenden Oxykörper
verwandelt und dieserverglichen
mit dem1-Oxy- 2-methylanthrachinon, welches,
wieBentley,
Gardner undWeizmann
angeben,
erhalten wird durch Kondensation vonPhthalsäureanhydrid
und o-Kresol mit Borsäure als Konden¬sationsmittel.
Übereinstimmend
mit denAngaben
von Eder undWidmerwurde nun der
Schmelzpunkt
für denOxykörper
von Römerund Link nach dessen
Reinigung
über dasAcetylderivat
eben¬falls zu
181/182° gefunden;
der durch Kondensation ausPhthal¬säureanhydrid
und o-Kresol mit Borsäure erhalteneKörper
er¬gab
denselben Wert.(Den
vonBentley,
Gardner undWeizmann
angegebenen Schmelzpunkt
von185/186°
konnteich nicht
erreichen.)
Der
Mischschmelzpunkt
der beidenKörper liegt
bei181/182°.
Damit ist die Identität dieser beiden
Körper
erwiesen. Darausfolgt,
daß in dem aus demMononitro-/9-methylanthrachinon
ab¬geleiteten Monooxy-/}-methylanthrachinon
dieOH-Gruppe
im selben Kerne stehen muß wie dieCH„-Gruppe.
Da aber nach I erwiesenist,
daß für dieNOa-Gruppe a-Stellung vorliegt,
sofolgt daraus,
daß demOxykörper
von Römer und Link dieStellung
einesl-Oxy-2-methylanthrachinons
zukommt. Damitist nun aber auch die Konstitution des bisher
einzig
bekanntenMononitro-/?-metbylanthrachinons endgültig aufgeklärt,
und wirhaben diesen
Körper
als einl-Nitro-2-methylanthrachinon
zu betrachten.
B. Dinitrokörper des /S-Methylanthrachinons.
Dinitro-/?-Methylanthrachinone
finden eine ersteErwähnung
im D.R.P. 131837 der B.A.S.F.
(1900).
DieDarstellung erfolgt
durch
längere Einwirkung
vonSalpeterschwefelsäure
auf/?-Methyl-
anthrachinon bei höherer
Temperatur.
Obwohl dieStellungen
der
Nitrogruppen
derReaktionsprodukte
imgenannten
Patent bereits bezeichnetwerden,
finden sich daselbst keineAngaben
über die