Philipps Universität Marburg Fachbereich 15: Chemie Experimentalvortrag
- Festkörper
- synthetisch hergestellte Makromoleküle (Polymere) - stets wiederholende Grundeinheiten (Monomere)
Abb.1: Kunststoffe
Gliederung
1. Historisches 2. Kunststoffarten
3. Kunststoffherstellung 4. Verwendung
5. Recycling
6. Schulrelevanz
1. Historisches
- 1531: Erfindung des Kunsthorns durch Wolfgang Seidel
- 1851: erster, mit technischen Mitteln, hergestellter Kunststoff Gummi (Goodyear)
- 1854: Förderung von Erdöl an die Erdoberfläche
- 1907: Herstellung von Bakelit aus Erdöl
Abb. 2: Vulkanisierungs- werkstatt
- 1922: Staudingers Theorie:
Kunststoffe sind aus Makromolekülen aufgebaut.
Geburtsstunde der Polymerchemie
- Herstellung von Plexiglas (1930), Polyvinylchlorid
(PVC; 1938), Nylon (1940), Polyethylen (PE) und Polypropylen (PP; 1956) - 1976: Entwicklung elektrisch leitfähiger Polymere
- ab 1980er Jahren: Herstellung von biologisch abbaubaren Polymeren
Abb. 3: Hermann Staudinger
(Quelle:
http://www.minerva.unito.it/Theatrum%20C hemicum/P2/Staudinger.htm)
2. Kunststoffarten
Versuch 1:
Erhitzen und Verformen von
Kunststoffen
weich und verformbar Makromoleküle
- van-der-Waals- und Wasserstoffbrücken- bindungen
- beim Erhitzen: gegenseitiges Verschieben der Bindungen
Duroplast - bleiben beim Erhitzen formstabil
- kovalente Querverbindungen
- Schwingungen werden beim Erhitzen unterbunden
Elastomer - leicht verformbar
- ziehen sich wieder in ihre Ausgangsform zurück
- kovalente Bindungen an manchen Stellen der Ketten
- „Verknäulung“
Demonstrationsversuch 1:
Trennung verschiedener Kunststoffe aufgrund ihres
spezifischen Gewichtes
Trennung verschiedener Kunststoffe aufgrund ihres spezifischen Gewichtes
Chemikalien:
Ethanol in Wasser (C2H5OH(aq) in H2O(l)) Dichte: 0,92 g/mL
Wasser (H2O(l)) Dichte: 1,0 g/mL
Natriumthiosulfat in Wasser (Na2S3O3(s) in H2O(l)) Dichte: 1,1 g/mL Natriumthiosulfat in Wasser (Na2S3O3(s) in H2O(l)) Dichte: 1,4 g/mL
- verwendete Kunststoffarten haben unterschiedliche Dichte
- Ein Kunststoff taucht in die Lösung ab, wenn seine Dichte größer als die der Lösung ist.
- Sortierung:
Polypropylen (PP) < Polyethylen (PE)
< Polystyrol (PS) < Polyethylenterephthalat (PET) Demonstrationsversuch 1:
Trennung verschiedener Kunststoffe aufgrund ihres spezifischen Gewichtes
3. Kunststoffherstellung
Darstellung von Kunststoffen
Polymerisation - radikalisch - ionisch
Polykondensation Polyaddition
Abb. 4: Plexiglas Abb. 5: Nylon Abb. 6: Polyurethan
Versuch 2:
Herstellung von Plexiglas
(Polymethylmethacrylat)
Versuch 2: Herstellung von Plexiglas (Polymethylmethacrylat) Chemikalien:
C O
O O
C O
Dibenzoylperoxid
Methacyrlsäuremethylester
Sudanrot
N N
N N O H
C
H 3 C H 2
O O
C H 3
(s)
(l)
(s)
C
H 3 C H 2
O O
C H 3
Polymerisation
O O
C H 3
Methacrylsäuremethylester Polymethylmethacrylat (PMMA)
(l) (s)
n n
Herstellung von Plexiglas
radikalische Polymerisation Gesamtgleichung:
DBPO
Dibenzoylperoxid
Phenylradikal Bildung des Startradikals:
Herstellung von Plexiglas - radikalische Polymerisation
•
• •
•
C O
O O C O
C O
O O C O
+
C O
O C
+
O C O1. Schritt: Kettenstart
2. Schritt: Kettenwachstum
• •
• •
C
+
H
H
C H 3
O
O
C H 3
H
H C
C H 3
O
O C H 3
H
H C
C H 3
O
O C H 3
H
H
C H 3
O
+
H
H
C H 3
O O H
H
C C H 3
O O
• •
H
H
C H 3
O O C H 3
H
H
C C H 3
O O
C H 3
+
H C H 3 H
O O C H 3 H H C
C H 3
O O C H 3
H
H
C H 3
O O H
H
C H 3
O O
H C H 3 H
O O H
C H H 3
O O
Herstellung von Plexiglas - radikalische Polymerisation 3. Schritt: Kettenabbruch durch Rekombination
3. Schritt: Kettenabbruch durch Disproportionierung
• •
H
H
C H 3
O O C H 3
H
H
C C H 3
O O
C H 3
+
H C H 3 H
O O C H 3 H H C
C H 3
O O C H 3
H
H
C H 3
O O H
H
C H 3
O O
H
H C H 3 H
O O H
C H 3 O
O C H 3
+
Plexiglas
lichtdurchlässig, kratzunempfindlich, fest Verwendung:
- Sicherheitsglas
- als Glas für Automobile und Flugzeuge - Kontaktlinsen, Brillengläser
- Uhren, Lupen, Linsen (Fotographie) - Medizin (Prothesen)
- Haushaltsartikel (Schüssel, Besteck)
Abb. 7: Kontaktlinse
(Quelle: http://www.kontaktlinsen- grohmann.de/linsen/linsen_hart.ht ml)
Abb. 8: Lupe
(Quelle: http://eflomi.de/vermisste- in-haiti-finden-aktion-gestartet/)
Abb. 9: Schüssel
(Quelle: http://www.kauf markt.cc/product_info.php/
Versuch 3:
Herstellung von Nylon 6.10
Versuch 3: Herstellung von Nylon 6.10 Chemikalien:
Sebacinsäuredichlorid
Hexamethylendiamin
Hexan (C6H14(l)) Wasser (H2O(l))
Phenolphtalein in Ethanol (C20H14O4(s) in C2H5OH(aq))
Cl O
O Cl
N H 2
N H 2
(l)
(s)
Polykondensation Gesamtgleichung:
- 2n HCl
Sebacinsäuredichlorid Hexamethylendiamin
Cl O
O Cl
+ H 2 N
N H 2
O
O
N H
N H
n n
n
Cl O
O Cl
N H 2
N H 2
O
N H Cl
O
O Cl
N
N H 2 H
H
Cl O
O N
N H 2 H
+ HCl
weitere
Polymerisation
sehr gute Elastizität, hohe Reißfestigkeit, fest Verwendung:
- Nylonstrümpfe
- hochwertige Kunststoffprodukte wie Getriebeteile und Knochenprothesen - Herstellung von Lacken und Klebstoffen
- Herstellung von Fallschirmen, Angelschnüren, Federbällen etc.
Abb. 11: Nylonstrumpfhose Abb. 10: Federbälle
(Quelle: http://www.seilnacht.com/Lexikon/k_polyam.html)
Versuch 4:
Herstellung von Polyurethan
Herstellung von Polyurethan
Polyaddition Gesamtgleichung:
n
n
Diisocyanat Diol Polyurethan
+
H O R 2O H O
R 2
O N H
O
R 1
N H O DABCO
O C
N R 1
N C
O
n
Herstellung von Polyurethan Chemikalien:
Lignin
Diphenylmethan-4,4-diisocyanat 1,4-Diazabicyclo[2.2.2]octan
(DABCO)
R1
R2 R
O C H 3 O
O R
O C H 3
O H O
O C H 3 H
N N
N N
C C
O O
(s)
(s)
(s)
Anlagerung von DABCO an den Dialkohol
δ-- δ+
δ-
δ++
δ-
δ- δ++
δ--
N N H
O R 2
O H N N H
O R 2
O H
N N H
O
R 2
O H O
C N
R 1 N
C
O O
C N
R 1
N O
O + R 2
O H H
N
Urethanbindung
Umlagerung eines Protons Entstehung einer Urethanbindung Herstellung von Polyurethan - Polyaddition
O C
N R 1
N O
O + R 2
O H H
N
N O
C N
R 1 N H
O O
R 2
O H
N N
n
Polyurethan
O
R 2
O N H
O
R 1
N H O
O C
N
R 1 N H
O O
R 2
O H
Schaumbildung (Nebenreaktion):
Kohlenstoff- dioxid
R N
C
O
+
H O H H 3 CN
C
O H
+
H O H 3 CN
O H O H
R
N H C
O
O H
R
NH 2 O
O
N H 2
R
+
O C OHerstellung von Polyurethan
unterschiedliche Eigenschaften, fest Verwendung:
- elastische Schaumstoffe (Schuhsohlen) - harter Schaum (Montageschaum)
- weicher Schaum (Möbelindustrie, z.B. Matratzen, Polster) - Skier, Autositze, Schläuche, Bowlingkugel
- Latexfreie Kondome
Abb. 12: Schwamm
(Quelle: http://www.seilnacht.
com/Lexikon/k_polyur.html)
Abb. 13: Skischuh
(Quelle: http://www.seilnacht .com/Lexikon/k_polyur.html)
Abb. 14:
Latexfreies Kondom
4. Verwendung
Polyethylen (PE) für Flaschen, Kästen, CDs…
Polyethylenterephthalat (PET) für Flaschen und Lebensmittelverpackungen Polypropylen (PP) für Lebensmittelverpackungen, Haushaltswaren etc.
- Kunststoffe in der Bauindustrie
Polyvinylchlorid (PVC) für Böden
Polypropylen (PP) für Gartenmöbel, Kunstrasen, Toilettendeckel etc.
Polyurethan (PU) und Polystyrol (PS) als Dämmstoffe - Kunststoffe in der Automobilindustrie
Demonstrationsversuch 2:
Leim aus Quarkbecher
- Quarkbecher = Polystyrol (PS) = unpolarer Thermoplast
unpolares Lösungsmittel
- Prinzip „Gleiches löst sich in Gleichem“
Quarkbecher aus PS ist in Toluol lösbar Viskositätszunahme - Klebefunktion aufgrund der Wirkung von Adhäsions- und Kohäsionskräften
Toluol
C H 3
5. Recycling
Wertstoffkreislauf der Kunststoffe - Energetische Verwertung
- Werkstoffliche Verwertung - Rohstoffliche Verwertung
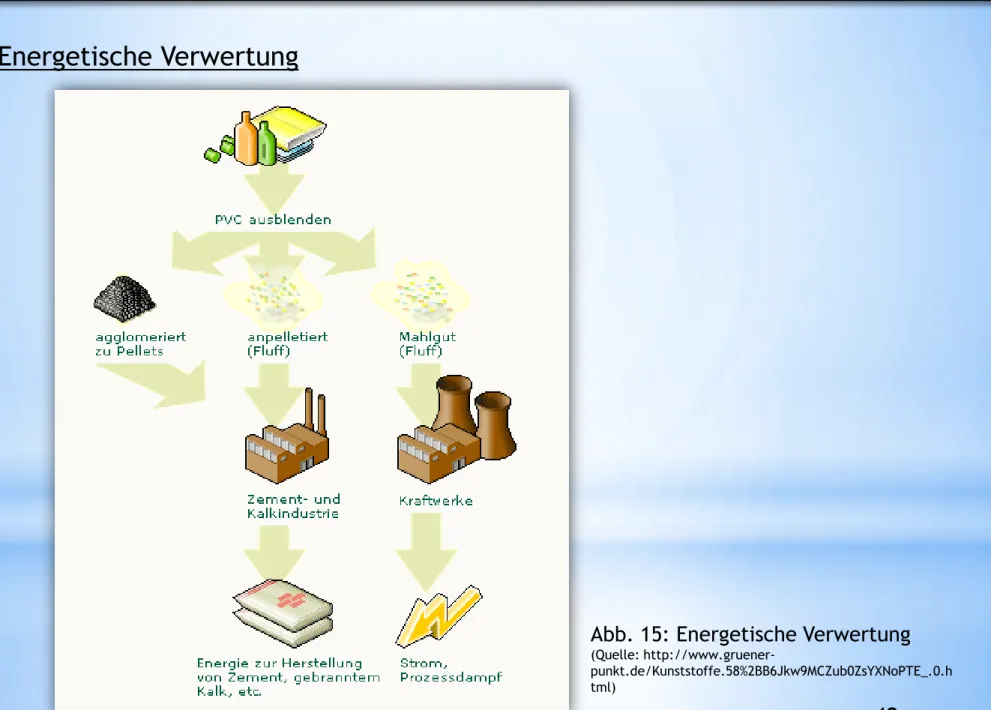
Abb. 15: Energetische Verwertung
(Quelle: http://www.gruener-
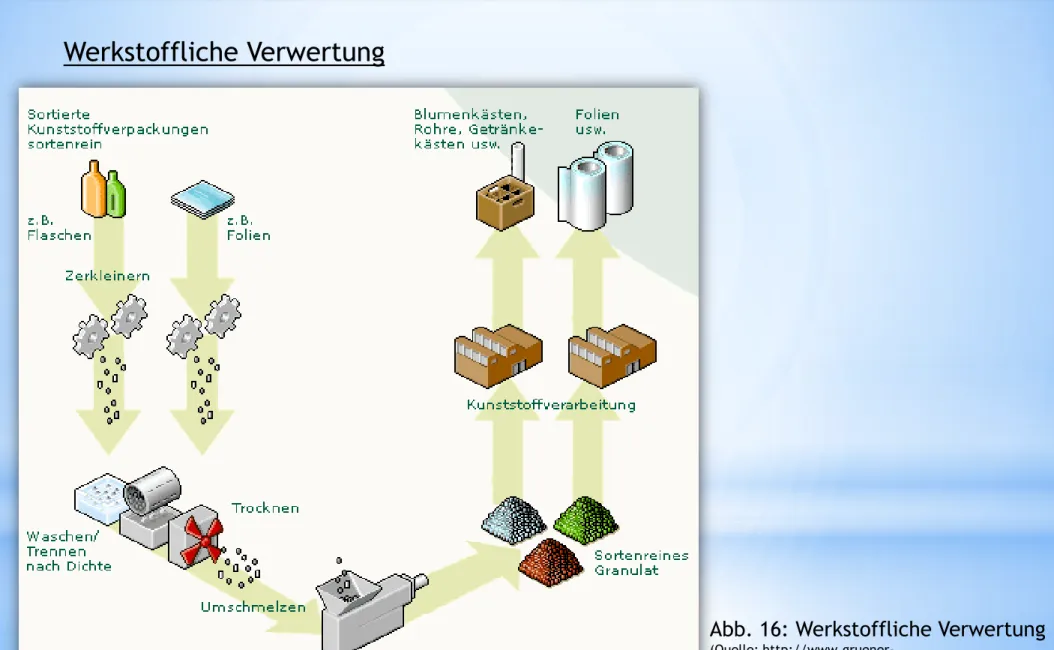
Abb. 16: Werkstoffliche Verwertung
Demonstrationsversuch 3:
Verformbarkeit eines
Thermoplasten
Verformbarkeit eines Thermoplasten
Aufbau Schmelzen des Thermoplasten Abkühlen/Erstarren
Abb. 17-20: Versuchsdurchführung
Abb. 21: Rohstoffliche Verwertung
Versuch 5:
Rohstoffliche Nutzung durch die Reduktion von
Metalloxiden
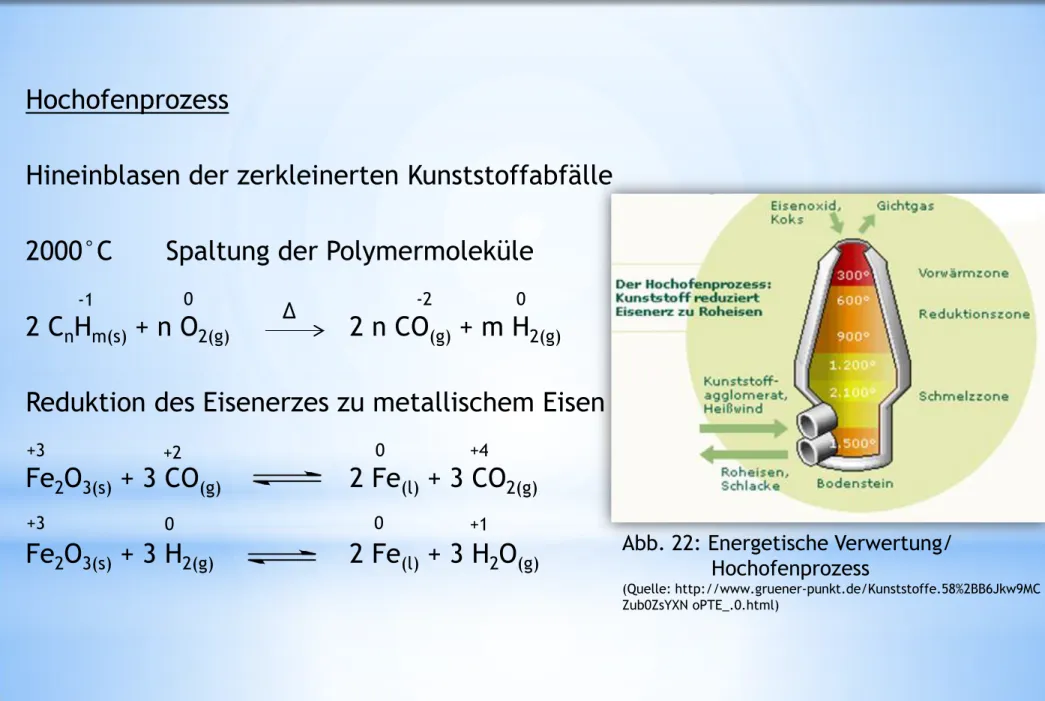
Hochofenprozess
Hineinblasen der zerkleinerten Kunststoffabfälle 2000°C Spaltung der Polymermoleküle
2 CnHm(s) + n O2(g) 2 n CO(g) + m H2(g)
Reduktion des Eisenerzes zu metallischem Eisen Fe2O3(s) + 3 CO(g) 2 Fe(l) + 3 CO2(g)
Fe2O3(s) + 3 H2(g) 2 Fe(l) + 3 H2O(g)
+3 0
+3 0
∆
+2 +4
0 +1
0 -2 0
-1
Abb. 22: Energetische Verwertung/
Hochofenprozess
(Quelle: http://www.gruener-punkt.de/Kunststoffe.58%2BB6Jkw9MC Zub0ZsYXN oPTE_.0.html)
- Kunststoffe = synthetisch hergestellten Makromoleküle (Polymere) - Kunststoffarten Thermoplast (verformbar)
Duroplast (nicht verformbar) Elastomer (elastisch)
- Kunststoffdarstellungen - Polymerisation, Polykondensation, Polyaddition - verschiedenste Verwendungsmöglichkeiten
- Recycling
Energetische-, Werkstoffliche- und Rohstoffliche Verwertung
6.Schulrelevanz
Klassenstufe 11 (LK/GK) – Thema: synthetische Makromoleküle (verbindlich) Klassifizierung von Kunststoffen (Versuch 1, Demo 3)
Aufbau von Makromolekülen (Versuch 2, 3, 4)
Reaktionstypen zur Verknüpfung von Monomeren zu Makromolekülen (Polymerisation, Polykondensation, Polyaddition) (Versuch 2, 3, 4)
Zusammenhänge zwischen Struktur und Eigenschaften (Versuch 1, Demo 3) Verwendung (Versuch 2, 3, 4; Demo 2)
Kunststoffabfälle, Recycling (Versuch 5, Demo 1)
Lehrplan Chemie G8
Klassenstufe 11 (LK) – Thema: Polymere mit besonderen Eigenschaften (fakultativ)
Klebstoffe (Demo 2)
Klassenstufe 12 (LK/GK) – Wahlthema: Angewandte Chemie (fakultativ) Thema: Werkstoffe – Natürliche und synthetische Makromoleküle
Kunststoffe: Klassifizierung (Duroplaste, Thermoplaste, Elastomere),
Zusammenhang: Struktur-Eigenschaften, Reaktionstypen zur Verknüpfung von Monomeren etc. (analog Klassenstufe 11)
52
Anonymus (2010): Lupe. Online im Internet: : http://eflomi.de/vermisste-in-haiti-finden-aktion-gestartet/.
[Stand: 03.07.2010].
Anonymus (2010): Nylonstrumpfhose. Online im Internet: https://www.preisroboter.de/ ergebnis4089274.html.
[Stand: 12.07.2010].
Appel, R. (2007): Hermann Staudinger. Online im Internet:
http://www.minerva.unito.it/Theatrum%20Chemicum/P2/Staudinger.htm. [Stand 02.07.2010].
Grohmann (2010): Kontaktlinse. Online im Internet: http://www.kontaktlinsen- grohmann.de/linsen/linsen_hart.html. [Stand: 03.07.2010].
Krüger, E. (1946): Vulkanisierungswerkstatt. Online im Internet:
http://de.academic.ru/pictures/dewiki/98/8f2310cc75db67de02dfe43052c09714.jpg. [Stand: 20.06.2010].
Seilnacht, T. (2010): Federbälle. Online im Internet: http://www.seilnacht.com/Lexikon/k_polyam.html. [Stand:
12.07.2010].
Seilnacht, T. (2010): Schwamm. Online im Internet: http://www.seilnacht. com/Lexikon/k_polyur.html. [Stand:
12.07.2010].
Seilnacht, T. (2010): Skischuh. Online im Internet: http://www.seilnacht. com/Lexikon/k_polyur.html. [Stand:
12.07.2010].
Quellen
Schreiter, S. et al.(2010): Energetische Verwertung. Online im Internet: http://www.gruener- punkt.de/Kunststoffe.58%2BB6Jkw9MCZub0ZsYXNoPTE_.0.html. [Stand: 13.07.2010].
Schreiter, S. et al.(2010): Rohstoffliche Verwertung. Online im Internet: http://www.gruener- punkt.de/Kunststoffe.58%2BB6Jkw9MCZub0ZsYXNoPTE_.0.html. [Stand: 13.07.2010].
Schreiter, S. et al.(2010): Werkstoffliche Verwertung. Online im Internet: http://www.gruener- punkt.de/Kunststoffe.58%2BB6Jkw9MCZub0ZsYXNoPTE_.0.html. [Stand: 13.07.2010].
Stolze, M. (2010): Kunststoffe. Eigenes Foto.
Stolze, M. (2010): Nylon. Eigenes Foto.
Stolze, M. (2010): Plexiglas. Eigenes Foto.
Stolze, M. (2010): Polyurethan. Eigenes Foto.
Stolze, M. (2010): Versuchsdurchführung. Eigene Fotos.
Vienna (2010): Latexfreies Kondom. Online im Internet: http://www.verhuet ungsmuseum.at/print.php?id=287.
[Stand: 13.07.2010].
Vuksan, N. (2010): Schüssel. Online im Internet: http://www.kauf markt.cc/product_info.php/products_id/4185.
[Stand: 08.07.2010].
- Gewinnung von Eisen (Fe); Fe2O3(s) Fe(s)
250°C Erze
400°C 3 Fe2O3(s) + CO(g) Fe3O4(s) + CO2(g) 700°C Fe3O4(s) + CO(g) 3 FeO(s) + CO2(g) 1200°C C(s) + CO2(g) 2 CO(g)
FeO(s) + CO(g) Fe(s) + CO2(g) 1600°C Fe(s) Fe(l)
2 C(s) + O2(g) CO2(g) 2300°C Abstich des Eisens
∆, C
0 0 +4 -2
+2 +2 0 +4
55
+3
+2 +2
+4