Einfache turbidimetrische Mikrolitermethode
zur Bestimmung der Sulfationenkonzentration im Serum und Urin - Referenzwerte, Stoffwechsel und diagnostische Bedeutung
Simple turbidimetric microliter method for determining the sulfate concentration in serum and urine - Reference values, metabolism and diagnostic relevance
F. Dreßler
Europäisches Institut für angewandte medizinische Forschung und Lehre, Kreischa/Sachsen
Zusammenfassung:
Es wird eine neuartige und einfache turbidimetrische Mikrolitermethode zur Bestim- mung der Sulfationenkonzentration im Serum und Urin beschrieben. Zur Sulfatpräzipi- tierung wird 4-Chloro-4'-aminodiphenyl benutzt, und die Trübungsmessung erfolgt photometrisch. Ergebnisse zur Präzision, Wiederfindung sowie Referenzwerte werden dargestellt und die diagnostische Bedeutung von Sulfat (Niereninsuffizienz, Proteo- glycan-/Glycosaminoglycansynthese, Biotransformation) diskutiert.
Schlüsselwörter:
Sulfat- Serum - Urin - Turbidimetrie - Referenzwerte - Diagnostik Summary:
A new and simple turbidimetric microliter method for the determination of the sulfate concentration in serum and urine is described. For the sulfate precipitation 4-chloro-4'- aminodiphenyl is used and the turbidity can be detected with a photometer. Resufts of the precision, recovery and reference values are described and the diagnostic relevance of sulfate (renal disease, synthesis of proteoglycane/glycosaminoglycane, and biotrans- formation) is discussed.
Keywords:
Sulfate - serum - urine- turbidimetry- reference value- diagnostics
Einleitung
Klinische Bedeutung
Sulfatanionen sind ein wichtiges Substrat für verschie- dene biochemische Prozesse bzw. Strukturkomponenten im Organismus. So .erfolgt die Biotransformation be- stimmter endogener Substanzen (Catecholamine, Tyra- min, Serotonin, Glucocorticoide, Androgene, Östrogene, Gallensäuren) sowie exogener Stoffe bzw. therapeuti- scher Xenobiotica (steroidale Antikonzeptiva, Analgetica, antiinflammatorischer Pharmaka, adrenergische Stimu- lantien und Blocker) auch durch Sulfatkonjugation (4, 13, 17,29, 38, 52, 60, 61,66). Desweiteren wird das Anion zur Synthese von Proteoglycanen bzw. Glycosaminoglycanen (2, 20, 24, 31, 34, 42) bestimmter Bindegewebsstrukturen, insbesondere der Knorpelmatrix und von Cerebrosiden der Myelinmembran im Gehirn (52, 57) benötigt. Die be- sondere Bedeutung des Sulfates während der Entwick- lungs- und Wachstumsphase wird durch den Sachverhalt
hervorgehoben, daß die Serumkonzentrationen von schwangeren Frauen, Föten, Säuglingen und Kindern (<3 Jahre) größer ist als bei Erwachsenen (7, 8, 10, 47, 64).
Die Sulfatkonjugation bzw. Sulfatierung erfolgt über das
„aktive Sulfat", das heißt über die Bildung von Phospho- Adenosin-3'-phosphat-5'-phosphosulfat (PAPS) unter Be- teiligung von Sulfotransferasen. Die intrazelluläre PAPS- Synthese erfordert neben Energie (2 Mol ATP) ein ausrei- chendes Angebot an Sulfationen, die vermutlich mit Hilfe eines Carriers aktiv im Austausch gegen Chlorid aus dem Serum entnommen werden können (3, 20, 51, 53, 57). Das vom Organismus benötigte Sulfat wird entweder durch enterale Resorption von anorganischen Sulfatsalzen oder von schwefelhaltigen Proteinen bzw. Aminosäuren (Me- thionin, Cystin bzw. Cystein) und Oxidation des Schwefels zu Sulfat (37, 53, 57, 64) gewonnen.
Die Ausscheidung des Sulfates erfolgt über die Niere. In
Analogie zum Creatinin kommt es bei Einschränkung der
glomerulären Filtrationsrate zu Hypersuifatämien (18, 22,
üooul(ioo) s«r IM +100 1(?0) 1,392 mol/1 PCS
Urin (RLW.St) tlOOOpl 0.255 mol/1 PCS mischen
*entrifugieren 7 ( ) überstand
»500 1(20 ) HiO (St)
50ul Oberstand
• HaO
200 1(100) Verdünnung 4·200 1(100) CAO-RL
in Küvette mischen nach O.5-1 m i n Messung der scheinbaren Extinktion
be i =430nm, d=lcm
Abb. 1: Analysenschema zur Bestimmung der Sulfationenkonzen- tration im Serum und Urin (RLW: Reagenzienleerwert, St: Stan- dard, PCS: Perchlorsäure, in Klammern Volumina bei Kapillarblut- abnahme)
45). Erhöhte Serumkonzentrationen werden auch bei Hyperthyreoidismus, in der Mitte des Menstruationscyc- lus, nach Proteinaufnahme, oraler Zufuhr von wäßrigen Sulfatlösungen (11, 43, 64) und möglicherweise nach Schwefelbädern (16) gefunden.
Erniedrigte Sulfatkonzentrationen im Serum verschiede- ner Tierspezies und beim Menschen werden durch be- stimmte Medikamente, insbesondere Salicylate und Para- cetamol, über eine erhöhte Sulfatausscheidung oder ver- mehrten Verbrauch bei der Sulfatkonjugation verursacht (19, 33, 35, 36, 48, 49, 67, 68, 71). Ein ungenügendes Sul- fatangebot beeinträchtigt die Synthese von wichtigen Strukturkomponenten in den Chondrozyten des Knorpels negativ. Es kommt zur Untersulfatierung der Glycosami- noglycane, das heißt die Proteoglycane enthalten weniger
Extinktion
150 S04 üL/moI/l]
Abb. 2: Einfluß der Perchlorsäure-Konzentration auf Sulfat-Stan- dardkurven ( Serum, D H
20, + 0,06 m, O 0,12 m, 0,23 m PCS;
Ansatz: WO Sulfatlösung + WO CAD-RL)
Extinktion
0,5 - 0,4 - 0,3 - 0,2 - 0,1 -
C-S04
20010 400
20 600
30 Serum jpmol/l]
Urin [mmol/Q
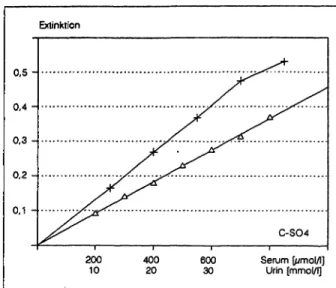
Abb. 3: Sulfat-Bezugskurven (+ Serum, Urin, Ansatz nach Abb. 1)
Chondroitinsulfat- und mehr nichtsulfatierte Chondroitin- Ketten (2, 23, 24, 27, 28, 31, 32, 34, 42, 68, 70).
Sulfatanalytik
Zur Sulfatbestimmung wurden bisher viele Methoden und Techniken, wie Photometrie (21, 62, 63, 69), Turbidimetrie (1,12,14,40,55), Flammenphotometrie (39), Atomabsorp- tionsspektrometrie (44), Radiometrie (46, 64), einfache Anionenaustauschchromatographie (6, 25, 56, 58) sowie HPLC (30, 50) entwickelt bzw. eingesetzt. Diese Verfahren sind aber für den routinemäßigen Einsatz, insbesondere in kleineren Laboratorien, auf Grund der notwendigen Spezialtechnik sowie des zum Teil hohen Arbeits- und Zeitaufwandes nur wenig geeignet. Außerdem bereitet die Sulfatbestimmung im Serum durch die notwendige Enteiweißung sowie Störungen von Fremdionen und an- deren Substanzen häufig Schwierigkeiten, so daß die bis- her getesteten photometrischen und turbidimetrischen Methoden nicht unproblematisch sind. Auch das von De Vries und Mitarbeitern (69) sehr ausgereift modifizierte Verfahren der photometrischen Sulfatbestimmung über Benzidin (kanzerogen).ist nicht sehr anwenderfreundlich und enthält mehrere und zum Teil schwierige Analysen- schritte.
Bei den turbidimetrischen Methoden mit Bariumionen ist die Niederschlagsbildung nur gering reproduzierbar und erfordert Zusätze zur Präzipitatbildung und -Stabilisierung (55). Demgegenüber scheint die Verwendung von 4-Chlo- ro-4'-aminodiphenyl (CAD) als Fällungsreagenz bezüglich Präzision, Empfindlichkeit sowie loneninterferenzen bes- ser geeignet zu sein. Allerdings ist die von Coleman und Mitarbeiter beschriebene Methode (12) nur für Sulfatbe- stimmungen in wäßrigen Lösungen geeignet. Eine Ana- lyse eiweißhaltiger Lösungen bzw. Serum ist derart nicht möglich.
Im folgenden wird eine schnelle und präzise Mikroliter-
methode mit CAD zur Bestimmung der Sulfationenkon-
106 Lab.med. 17: 106 (1993)
Tab. 1: Pr zision von Sulfatbestimmungen im Serum und Urin in der Serie
(n = 12)
Serumpool
* [μιτιοΙ/Ι]
s [μηηοΙ/Ι]
s [%]
SP1241 8,43,5
SP2372 9,82,6
von Tag zu Tag (n = 20) SP1245
12,6 5,1
SF2377 19,65,2
Urinpool
* [mmol/l]
s [mmol/ll
s [%]in der Serie
(n = 12)22,70,82 3,6
zentration im Serum und Urin vorgestellt, wobei die Tr - bungsmessung mit einem einfachen Photometer erfolgen kann. Desweiteren werden Referenzwerte sowie Ergeb- nisse zum Vergleich der Serumkonzentrationen von Sulfat und Creatinin mitgeteilt.
Material und Methoden
Reagenzien und L sungen
- Perchlors ure
1(PCS): 1,392 mol/l (Serum); 0,255 mol/l (Urin)
- Natriumsulfat
1-Standard: 50 μηηοΙ/Ι (Serum); 25 mmol/l (Urin)
- Pr zisionskontrollmaterialien: gepoolte Seren mit Sul- fationenkonzentrationen <300 μηηοΙ/Ι (SPD und >300 μηηοΙ/Ι (SP2); bei -20°C ber Monate haltbar
- 4-Chloro-4'-aminodiphenyl
2-Reagenzl sung (CAD-RL):
12,2 mmol/l CAD in 0,05 mol/l Salzs ure
1; bei Raum- temperatur ber Monate haltbar, gelegentlich filtrieren
1
Merck AG, Darmstadt
2Eigensynthese Analysenschema
Das Verfahren ben tigt nur wenige und unproblematische Analysenschritte (Abb. 1). Die Enteiwei ung und Verd n- nung wird einfach angesetzt, w hrend die Pr zipitatbil- dung von (CAD)
2SO
4in der K vette mehrfach durchge- f hrt werden kann und nach 30-60 sec abgeschlossen ist.
Bei der Bestimmung im Serum mu auf einen internen Standard und bei Urin auf einen w rigen Vergleichsstan- dard bezogen werden.
Ergebnisse und Diskussion
Analytik
Trotz vieler bekannter Varianten zur Enteiwei ung berei- tet die Adaption der Probenaufbereitung, insbesondere von Serum, an .die nachfolgende Pr zipitation der Sulfat- ionen erhebliche Schwierigkeiten (geringe Wiederfin- dung, Erh hung der L slichkeit des Pr zipitats durch S u- ren, Sulfatverunreinigung). Am besten geeignet erwies sich eine Deproteinisierung mit Perchlors ure, wobei al- lerdings einige Besonderheiten zu beachten sind. Einer- seits wird zur Enteiwei ung von Serum eine Mindestkon- zentration an Perchlors ure von ca. 0,232 mol/l ben tigt und andererseits tritt die L slichkeitsbeeinflu ung erst bei einer PCS-Konzentration von 0,05 mol/l nicht mehr auf (Abb. 2). Aus diesen Sachverhalten und aus Empfindlich- keitsgr nden darf daher bei der Serumanalyse nur ein kleines Volumen an Perchlors ure mit entsprechend ho-
her Konzentration zugesetzt werden, das anschlie end durch Wasserzugabe auf die zur Pr zipitierung notwen- dige S urekonzentration verd nnt wird. Die durch den Volumen-Verdr ngungs-Effekt (Verlust des Volumenan- teils der Proteine) auftretende Konzentrierung ist bei Ver- gleich mit Sulfatwerten, die ohne Enteiwei ung bestimmt wurden bzw. wo dieser Effekt zu vernachl ssigen ist, zu beachten und kann korrigiert werden (ca. 5% (59)). Eine weitere Besonderheit bei der Sulfatbestimmung im Serum ist der Bezug auf einen internen Standard, da der Anstieg im Serum gegen ber einer w rigen Sulfat- l sung etwas steiler verl uft. Dieser kann durch Zugabe einer Sulfatl sung, z.B. 50 μηηοΐ/l, statt Wasser zum ent- eiwei ten berstand hergestellt werden, oder der Bezug erfolgt auf einen eingestellten Serumpool bzw. ein Kon- trollmaterial mit bekannter Konzentration.
Die Sulfat-Eichkurven verlaufen im Serum bis ca. 800 μηηοΙ/Ι bzw. im Urin bis ca. 50 mmol/l linear. Bei h heren Konzentrationen wird mit Wasser entsprechend weiter verd nnt (Abb. 3).
Untersuchungen zur Pr zision des Verfahrens (Tab. 1) ergaben prozentuale Standardabweichungen in der Serie
<5% und von Tag zu Tag um 5%. Die Wiederfindung f r zum Serumpool 1 zugesetztes Sulfat betrug 103% (SP1 + 91 μΓηοΙ/Ι) bzw. 97% (SP1 + 182 μΓηοΙ/Ι).
Referenzwerte
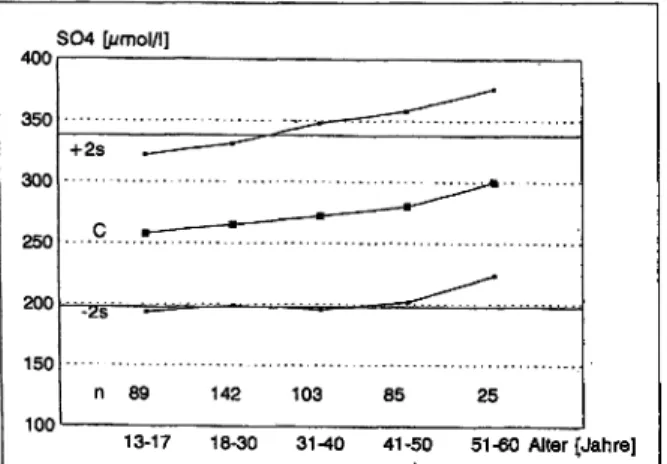
Zur Erhebung von Referenzwerten wurden im Rahmen von Gesundheitskontrollen Sulfatanalysen im Serum (morgentliche N chternblutabnahme) von 443 m nnliche Personen durchgef hrt. F r Erwachsene von 18-50 Jahre (nichtsignifikante Unterschiede der Altersgruppen) wurde ein Referenzwert von 268±35 μηιοΙ/Ι mit einem 2s-Bereich von 198-338 μηποΙ/Ι gefunden, was gut mit anderen Auto- ren bereinstimmt (30, 44, 58,64). Die Werte sind normal- verteilt (Abb. 4). Ein deutlicher Anstieg mit dem Alter, wie von Meier und Mitarbeiter (43) f r 25-65 Jahre beschrie- ben wird, kann derart nicht best tigt werden bzw. erfolgt erst ab 50 Jahre (Abb. 5). bereinstimmend zu Cole und Mitarbeiter (5) entsprechen die Serumwerte von Jugend- lichen (13-17 Jahre: 258±32 μπιοΙ/Ι) nahezu denen von Erwachsenen.
F r 24h-Sammelurin von erwachsenen M nnern (n = 24) wurde ein Referenzwert von 28,2±6,4 mmol/d ermittelt, der mit anderen Ergebnissen (40, 54) gut vergleichbar ist.
Sulfat-Creatinin-Vergleich
Von 160 Patienten mit Verdacht oder bekannter Nieren-
insuffizienz wurden die Serumkonzentrati nen von Sulfat
H ufigkeit
, 100η
20-
160 200 240 280 320 360 400 SO4 [μΓΤΐθΙ/1]
Abb. 4: H ufigkeitsverteilung von Serumsulfat bei Erwachsenen (18-50 Jahre)
3600 3000-
2600-
2000- 1600- 1000-
8O4 fyjmol/l]
Y(SO4)= 330 + 1,61X(CREA) r- 0.85 200 400 600 1000 1200 1400
CREA 0/mol/l]
Abb. 6: Korrelation der Serumkonzentrationen von Sulfat und Creatinin (Creatinin >ΊΟΟμΓηοΙ/1)
und Creatinin (Prikrins uremethode) bestimmt. Die ermit- telte Regressionsgerade (Abb. 6; Creatinin >100 μιτιοΙ/Ι) von y(S0
4) = 330 + 1,61x(Crea) mit einem Korrelations- koeffizient von 0,85 entspricht denen anderer Autoren (18, 45). Demgegen ber existiert im Creatininnormbereich keine Korrelation zum Sulfat (r = 0,07). Hierbei ist bemer- kenswert, da auff llig viele Sulfatwerte oberhalb der ge- fundenen 2s-Referenzgrenze liegen (Abb. 7). Dies stimmt mit Ergebnissen von H nze (22) berein, wonach Sulfat bereits bei Einschr nkung der glomerul ren Filtrations- rate (Creatininclearence) unter 75ml/min 1,75m
2, das hei t fr her als Creatinin, ansteigen soll. Hingegen fand Michalk bei Bezug auf die Inulinclearence (45) analog zum Creatinin einen Anstieg des Serumsulfates ab 50 ml/min 1,75m
2.
Die entwickelte turbidimetrische Mikrolitermethode ist auf Grund der einfachen und schnellen Analysendurchf h- rung sowie der Verwendung eines photometrischen Me - prinzips (scheinbare Extinktion) sehr gut f r den routine-
400 350 300 250 200
100
SO4 [μΓηοΙ/Ι]
^_^^
_^-~^~*
+2s . — ~~"^
c ^^^____^^
^
n 89 142 103 85 25
13-17 18-30 31-40 41-50 51-60 Alter [Jahre]
Abb. 5: Alterseinflu und 2s-Referenzbereich von Serumsulfat ·
m igen Einsatz in Laboratorien geeignet. Pr zision und Wiederfindung entsprechen den analytischen Anforde- rungen an klinisch-chemische Methoden. Die Analyse kann mit 100 μΐ Serum durchgef hrt werden, was Kapillar- blutabnahmen und damit geringere Belastungen, insbe- sondere bei Neugeborenen und Kindern sowie bei h ufi- gen Abnahmen, gestattet. Eine Teilautomatisierung der Analyse nach der Enteiwei ung ist m glich. Folgende An- wendungsbereiche von Sulfatbestimmungen k nnen f r Klinik und Forschung von Bedeutung sein:
- Bestimmungen bei Patienten mit glomerul rer Nieren- insuffizienz in Erg nzung zum Creatinin, insbesondere bei Verwendung der Pikrins uremethode, da diese durch viele St rfaktoren und Unspezifit ten beeinflu t wird (65).
- Kontrollanalysen bei Dialysepatienten bez glich der Einsch tzung der Sulfateliminierung (18, 30, 41), da er-
ftfi
C/Yl
ΛΛΛ
ΟΛΛ
200
1ΠΠ
3
S04 fei mol/l]
•
β ·
; v ;ί§ - . , - . « .
• · · · · ·
• " ; *· · -" ' " ·-
:·- * · - ' . . ' : · : - -
.
5' 45 55 65 75 85 95 CREA fy/mol/l]
Abb. 7: Korrelation der Serumkonzentration von Sulfat und Crea- tinin (Creatinin <100μηιοΙ/Ι)
höhte Sulfationenkonzentrationen im Serum einen Ab- fall des ionisierten Calciums bewirkt (bei 1 mmol/l Sul- fat verringern sich die Calcium-lonen um 0,017mmol/l (9)), und außerdem wird die renale Reabsorption von Calcium und Magnesium inhibiert (15), was insgesamt zur Entstehung der renalen Osteopathie beitragen kann.
Überprüfungen zum Einfluß verschiedener Medika- mente (vor allem nichtsteroidale antiinflammatorische Pharmaka) sowie Reduktionsdiäten (Elekrolyt- und Pro- tein- bzw. SH-Ammosäure-Mangel) auf das Serumsul- fat da diese zu Hyposulfatämien führen können und nach Maroudas und Mitarbeiter (42) bei Konzentratio- nen <200 / untersulfatierte und damit minderwer- tige Proteoglycane bzw. Glycosaminoglycane im huma- nen Knorpel synthetisiert werden (2, 24, 31, 34).
Schrifttum:
1. Berglund, F., Sörbo, B. (1960) Turbimetric analysis of inorganic sulfate in serum, plasma and urine. Scand. J. Clin. Lab. Invest. 12, 147-153.
2. Brand, H. S., Van Kämpen, G. P. J., Van de Stadt, R. J., Kuijer, R., Van der Korst, J. K. (1989) Effect of sulfate concentration on glycosaminoglycan synthesis in explant cultures of bovine articulare cartilage. Cell Biol. Int.
Rep. 13, 153-162.
3. Cabantchik, Z. I., Knauf, P. A., Rothstein, A. (1978) The anion transport System of red blood cells. The role of membrane protein evaluated by the use of probes. Biochim. Biophys. Acta 575, 239.
4. Campbell, N. R. C., Sundaram, R. S., Werness, P. G., Van Loon, J., Weinshilboum, R. M. (1985) Sulfate and methyldopa metabolism: Metabo- lite patterns and platelelet phenol sulfotransferase activity. Clin. Pharmacol.
Ther. 37,308-315.
5. Cole, D. E. C., Scriver, C. R. (1985) Age-dependet serum sulfate levels in children and adolescents. Clin. Chim. Acta 707,135-139.
6. Cole, D. E. C., Scriver, C. R. (1985) Microassay of inorganic sulfate in biological fluids by controlled flow anion chromatography. J. Chromatogr.
225, 359-367.
7. Cole, D. E. C., Shafari, J., Scriver, C. R. (1982) Inorganic sulfate in cere- brospinal fluid from infants and children. Clin. Chim. Acta 720,153-159.
8. Cole, D. E. C., Baldwin, L, Stirk, L. J. (1984) Increased inorganic sulfate in mother and fetus at parturition. Evidence for a fetal-to-maternal gradient.
Am. J. Obstet. Gynecol. 148, 596-599.
9. Cole, D. E. C., McPhee, M. D., Crocker, J. F. S. (1989) The hypocalcemic effect of inorganic sulfate infusions. Nephron 53, 78-80.
10. Cole. D. E. C., Evans, J. R., Raad, M., Hamilton, D. C. (1990) Inorganic sulfate metabolism in the very Iow birthweight infant. Biol. Neonate 57, 292-299.
11. Cole, D. E. C., Thurgpod, A. M., Whiting, S. J. (1991) Increased serum sulfate after protein loading in adult humans. Can. J. Physiol. Pharmacol.
69, 25-27.
12. Coleman, R. L, Shults, \Nri>„ Kelly, M. T., Dean, J. A. (1972) Turbidi- metriy via parallel photometric analysis. Determination of sulfate. Anal.
Chem. 44, 1031-1034.
13. Dessypris, A. G. (1975) Testosterone sulphate, its biosynthesis, metabo- lism, measurement, functions and properties. J. Steroid Biochem. 6, 1287-1298.
14. Dieu, J. P. (1971) Automated determination of urinary inorganic sulfates with the „Auto Analyzer". Clin. Chem. 77, 1183-1185.
15. McDougal, W. S., Koch, M. O. (1989) Effect pf sulfate on Calcium and magnesium homeostasis following urinary diversion. Kidney Int. 35, 105-115.
16. Dreßler, F., Käßner, R., Kresse, H. (1990) Zum Einfluß von Schwefel- bädern [Sulfosan(R)] auf die Sulfationenkonzentration im Serum und Urin von Patienten mit Erkrankungen des Stütz- und Bewegungsapparates.
Forschungsbericht, Rehabilitationszentrum Klinik Bavaria Kreischa für Bom- bastus-Werke GmbH Freital.
17. Forth, W., Henschler, D., Rummel, W. (1980) Pharmakologie und Toxiko- logie, Bibliographisches Institut, Mannheim, Wien, Zürich.
18. Freeman, R. M., Richard, C. J. (1979) Studies on sulfate in end-stage renal disease. Kidney Int. 75, 167-175.
19. Greiling, H., Schuler, B. (1963) Zur Wirkungsweise der Salizylsäure, Azetylsalizylsäure und des Salizylamids. Z. Rheumaforsch. 22, 47-56.
20. Greiling, H., Gressner, A. M. (1989) Lehrbuch der klinischen Chemie und Pathobiochemie. Schattauer, Stuttgart, New York.
21. Häkkinen, l. P. T., Häkkinen, L M. (1959) Spectrophotometric determina- tion of sulfate in serum and urine with barium chloranilate. Scand. J. Clin.
Lab. Invest. 77.294-297.
22. Hänze, S. (1966) Serumsulfat und Sulfatclearence bei normaler und ein- geschränkter Nierenfunktion. Klin. Wschr. 44,1247-1251.
23. Herman, J. H., Appel, A. M., Khosla, R. C., Hesse, E, V. (1986) The in vitro effect of select classes of nonsteroidal antiinflammatory drugs on normal cartilage metabolism.J. Rheumatol. 13,1014-1018.
24. Ito, K., Kimata, K., Sobue, M., Suzuki, S. (1982) Altered protepglycan synthesis by epiphyseal cartilages in culture at Iow S04 concentrations. J.
Biol. Chem. 257, 917-923.
25. De Jong, P., Burggraaf, M. (1983) Anion Chromatographie method for the simultaneous determination pf inorganic phosphate, bromide, nitrate and sulphate in human serum. Clin. Chim. Acta 732, 63-71.
26. Kaneko, M., Greiling, H. (1973) Hemmung des Sulfatstoffwechsels und der 3'-Phosphoadenylylsulfat: Chpndroitin-Sulfotransferase durch ein Glycosaminoglycanpolysulfat. Arzneim.-Forsch. (Drug Res.) 23, 737-740.
27. McKenzie, L. S., Horsburgh, B. A., Gosh, P., Tayler, T. K. F. (1976) Effect of anti-inflammatory drugs on sulphated glycosaminoglycan synthesis in aged human articular cartilage. Ann. Rheum. Dis. 35, 487-497.
28. McKenzie, L S., Horsburgh, B. A., Ghosh, P., Taylor, T. K. F. (1977) Sul- phated glycosaminoglycan synthesis in normal and osteoarthrotic hip carti- lage. Ann. Rheum. Dis. 36, 369-373.
29. Khan, F. S., Fothbery, K. (1983) Sulphation of contraceptiva steroids.
J.Steriod Biochem. 19, 1657-1660.
30. Koopman, B. J., Jansen, G., Wolthers, B. G. (1985) Determination of inorganic sulphate in plasma by reversed-phase chromatography using ultraviolet detection and its application to plasma samples of patients receiving different types of haemodialysis. J. Chromatogr. 337, 259-266.
31. Van der Kraan, P. M., Vitters, E. L, De Vries, B. J., Van den Berg, W. B., Van de Putte, L. B. A. (1988) Synthesis of aberrant glycosamino glycans during cartilage culture in „sulfate free" medium. J. Biochem. Biophys.
Meth. 75, 273-277.
32. Van der Kraan, P. M., De Vries, B. J., Vitters, E. L., Van den Berg, W. B., Van de Putte, L. B. A. (1988) Inhibition of glycosaminoglycan synthesis in anatomicaily intact rat patellar cartilage by paracetamol-induced serum sul- fate depletion. Biochem. Pharmacol. 37, 3683-3690.
33. Van der Kraan, P. M., De Vries, B. J., Van den Berg, W. B., Vitters, E., Van de Putte, L B. A. (1988) Effects of drug-mediated serum sulfate depletion on glycosaminoglycan synthesis. Agent. Action. 23, 55-57.
34. Van der Kraan, P. M., De Vries, B. J., Vitters, E. L., Van den Berg, W. B., Van de Putte, L. B. A. (1989) The effect of Iow sulfate concentrations on the glycosaminoglycan synthesis in anatomicaily intact articular cartilage of the mouse. J. Orthop. Res. 7, 645-653.
35. Van der Kraan, P. M., Vitters, E. L, De Vries, B. J., Van den Berg, W. B., Van de Putte, L. B. A. (1990) The effect of chronic paracetamol administra- tion to rats on the glycosaminoglycan content of patellar cratilage. Agent.
Action. 29, 218-223.
36. Krijgsheld, K. R., Scholtens, E., Mulder, G. J. (1981) An evulation of methods to decrease the availability of inorganic sulphate for sulphate con- jugation in the rat in vivo. Biochem. Pharmacol. 30, 1973-1979.
37. Krijgsheld, K. R., Galzenburg, E. J., Scholtens, E., Mulder, G. J. (1981) The oxidation of L- and D-cysteine to inorganic sulfate and taurine in the rat. Biochim. Biophys. Acta 677, 7-12.
38. Levy, G. (1986) Sulfate conjugation in drug metabolism: role of in- organic sulfate. Fed. Proc. 45, 2235-2240.
39. Leskovar, R., Weidemann, G. (1974) Flammenphotometrische Bestim- mung der freien Sulfationen im Serum. Z. Klin. Chem. Klin. Biochem. 72, 98-102.
40. Lundquist, P., Martensson, J., Sorbo, B., Ohman, S. (1989) Turbidimetry of inorganic sulfate, ester sulfate and total sulfur in urine. Clin. Chem. 26, 1178-1181.
41. Marangella, M., Petrarulo, M., Cosseddu, D., Vitale, C., Linari, F. (1991) Plasma profiles and removal rates of inorganic sulphate, and their influence on serum ionized calcium, in patients on maintenance haemodialysis. Clin.
Sei. 80, 489-495.
42. Maroudas, A., Evans, H. (1974) Sulphate diffusion and incorporation into human articular cartilage. Biochim. Biophys. Acta 333, 265-279.
43. Meier, M. S., Schmidt-Kessen, W. (1978) Untersuchungen über den Stoffwechsel des anorganischen Sulfates. Münch. med. Wschr. 720, 357-362.
44. Michalk, D., Manz, F. (1980) Determination of inorganic plasma sulfate by indirect atomic absorption spectrophotometry. Clin. Chim, Acta 707, 43-48.
45. Michalk, D. V. (1988) Der Stoffwechsel von Sulfat und Taurin in der Urämie. Habilitationsschrift, Universität Erlangen-Nürnberg.
46. Miller, E., Hlad, C. J., Levine, S., Holmes, J. H., Elrick, H. (1963) The use of radioisotopes to measure body fluid constituents. l. Plasma sulfate. J.
Lab. Clin. Med. 62, 710-714.
47. Morris, M. E., Levy, G. (1983) Plasma inorganic sulfate concentrations in pregnant woman. J. Pharm. Sei. 72, 715-716.
48. Morris, M. E., Levy, G. (1983) Serum concentration and renal excretipn by normal adults of inorganic sulfate after acetaminophen, ascorbic acid, or sodium sulfate. Clin. Pharmacol. Ther. 33, 529-536.
49. Morris, M. E., Kwon, D., Mansfield, l. L (1988) Sulfate homeostasis. l.
Effect of salicyclic acid and its metabolites on inorganic sulfate in rats. J.
Pharmacol. Exp. Ther. 244, 945-949.
50. Morris, M. E., Levy, G. (1988) Assay of inorganic sulfate in bilogical fluids by nonsuppressed (single-column) ion chromatography. Anal. Bio- chem. 772, 16-21.
51. Mulder, G. R., Scholtens, E. (1978) The availability of inorganic sulphate in blood for sulphate conjugation of drugs in rat liver in vivo. Biochem. J.
772,247-251.
52. Mulder, G. J. (1981) Sulfation of drugs and related compounds. CRC Press, Boca, Raton, Florida.
53. Mulder, G, J., Caldwell, J., Vonk, J., Van Kempen, G. M. J. (1982) Sulfate metabolism and sulfate conjugation. Tayle Francis, London.
54. Müller, T. (1984) Untersuchungen zum Sulfathaushalt von Normalper-
sonen und zur Kinetik oral und parenteral applizierten Sulfates. Dissertation, Rheinische-Friedrich-Wilhelms-Universtät, Bonn.
55. Pascoe, P. J., Peake, M. J., Waimsley, R. N. (1984) Determination of inorganic sulfate in plasma with a centrifugal analyzer, Clin. Chem. 30, 275-277.
56. Politi, L., Chiaraluce, R., Consalvi, V., Cerulli, N., Scandurra, R. (1989) Oxalate, phosphate and sulphate determination in serum and urine by ion chromatography. Clin. Chim. Acta 184,155-166.
57. Rapoport, S. M. (1987) Medizinische Biochemie. Volk und Gesundheit, Berlin.
58. Reiter, C., Müller, S., Müller, T. (1987) Improved method for the determi- nation of sulphate in human serum using chromatography. J. Chromatogr.
473,251-256.
59. Richterich, R. (1971) Klinische Chemie. Basel, München.
60. Smith, !„ Mitchell, P. D. (1974) The effect of oral inorganic sulphate on the metabolism of 4-hydroxyphenetylamine (thyramine) in man: Thyramine O-sulphate measurement in human urine. Biochem. J. 142,189-191.
61. Stiehl, A. (1975) Die Sulfatierung der Gallensäuren. Fortschr. Med. 93, 1092-1093.
62. McSwain, M. R., Watrous, R. J., Douglass, J. E. (1974) Improved methyl- thymol blue procedure for automated sulphated determinations. Anal.
Chem. 46, 1329-1331.
63. Swaroop, A. (1973) A micromethod for the determination of urinary inorganic Sulfates. Clin. Chim. Acta 46, 333-336.
64. Tallgren, L. G. (1980) Inorganic sulphates in relation to the serum thyro- xine level and in renal failure. Acta Med. Scand. Suppl. 640, 1-100.
65. Thomas, L (1988) Labor und Diagnose. Medizinische Verlagsgesell- schaft Marburg.
66. Tyce, G. M., Messick, J. M., Yaksh, T. L, Byer, D. E., Danielson, D. R., Rorie, D. K. (1986) Amine sulfate formation in the central nervous system. · Fed. Proc. 45. 2247-2253.
67. De Vries, B. J., Van der Berg, W. B., Van de Putte, L B. A. (1985) Sali- cylate-induced depletion of endogenous inorganic sulfate. Arthritis Rheum.
28, 922-929.
68. De Vries, B. J., Van den Berg, W. B., Vitters, E., Van de Putte, L. B. A.
(1986) The effect of salicylate on anatomically intact articular cartilage is influenced by sulfate and serum in the culture medium. J. Rheumatol. 13, 686-693.
69. De Vries, B. J., Vitters, E., Van den Berg, W. B., Schräm, D., Van de Putte, L B. A. (1987) Determination of small quantities of sulfate (0-12 nmol) in serum, urine, and cartilage of the mouse. Anal. Biochem. 163, 408-417.
70. De Vries, B. J., Van den Berg, W. B., Vitters, E., Van de Putte, L B. A.
(1988) Effects of NSAID on the metabolism of sulphated glycosaminogly- cans in healthy and (post) arthritic murine articular cartilage. Drugs 35, 24-32.
71. De Vries, B. J., Van der Kraan, P. M., Van den Berg, W. B. (1990) Decrease of inorganic blood sulfate following treatment with selected anti- rheumatic drugs: potential consequence for articular cartilage. Agent.
Action. 29, 224-231.
Anschrift des Verfassers:
Dr. rer. nat. Frank Dreßler
Europäisches Institut für angewandte medizinische Forschung und Lehre
Klinik Bavaria
August-Bebel-Straße 12 O-8216 Kreischa/Sachsen
110
Lab.med. 17: 110(1993)
weit gehören ebenso zu unseren Identitätsmerkmalen wie umweltge- rechtes Handeln.
Die Kooperation mit internationalen Universitäten, modernste Technologie, garantieren unvergleichliche Produkt- qualität.
Der intensive Kontakt zu Wissenschaft und Forschung ermöglicht es uns, Ihnen eine große Anzahl von wissen- schaftlich fundierten Publikationen zu unseren Kits zur Verfügung zu stellen.
Entdecken Sie die Vorzüge unseres Rund-um-Services.
Gerne senden wir Ihnen detaillierte Produktinformatipnen. Oder lassen Sie sich von einem unserer Außen- dienstmitarbeiter fachkundig beraten.
HGH-rCUA
Einfache 2 Stunden Inkubation
Sensitivität 0,02ng/ml CZ3 nicht Isotope,
nicht eniyrriatische , Methode "
E2J für Serum und Urin
Nichols .Institute
D i a g n o s t i k a G m b H D i e s e l s t r a s s e 1 8 . W - 6 3 5 0 B a d N a u h e i m '- 0 6 0 3 2 - 3 S 0 5 7
:Fax 0 6 0 3 2 - 3 5 0 5 0 . I h r S e r v i c e - P a r t n e r . i n der S c h w e i z :
N i c h o l s · I n s t i t u t e D i a g n o s t i c s .S.A.
l
•\
A Jugendarbeitsschutzgesetz, wenn regelmäßig mindestens ein Jugendlicher beschäftigt wird,
A Mutterschutzgesetz, wenn regelmäßig mehr als drei Frauen beschäftigt werden,
A die Arbeitszeitordnung in jedem Fall,
A die Unfallverhütungsvorschrift (Berufsgenossenschaft) in jedem Fall, A die Röntgenverordnung, wenn ein Röntgengerät betrieben wird, A das Bestandsverzeichnis oder Gerätebuch gem. Medizingeräte- verordnung, wenn energetisch betriebene med.-technische Geräte betrieben werden.
Jetzt bestellen!!
Coupon ausschneiden und einsenden an:
Verlag Kirchheim + Co GmbH, Postfach 25 24.
W 6500 Mainz 1 Telefon 0 61 31/9 60 70 32
(Arzte, Zahnärzte, Tierärzte) von W. M· Nentwig (Notar) und R· J. Gläser (Rechtsanwalt)
220 Seiten, Broschur, 45,- DM, ISBN 3-87409-195-3,6. Auflage
Eine komplette Sammlung aller Gesetze und Verordnun- gen, die in jeder Praxis ausgelegt werden müssen. Geld- bußen bis zu 1.000 DM drohen, wenn ausiegepflichtige Vorschriften dem (ohne vorherige Anmeldung in der Pra- xis erscheinenden) Beamten des Gewerbeaufsichtsamtes nicht vorgelegt werden können.
Kann ein Bestandsverzeichnis oder Gerätebuch nicht vor- gelegt werden, droht eine Geldbuße bis zu 10.000 DM!
Die Anschaffung dieses Werkes kann daher ohne Über- treibung als „Pflichtlektüre für jede Praxis" bezeichnet wer- den. Demgemäß sind die Anschaffungskosten selbstver- ständlich als Praxisausgaben steuerlich absetzbar.
Bei der 6. Auflage wurde neben geringfügigen Ände- rungen des Bundeserziehungsgeldgesetzes und der Medi- zingeräteverordnung inbesondere die Neufassung des Mutterschutzgesetzes berücksichtigt. Danach ist beispiels- weise das Überschreiten der Frist zur Mitteilung einer Schwangerschaft gegenüber dem Praxisinhaber dann un- schädlich, wenn es auf einem von der Frau nicht zu ver- tretenden Grund beruht und die Mitteilung unverzüglich nachgeholt wird. Deshalb ist die Kündigung einer Helferin auch dann unwirksam, wenn diese nicht innerhalb von zwei Wochen, nach Zugang der Kündigung ihre Schwan- gerschaft mitgeteilt hat, sofern ihr dies selbst beispiels- weise nicht bekannt war.
Darüber hinaus wurden in der 6. Auflage die Anschrif- ten und Zuständigkeitsbereiche der Gewerbeauf- sichtsämter überarbeitet und ak- tualisiert, sofern sich Änderungen ergeben haben, was inbesondere für die neuen Bundesländer zutrifft.
bestelle l < Nentwlg/Gläser: Die auslegepflichtigen Praxisvorschriften 6. Auflage 1993, ISBN 3-87409^95^3,45
rDM
XII
![Tab. 1: Pr zision von Sulfatbestimmungen im Serum und Urin in der Serie (n = 12) Serumpool * [μιτιοΙ/Ι] s [μηηοΙ/Ι] s [%] SP1241 8,43,5 SP2372 9,82,6](https://thumb-eu.123doks.com/thumbv2/1library_info/5133425.1659354/3.759.29.711.112.211/zision-sulfatbestimmungen-serum-urin-serie-serumpool-μιτιοι-μηηοι.webp)