Thomas Kuster 25. Januar 2007
1 N 2 O–NO y Antikorrelation
1.1 Abbildung 1 (A)
Das Lachgas (N 2 O) in der Stratosph¨ are stammt aus der Troposph¨ are.
In der Stratosph¨ are kann N 2 O durch folgende Reaktionen abgebaut werden (Brasseur und Solomon, 2005, Seite 329):
N 2 O + O( 1 D) → 2NO (1)
N 2 O + O( 1 D) → N 2 + O 2 (2) N 2 O + hν(λ ≤ 200 nm) → N 2 + O( 1 D) (3) Folgende Bildungreaktion ist bekannt:
N 2 + O( 1 D) + M → N 2 O + M (4)
Die Bildung von N 2 O (4), ist extrem langsam und kann daher vernachl¨ assigt werden. 5.8% (Hegglin u. a., 2005, Seite 8657) des N 2 O Abbau erfolgen durch die Reaktion (1), die beiden anderen Abbaureaktionen f¨ uhren zu Produk- ten ausserhalb der NO y -Familie und sind deshalb f¨ ur diese Aufgabe ohne Bedeutung.
Die globale Durchschnittskonzentration von N 2 O betr¨ agt 319.2 ppb (WMO, 2006, Seite 3), die maximale Konzentration in der tieferen Sratosph¨ are (X in Abbildung 1 (A)) kann daher ebenfalls maximal 319.2 ppb betragen.
Der Zusammenhang zwischen N 2 O und NO y ist linear, da aus der Reaktion (1) folgendes folgt (mit p = 5.8%):
[N 2 O] · p = − 1
2 · [NO y ] (5)
Aus Gleichung (5) folgt f¨ ur die Steigung:
m = −2 · p = −2 · 5.8% = 0.116 (6) Mit diesem Wert kann nun (Y ) berechnet werden:
[N 2 O] · 2 · p = 319.2 ppb · 2 · 0.058 = 37, 0 ppb (7) Diese Sch¨ atzung widerspricht der Abbildung 5.45 (Brasseur und Solomon, 2005, Seite 352) mit einem Wert von etwa 23 ppb.
1
y
[N 2 O] 1 · 2 · p = [NO y ] 1 (8) [N 2 O] 2 · 2 · p = [NO y ] 2 (9) (10) Mischen der Luftpakete ergibt f¨ ur das neue Luftpakete folgende Zusammen- setzung f¨ ur N 2 O: [N 2 O] 1 + [N 2 O] 2 und f¨ ur NO y : [NO y ] 1 und [NO y ] 2 . Die Addition von Gleichung (8) und (9) ergibt:
([N 2 O] 1 +[ N 2 O] 2 ) · 2 · p = [NO y ] 1 + [NO y ] 1 (11) wodurch kurz auf mathematische Weise gezeigt wurde, dass das neue Luft- paket ebenfalls auf der linearen Korrelation liegen muss.
1.3 Tiefe NO 2 und NO y Werte
Luftpakete mit tiefen N 2 O Konzentrationen stammen aus der h¨ oheren Stra- tosph¨ are oder sogar der Mesosph¨ are. Neben der bereits behandelten Reak- tion (1), kann N 2 O auch durch Reaktion (2) und (3) abgebaut werden. Die Reaktion (3) ist von kurzwelliger Strahlung abh¨ angig. Diese Strahlung ist in der oberen Startosph¨ are und Mesosph¨ are viel gr¨ osser, wodurch der Abbau von N 2 O beschleunigt wird.
Da NO y ebenfalls eine tiefe Konzentration aufweist, muss es auch Reaktionen geben die NO y abbauen. NO y liegt vorallem als NO vor in der Startosph¨ are (Brasseur und Solomon, 2005, Abbildung 5.38, Seite 344). Denkbar ist die Reaktion (4) (Bildung von N 2 O) und die Reaktion:
NO + hν → N( 4 S) + O (12)
in der das Gebildete N( 4 S) sofort mit einem weiterem N( 4 S) zu einem N 2 reagiert (N( 4 S) ist auch ein Mitglied der NO y -Familie (oder nicht?)).
1.4 Luftpakete der Mesosph¨ are und der mittleren Strato- sph¨ are mischen
Das Luftpakete in der Mesosph¨ are enth¨ alt weder N 2 O noch NO y und wird
mit einem Luftpaket der mittleren Stratosph¨ are gemischt (Abbildung 1 auf
der n¨ achsten Seite).
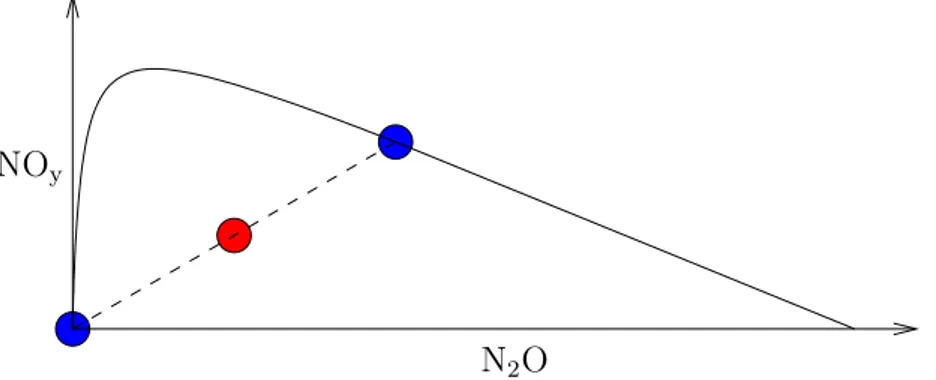
N 2 O NO y
Abbildung 1: Mischung der beiden blauen Luftpakete f¨ uhrt zum rotem Luft- paket
1.5 Wintermessungen in der Arktik
Im Graph gibt es einen Bereich mit einer tieferen NO y Konzentration als auf Grund der linearen Korrelation zu erwarten ist. Chemische Reaktionen wie in Aufgabe (1.3) k¨ onnen ausgeschlossen werden, da die N 2 O Konzentration hoch ist. Somit kommen nur noch physikalische Prozesse in Frage, dazu z¨ ahlt die Denitrifikation. Aus NO 3 und NO 2 bildet sich N 2 O 5 welches, durch eine heterogene Reaktion an der Oberfl¨ ache von Sulfat Aersolen oder falls es gen¨ ugend kalt ist an der Oberfl¨ ache von PSC, zu HNO 3 wird. Sedimentieren diese Partikel nun, f¨ uhrt dies zu einer Denitrifikation, da in ihnen nun HNO 3 enthalten ist (Brasseur und Solomon, 2005, Seite 349).
2 Effizienz von Denitrifikation und chemischen Pro- zessen
2.1 Sedimentationsrate von Supercooled Ternary Solution (STS) Tropfen
STS Tropfen bestehen aus HNO 3 , H 2 SO 4 und H 2 O. Die Massenanteile der drei Stoffe ist Temperaturabh¨ angig und betr¨ agt bei 192 K: HNO 3 :H 2 SO 4 :H 2 O
= 25%:25%:50% = 1:1:2 (Peter, 2006/2007).
Eine Temperatur von 192 K wird in der Stratosph¨ are ¨ uber der Antarktis bei einer H¨ ohe von etwa 25 km erreicht (Peter, 2006/2007). Da mir keine Werte f¨ ur die Arktis bekannt sind, wird 25 km also H¨ ohe verwendet. Die Anzahldichte ist in dieser H¨ ohe N = 9.6 · 10 17 # cm −3 .
Die Anzahl Aerosol betr¨ agt: N STS = 10 cm −3 (Peter, 2006/2007, Notiz) und die NO y Molek¨ ulanzahl: N NO
y= 5.90 · 10 9 cm −3 (Brasseur und Solomon, 2005, Seite 621f).
F¨ ur die Sinkgeschwindigkeit kann die Gleichung von Stokes verwendet wer-
Der Durchmesser des Partikels kann durch die Masse ausgedr¨ uckt werden:
V % = m (14)
1
6 πd 3 p % = m (15)
1
6 πd 3 p = m
% (16)
d p =
6m π%
13(17) Durch einsetzen von Gleichung (17) in (13) ergibt sich eine Gleichung f¨ ur v:
v = mg
3πη 6m
π%
13(18) Mit:
g = 9.81 m s −2 (19)
η = 2 · 10 −5 Pa s (20)
m = N NO
yN STS
· M HNO
3N A
· 4 (21)
= 5.90 · 10 9
10 · 63.02
6.022 · 10 23 · 4 g
# STS (22)
= 2.47 · 10 −13 g
# STS
(23) m tot
% = 0.25m tot
% HNO
3+ 0.25m tot
% H
2SO
4+ 0.5m tot
% H
2O
(24)
% =
0.25
% HNO
3+ 0.25
% H
2SO
4+ 0.5
% H
2O
−1
(25)
=
0.25
1.522 + 0.25 1.84 + 0.5
1.00 −1
g cm −3 (26)
= 1.25 g cm −3 (27)
folgt:
v = 2.47 · 10 −16 · 9.81 3π · 2 · 10 −5
6·2.47·10
−16π1250
13(28)
= 1.78 · 10 −5 m s −1 = 0.064 m h −1 (29)
2.2 Sedimentationsrate von Nitric Acid Trihydrate (NAT) Kristallen
Die Masse und die Dichte ¨ andern sich und auch die Anzahl der Partikel:
N NAT = 10 −4 cm −3 (30)
m = N NO
yN NAT
·
M HNO
3N A
+ 3 M H
2O
N A
(31)
= 5.90 · 10 9 10 −4 ·
63.02
6.022 · 10 23 + 3 18.01 6.022 · 10 23
g
# STS (32)
= 1.45 · 10 −8 g
# NAT
(33)
% =
M
HNO3M
HNO3+3M
H2O% HNO
3+
M
H2OM
HNO3+3M
H2O% H
2O
−1
(34)
=
0.54
1.522 + 0.46 1.00
−1
g cm −3 (35)
= 1.23 g cm −3 (36)
v = 1.45 · 10 −11 9.81 3π · 2 · 10 −5
6·1.45·10
−11π1226
13(37)
= 0.023 m s −1 = 82.2 m h −1 (38) Die NAT-Partikel sedimentieren viel schneller. Die Denitrifikation via NAT- Partikel ist viel bedeutender.
2.3 Effizienz der Chlorumsetzung an NAT und STS
In Aufgabe 2.1 und 2.2 wurde die Masse und Dichte berechnet. Mit diesen Daten kann der Durchmesser berechnet werden (Gleichung 17):
d p =
6m π%
13(39) Das totale Volumen ergibt sich dann wie folgt:
A STS/NAT = N STS/NAT · πd 2 p
STS/NAT
(40)
(39) = N STS/NAT · π
6m STS/NAT π% STS/NAT
23