Lab.med. 8:268-271 (1984)
Hb Ai c -Bestimmung
mittels Flüssigkeitschromatographie
Elizabeia Topio
Institut für Diabetes. Endokrinologio und Stoffwechselkrankheiten „Vuk Vrhovac", Medizinische Fakultät Zagreb (Direktor: Prof. Dr. mcd. Z Skrabalo, Dr. Sc.)
Zusammenfassung :
Es hat sich herausgestellt, daß glykolisiertes Hämoglobin ein neuer, sinnvoller Parameter zur Abschätzung der langfristigen Stoffwechseleinstellung des Diabetikers ist. Keine der zur Verfügung stehenden Methoden entspricht völlig den Forderungen analytischer und klinischer Praxis.
Wir haben uns mit einigen, wie wir glauben, noch nicht genug geprüften methodischen Aspekten der chromatographischen Nachweistechnik beschäftigt, unter anderem auch mit Fragen der Probenaufbereitung und Lagerung, sowie mit dem direkten Einfluß der Blutzuckerkonzentration auf die ermittelten Hb Afc- Werte.
Zusätzlich wurde die Möglichkeit der Probenaufbewahrung auf Filterpapier untersucht und mit der üblichen Technik in Entnahmeröhrchen verglichen. Die Ergebnisse zeigen eine gute Übereinstimmung der ermittelten Werte. Für epidemiologische Studien ist daher die Probenaufbewahrung auf Filterpapier gut geeignet Weitere Untersuchungen befassen sich mit der Differenzierung des Hb AIC in dem instabilen (Aldimin-Form) und stabilen (Ketoamin · Form) A n teil.
Schlüsselwörter:
Glykosyliertes Hämoglobin - Filterpapier - stabile und instabile Komponente - Chromatographie
Summary:
Glycosylated hemoglobin has been shown to be a new biologic criter/on in assessing the state ofa diabetic patient, but none ofthe available methods completely meets either analytical orclinicalpractice requirements.
Some still insufficiently investigated methodologic aspects ofthe Chromatographie technique were examinedf
including preparation and storing of the material, and the direct impact of glucose intake on Hb AIC. The possibility of collecting samples on a filter-paper was investigated. The results have shown that the Hb A\c
values in such a sample are equal to those from the test-tube, thus the analysis being proved more convenient for epidemiologic studies.
Keywords:
Glycosylated hemoglobin - filter-paper - stable and unstable components - chromatography
Einführung
Heute gibt es keinen Zweifel mehr, daß die Bestimmung des glykosylierten Hämoglobins ein neues biologisches Kriterium bei der Abschätzung der langfristigen Stoff- wechseleinstellung des Diabetikers ist (1-5).
Seine Quantifikation ist zweifach anwendbar: routinemä- ßig bei der Untersuchung von Diabetikern und außerdem zu Forschungszwecken.
Die Gruppe der glykosylierten Hämoglobine setzt sich - je nach dem angelagerten Kohlenhydratrest - aus den drei Anteilen Hb Aia, Hb A(b und Hb A|Czusammen. In der Regel erfolgt die gemeinsame Analyse aller drei Kompo- nenten als Hämoglobin AI (Hb AI = Hb Aia+b+c). Einige Untersucher führen auch die isolierte Bestimmung von Hb Aic durch. Während beim Hb Ajc Glukose an das Hä- moglobinmolekül angelagert ist, sind es bei den beiden anderen glykosylierten Hämoglobinen Hb A|a und Hb Aib Kohlenhydratreste aus dem Stoffwechsel.
Keine der zur Verfügung stehenden Methoden ist ideal, weil jede Vor- und Nachteile hat. Die Nachteile müssen mit viel Aufmerksamkeit in Betracht gezogen werden, um 268 Lab.med. 8: 268 (1984)
die Resultate genau interpretieren zu können. Eine von diesen Methoden ist die isolierte Bestimmung von Hb A|C
durch Flüssigkeitschromatographie, wobei hier methodi- sche Aspekte der chromatographischen Technik aufge- zeigt werden sollen. Das sind vor allem Probenaufberei- tung und -lagerung, sowie der direkte Einfluß der Gluko- sekonzentration auf die Höhe der ermittelten Hb A|C-Wer- te.
Material und Methoden Probenaufbereitung
Die Blutproben für die chromatographische Bestimmung von Hb Aic wurden nach zwei Verfahren abgenommen:
a) konventionell in EDTA-Röhrchen. Danach wird ein Aliquot mit physiologischer Kochsalzlösung im Über- schuß gemischt und die Erythrozyten abzentrifugiert. Der Überstand wird verworfen. Anschließend werden die Ery- throzyten mit Hämolysereagenz versetzt, darauf wird eine bestimmte/Menge Puffer zugegeben. Zellreste werden durch erneute Zentrifugation entfernt. Der klare Hämoly- satüberstand dient zur weiteren Analyse;
b) auf Filterpapier, in dem 50 Blut mit einer Mikropi- pette auf ein Stück Filterpapier gegeben wird (Whatman
*No. 1). Dies wird zur Trocknung bei Zimmertemperatur belassen. Die kommerziell erhältlichen Filterpapierstücke der Abbot Laboratories (Thyroscreen TM, Specimen Col- lection paper No. 5667) haben einen Kreis, in den die Probe mittels „End zu End Kapillaren" eingebracht wer- den kann. Vor der Analyse wird das Filterpapier in Aqua dest. gegeben und die Blutprobe während 15-30 min eluiert (Abb. 1). Ein Aliquot des Hämolysats dient zur weiteren Untersuchung.
Chromatographische Trennung
Das Prinzip der chromatographischen Trennung beruht darauf, daß aufgrund der Ladungsunterschiede zwischen den glykosylierten Hämoglobinen untereinander und ge- genüber dem nicht glykosylierten Hämoglobin die einzel- nen Fraktionen durch geänderte Pufferzusammensetzung nacheinander von der Säule eluiert werden können.
Vor zwei Jahren haben wir über eine modifizierte Säulen- chromatographische Trennung der glykosylierten Hämo- globine mittels dem Kationenaustauscher Bio Rex 70 und zwei Phosphatpuffern verschiedener pH-Werte und Osmolaritäten berichtet (6a). Dabei wurde die Methode von Trivelli so modifiziert daß eine kontinuierliche, auto- matische Sammlung der Hämoglobinfraktionen in kleinen Portionen durchgeführt wurde (7). Die Durchflußge- schwindigkeit betrug 1 ml/min unter Anwendung einer Peristaltikpumpe. Dabei wurde eine gute Trennung zwi- schen glykosyliertem und nicht-glykosyliertem Hämo- globin erreicht sowie die isolierte Abtrennung der Kom- ponente Hb A|C.
Unsere Methode ist aber nur für Forschungszwecke ge- eignet, da die Analysendauer von 90 min für eine Einzel- probe zu lange ist, um in der täglichen Routine Anwen- dung zu finden. Zur Verkürzung der Analysenzeit wurde die Mikrosäulentechnologie eingeführt. Sie ist heute die am häufigsten angewendete Methode zur Hb AI-Mes- sung (9-11).
Untersuchungen zur Hämolysataufbewahrung
Hierzu wurde das gleiche Hämolysat bei 4°C, -20°C und -80°C gelagert. Die Bestimmung erfolgte nach 1, 2 (nur bei +4°C), 5 und 21 Tagen. Dabei wurden Hb A|C
und Hb Aia+b getrennt bestimmt mittels HPLC, außerdem erfolgte die gemeinsame Bestimmung von Hb A|a+b+c mit Mikrosäulenmethode. Die Aufbewahrung von Vollblut- proben, die auf Filterpapier gesammelt wurden, erfolgte unter gleichen Bedingungen, die Analyse hier nur mittels Mikrosäulentechnik.
Differenzierung in Aldimin- und Ketoamin-Form In-vivo-Studien haben gezeigt, daß der Aldimin-Anteil des glykosylierten Hämoglobins mit steigender Blutzuk- kerkonzentration zunimmt.
Um nur die vom aktuellen Blutzucker unabhängige, sta- bile Ketoamin-Form bei der chromatographischen Be- stimmung zu erfassen, muß die Aldimin-Form vorher ent- fernt werden. Dies wurde erreicht durch Inkubation der Erythrozyten (aus den EDTA-Vollblutproben) in 0,9%
Kochsalzlösung bei 37°C über fünf Stunden vorder Ana- lyse.
Anstieg der Aldimin-Form
während des oralen Glukosetoleranztestes
Um das Ausmaß der Bildung der Aldimin-Form zu unter- suchen, wurde eine Gruppe von 38 Probanden einem oralen Glukosetoleranztest (OGTT) unterzogen. In den Ausgangsblutproben sowie nach 120 min erfolgte die Hb A|C-Bestimmung. Dabei wurde sowohl der stabile (Ke- toamin-Form) als auch der instabile Anteil (Aldimin- Form) ermittelt.
Ergebnisse
Probenaufbereitung
Die Ergebnisse der aus EDTA-Vollblutproben ermittelten H b Aic-Werte im Vergleich mit der Probensammlung auf
BLUTPROBE AUF FILTERPAPIER
BLUTELUATION AUS FILTERPAPIER
SÄULENCHROMATOGRAPHIE ABLESEN DER EXTINKTIONSWERTE
DENTIFIKATIONS DATEN
50>Jl ALIQUOT
destilliertes1ml
wasser :::::::::
ELUAT1
ELUAT2
Abb. 1: Chromatographische Bestimmung von Hb A/c aus Filterpapierproben
HbAj -PROZENT KALKULATION
Lab.med. 8: 269 (1984) 269
Filterpapier zeigt Abb. 2. Es besteht eine signifikante Korrelation zwischen zwei Materialsammeltechniken (r = 0,87, p < 0,005). Die Differenz zwischen beiden Methoden ist statistisch nicht signifikant (t - 1,78, p > 0,005). Die Überprüfung der Stabilität von Proben auf Filterpapier hat gezeigt, daß während Lagerung bei 4*C über 48 Std. keine Änderung der Hb Aic-Werte auf- tritt. Diese Art der Probensammlung könnte z. B. bei epi- demiologischen Studien zur Anwendung kommen, ähn- lich wie die Aufbewahrung von Proben auf Filterpapier zur Blutzuckerbestimmung (6).
Chromatographische Trennung
Durch die Mikrosäulenmethode wurde eine gute Tren- nung der glykosylierten Hämoglobine AI«, Aib und A|C
gemeinsam von nicht-glykosyliertem Hämoglobin A er- reicht. Eine isolierte Bestimmung der einzelnen glykosy- lierten Hämoglobinkomponenten erfolgte nicht, was ei- gentlich im Sinne der analytischen Präzision ein Verlust ist. Doch vom statistischen Standpunkt aus gesehen ist diese Technik ausreichend, weil die Korrelation zwischen der gemeinsamen Bestimmung aller glykosylierter Hämo- globine als Hb AI (= Hb Aia+t>+c) und dem isolierten Nachweis von Hb A|C sehr hoch ist (r = 0,92, p < 0,001) (8).
Die Methode ermöglicht schnelle Resultate, sie ist relativ preiswert und benötigt wenig Probenmaterial. Sie ist aber sehr empfindlich, was die Temperatur und Puffereigen- schaften (pH-Wert und lonenstärke) betrifft. In verschie- denen kommerziell erhältlichen Mikrosäulenverfahren sind Temperaturnomogramme beigefügt, mit denen eine
Umrechnung der bei verschiedenen Temperaturen ermit- telten Ergebnisse erfolgen kann.
Um optimale Resultate zu erhalten, wäre die beste Lö- sung, Säulen sowie Elutionspuffer vor dem Beginn der Analyse bei der erforderlichen Temperatur (je nach Her- steller zwischen 22* C und 24*C) zu äquilibrieren.
Die HPLC-Methode hat demgegenüber einige andere Vorteile (12,13). Sie erlaubt die Auftrennung der glyko- sylierten Hämoglobine voneinander in einzelne Fraktio- nen. Bio Rex 70, das hierzu auch verwendet wurde, ist zu weich, um mehrmals hohem Druck ausgesetzt werden zu können. Auf diese Weise kommt es zur Geldeformation, dadurch entstehen geänderte Durchflußraten mit der Folge falscher Resultate. In letzter Zeit wurde ein neuer Typ von hydrophober stationärer Phase für die H PLC syn- thetisiert. Er besteht aus kreuzartig vernetzten syntheti- schen organischen Polymeren, die wiederholt im HPLC- System benutzt werden können..Die Korrelation zwischen den mit Bio-Rex 70 ermittelten Werten ist groß (r = 0,86, p < 0,005). Nachteil der Methode ist der sehr hohe Preis der Ausrüstung.
Untersuchungen zur Hämolysataufbewahrung
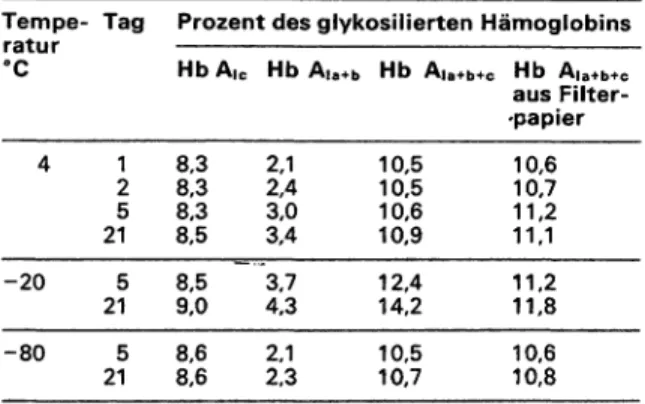
Tab. 1 zeigt den Einfluß verschiedener Temperaturen bei der Lagerung von Hämolysat und Proben auf Filterpapier.
Die Ergebnisse zeigen, daß durch Hämolysataufbewah- rung bei 4°C, -20°C und bei -80°C die Werte für das mittels HPLC bestimmte Hb A)c nicht beeinflußt werden.
Auffallend war der Anstieg der glykosylierten Hämoglo- bine Aia+bbei 4°C und -20°C. Der Anstieg dieser Frak-
HbA
lc12 · 11 - 10 - 9 - 8 7 -) 6 5
r = 0-98
~~" ' ' 1—— 1 1 1 1 1 1 1 1 1 1 5 6 7 8 9 10 11 12 . 13 U 15 16 17 18 19
MIKROSÄULEN CHROMATOGRAPHIE
Abb. 2: Korrelation zwischen dem mittels HPLC bestimmten Hb Alc aus frischem Hämolysat und dem mittels Mikrosäulen be- stimmten Hb AI (= Hb Aia+b+c) aus Filterpapierproben
270 Lab.med. 8: 270 (1984)
tionen ist wahrscheinlich die Ursache für den Anstieg, der beobachtet wurde, wenn eine gemeinsame Bestimmung 'aller glykosylierten Hämoglobine (= Hb Aia+b+c) mittels Mikrosäulentechnik durchgeführt wurde. Dabei war die Lagerung von Hämolysatproben bei 4°C während fünf Tagen noch ohne Einfluß auf das Ergebnis.
In Proben, die auf Filterpapier gesammelt wurden, änderte sich der nachweisbare Gehalt von dem mit Mikrosäulen bestimmten Hb Aia+t>+c bereits nach fünf Tagen während der Lagerung bei 4°C und -20°C.
Eine gute Probenstabilität sowohl bei der mit HPLC durchgeführten isolierten Bestimmung von Hb A!c und Hb Aia+b sowie der mit Mikrosäulen durchgeführten ge- meinsamen Bestimmung von Hb Äia+D+c bestand bei -80°C. Dies ist jedoch für Routineuntersuchungen nicht praktikabel.
Anstieg der Aldimin- Form
während des oralen Glukosetoleranztestes
Die Ergebnisse der Hb A|C-Bestimmung während der Durchführung des OGTT zeigt Tab. 2. Dabei wurde so- wohl der stabile (Ketoamin-Form) als auch der instabile (Aldimin-Form) Anteil untersucht. Es zeigt sich, daß es weder bei den stoffwechselgesunden Probanden mit nor- malem Ausfall des OGTT noch bei den Probanden mit diabetischem OGTT zu einem Anstieg der Hb Aic-Werte nach 120 min kommt, wenn nur die stabile Form bestimmt wird. Demgegenüber steigt die instabile Form durch den Blutzuckeranstieg im OGTT bereits nach 120 min an. Die- ser Anstieg ist um so deutlicher, je höher der Blutzucker- anstieg ist, er beträgt in der Probandengruppe mit diabe- tischem Ausfall des OGTT 2,5%. In dieser Gruppe beträgt das Verhältnis zwischen unstabilem und stabilem Anteil nur noch 1:4,2. Die Ergebnisse zeigen, daß bei raschen Tab. 1: Der Einfluß der Lagerungstemperaturen auf Hämolysat und Filterpapierproben
Tempe- Tag ratur
°C
4
-20
-80 12 215
215
215
Prozent des glykosilierten Hämoglobins HbAl c
8,38,3 8,38,5
8,59,0
8,68,6
Hb Ala+b
2,12,4 3,03,4
4,33,7
2,32,1
Hb A|a+b+c
10,510,5 10,610,9
12,414,2
10,510,7
Hb A|a+b+c
aus Filter- 'papier
10,610,7 11,211,1
11,211,8
10,610,8
Tab. 2: Verlauf der stabilen und instabilen Form des HbA,c beim oralen Glukosetoleranz-Test
Stabil Un- Unstabil stabil
Stabil Normale
OGTT- Werte
Diabetische OGTT-Werte
n - 16 n - 9 n - 13
1200 1200 1200
7,707,70 6,97,0 10,01 10,05
0,260,30 0,230,74 0,342,5
1 :29,6 1:25,7 1:301:9,45 1:291:4,2
Blutzuckerschwankungen eine deutliche Änderung der Hb Aic-Werte erfolgt, wenn die gemeinsame Bestimmung von stabilem und unstabilem Anteil erfolgt.
Es sollte daher auch in der Routinediagnostik nur der stabile Anteil glykosylierter Hämoglobine bestimmt wer- den.
Schlußfolgerungen
Für routinemäßige Hb A|C-Bestimmungen eignet sich die Probenaufbewahrung als Hämolysat bei +4°C, wobei zumindest über fünf Tage keine Änderung der Hb Aic- Werte auftritt. Bei epidemiologischen Studien könnte die Probensammlung auf Filterpapier erfolgen, allerdings muß dann die Lagerung bei -80°C erfolgen oder die Analyse nach zweitägiger Aufbewahrung bei +4°C.
Durch Inkubation von Erythrozyten in 0,9% NaCI bei 37°C über 5 Std. wird die Entfernung der direkt blut- zuckerabhängigen instabilen Aldimin-Form des Hb A|C
erreicht. Der isolierten Bestimmung des stabilen Hbic
sollte daher der Vorzug gegeben werden.
Schrifttum:
1. JOVANOVIC, L. PETERSON, C. M.: Clinical Utility of glycosylat hemoglobin. Am.
J. Med. 70. 331-338(1981).
2. McDONALD, J. M.. DAVIS, J. E.: Glycosylated hemoglobins and diabetes mellitus.
Human Pathology 10. 279-291 (1979).
3. GONEN, B.. RUBENSTEIN, A.H.: Hemoglobin A, and diabetes mellitus. Diabetolo- gia 15. 8(1978).
4. GABBAY. K. H., HASTY, K., BRESLOW, J. L. ELLISON. R. C., BUNN, H. F., GALLOP. P. M.: Glycosylated hemoglobin and long-term blood glucose control in diabetes mellitus. J. Clin. Endocrinol. Metab. 44. 859-864 (1977).
5. BUNN, H. F.: Evaluation of glycosylated hemoglobin in diabetic patients. Diabetes 30.613-617 (1981).
6. SOLAJIC-B02lCEVlC, N.. JAKSIC. 2.. MENIGA. A.. STAVLJENIC, A.: Enzymatic determination of glucose using blood collected on filier paper. Acta Pharm. Jugoslav.
26.317(1976)
7. TRIVELLI. L. A.. RANNEY, H. M.. LAI. H. T.: Hemoglobin components in patients with diabetes mellitus. N. Engl. J. Med. 284, 353-357 (1971).
8. TOPIC. E.. GRANlC. M.. PRASEK, M.. §KRABALO, Z.: Possible new criteria for diagnosis of diabetes mellitus. Abstr. XVI Annual Meeting of EDESG, Deidesheim, 1980.
9. ABRAHAM, E. C., HUFF. T. A., COPE. N. D.. WILSON. J. B.. BRANSOME, E. D., HUISMAN. T. H. J.: Determination of the glycosylated hemoglobin (Hb A,) with a new micro-column procedure. Diabetes 27. 931-937 (1978).
10. GAIN, Th.. HENDERKOTT, U., BOTTERMANN, P.: Ein Routineverfahren zur chromatographischen HbAIc-Bestimmung mittels Mikrosäulentechnik. Klin. Wschr.
59.219(1981).
11. WAJCMAN, H.. DASTUGUE, B., LABIE. D.: Quantitation of hemoglobin A1c: A rapid, aulomated precision-chromatography technique. Clin. Chim. Acta 92. 33-39 (1979)
12. COLE, R. A.. SOELDNER. J. S.. DÜNN, P. J.. BUNN, H. F.: A rapid method for the determination of glycosylated hemoglobins using high-performance liquid chromatography. Metabolism 27. 289-301 (1978).
13. DAVIS. J. E., McDONALD, J. M.. JARETT. l.: A high-performance liquid chroma- tography method for hemoglobin A1c. Diabetes 27,102-107 (1978).
14. TOPIC, E.: Glycosylated hemoglobins and diabetes mellitus. Doctoral dissertation, Zagreb University, Zagreb (1981).
15. GOLDSTEIN. D. E.. PETH. S. B., ENGLAND. J. D., HESS. R. L. DaCOSTA. J.:
Effects of acute changes in blood glucose on HbA1c. Diabetes 29. 623-629 (1980).
16. WIDNESS. J. A.. ROGLES-BROWN, T. L, McCORMICK. K. L, PEFZOLD. K. S..
SUSA J2B., SCHWARTZ. H. C.. SCHWARTZ, R.: Rapid fluctuations in glycohemoglo- bin (hemoglobin AIC) related to acute changes in glucose. J. Lab. Clin. Med. 95.
386-394 (1980).
17. DANEMANN. D., SCHANE, N.. BECKER. D.: In vitro glycoxylation of hemoglo- bin. Diabetes 29 (Suppl. 2). 119A (1980).
18. SVENDSEN. P. Aa., CHRISTIANSEN. J. S.. SOEGAARD. U.. WELINDER. B.
S.. NERUP, J.: Rapid changes in chromatographically determined hemoglobin AIC induced by short-term changes in glucose concentrations. Diabetologia 19.130-136 (1980).
6a TOPIC, E.: Chromatography determination of HbA,c: Reported at the HbA(c
Tagung, München, October, 1980.
Anschrift des Verfassers:
Dr. Sc Dipl-lng ehem. E. Topio Leiter des Klinischen Biochemischen Laboratoriums des Institutes Vuk Vrhovac Krijesnice bb
41 000 Zagreb/Jugoslawien
Lab.med. 8: 271 (1984) D 271