Polymere in Industrie & Technik
Experimentalvortrag
von Tobias Gerhardt
am 16.06.2010
Inhalt
1. Einleitung
2. Erstes industriell produziertes Polymer
• Versuch 1
3. Industrieübergreifende Polymere
• Demonstration 1
4. Verpackungs- und Lebensmittelindustrie
• Versuch 2 & 3
5. Medizintechnik
• Versuch 4
6. Elektrotechnik
• Demonstration 2
7. Bauindustrie
• Demonstration 3 & Versuch 5
Polymere
• Ketten von konstitutiven Einheiten, welche durch
kovalente, ionische oder Wasserstoffbrückenbindungen miteinander verknüpft sind
• diese Grundbausteine entstehen aus den Monomeren
• Polypropylen:
Monomer Grundbaustein (Propen) (konstitutive Einheit)
C
H2 CH3
CH3
n
Klassifizierung
• Molekulare Struktur:
–
Thermoplaste
• lineare oder verzweigte Polymere
–
Elastomere
• weitmaschig vernetzte Polymere
–
Duroplaste
•
Klassifizierung der Polymere
• Herkunft:
– anorganische Makromoleküle, z.B. Polyphosphate oder Silikone
– organische Makromoleküle
• natürliche Polymere (Biopolymere), z.B. Stärke, Cellulose, DNA
• chemisch modifizierte Polymere, z.B. Cellulosetrinitrat (Schießbaumwolle), Zelluloid
• synthetische Polymere, z.B. Polypropylen (PP), Polystyrol (PS), Polyvinylchlorid (PVC)
Vorbereitung für Versuch 5
• Temperaturmessung in den Bechergläsern
• aufbewahren in den Dosen
Erster industriell produzierter Kunststoff
• Anfang des 20. Jahrhunderts:
Versuche zur Herstellung elektrischer Isolatoren durch die Phenol-Formaldehyd-Kondensationsreaktion
• Schellack: natürliches Harz aus den Ausscheidungen der Lackschildlaus war sehr teuer
• Kautschuk brannte bei hohen Strombelastungen durch
• Baekeland gelang bei Experimenten mit Phenol und Formaldehyd die Herstellung eines harten Kunstharzes (1905 - 1907)
Erster industriell produzierter Kunststoff
• elektrisch nicht-leitend und beständig gegen Säure und Hitzeeinwirkung
• Hitze-Druck-Patent (1907) zur Produktion von Bakelit
• selbstentwickelter Bakelizer ermöglichte ihm die Temperaturführung unter
Überdruck
Versuch 1 - Bakelit
• Deprotonierung des Resorcins und SE-Ar mit Formaldehyd
• Anlagerung eines zweiten Resorcinmoleküls
OH
OH
- H2O + OH-
O
OH H O-
O-
OH O- OH
OH
O
H H
O-
OH
OH O- O
OH OH - OH- H
O
OH CH2
O-
OH
Versuch 1 - Bakelit
O
O
O O
O O
O
H
H
H H
H
H H
H
O- OH
OH OH
O OH
OH OH
CH2
O
H H
- OH-
Bakelit
• der hohe Vernetzungsgrad bedingt die Widerstandsfähigkeit dieses Duroplasten
• früher: Isolatoren für Hochspannungsleitungen, Aschenbecher, ...
• heute: mechanische und thermische Belastbarkeit, Brandresistenz, chemische Beständigkeit Schleifscheiben, elektrische Isolatoren, flammenhemmende Bindemittel in Schaumstoffen
Abb. 6: Fernsprech- apparat W48
Abb. 5: Schaltersystem aus Bakelit
Plexiglas
Polymethylmethacrylat (PMMA)
• amorpher, thermoplastischer Kunststoff
• glasklar, witterungsbeständig, hart, leicht
• 1928 von Otto Röhm patentiert und seit 1933 industriell produziert
• sehr gute optische Eigenschaften führen zur Verwendung als Lupen, Prismen und Linsen (bereits 1933)
• beständig gegen die meisten Chemikalien
• brennbar, wobei ein süßlicher fruchtiger Geruch entsteht
Demonstration 1 - PMMA
Polymethylmethacrylat
• industrielle Herstellung nur durch radikalische Polymerisation von Methylmethacrylat
• Bildung des Startradikals durch Erwärmen
O O
O O
O
2 O 2 + C
O
O
2
Polymethylmethacrylat
•
Kettenstart
•
Fortpflanzung
C
H2 CH3 O O
CH3
+
C
CH3 O O
CH3
C O O
CH3
C
H3 H3C H3C O O
CH3
O O CH3
O O CH3
CH3 C
CH3 O O
CH3
+
C
H2 CH3 O O
CH3
Polymethylmethacrylat
• Abbruchreaktionen
–
Rekombinationen
–
Disproportionierung
R1 C
CH3 O O
CH3
R2 C C H3
O O
CH3
+
O CH3
C H3
O CH3
CH3 O O
R1 R2
C O O
CH3
O O CH3
C
O O
CH3
O O
CH3
O O CH3
O O CH3
O O
CH3
O O
CH3
+
Polymethylmethacrylat
• Änderung der Eigenschaften durch Einbau anderer Grundbausteine ( Copolymere)
– mit < 10 Massenprozent Butylacrylat ergibt sich schlagfestes PMMA
• auch reines PMMA besitzt bereits eine sechsmal höhere Schlagzähigkeit als Glas bei einem
deutlich geringeren Gewicht
C H2
O CH3
O
Industrieübergreifendes Polymer
• Copolymerisate von PMMA sind relativ teuer und werden nur dort eingesetzt, wo die
Qualität entscheidend ist
– Verglasung von Flugzeugen, Aquarienschaufenster
• homopolymeres PMMA: Brillengläser, Autoleuchten, Rohre in der Getränkeindustrie
Abb. 7: Schaufenster Monterrey Bay Aquarium
Verpackungs- und Lebensmittelindustrie
• Polymethylmethacrylat (PMMA): Rohre
• Polyethylentherephthalat (PET): Getränkeflaschen
• Polytetrafluorethylen (PTFE):
Pfannenbeschichtungen (Teflon)
• Polystyrol (PS): Joghurtbecher und
Verpackungsmaterial (Styropor)
Versuch 2 - Styropor aus Joghurtbechern
• Gleiches löst sich in gleichem: Polystyrol und Essigsäureethylester sind unpolar
• in Pentan erfolgt Agglomeration
• Pentan dringt in die Zwischenräume ein und umgibt die Polymerketten vollständig
C
H3 O O
CH3
H H H H
Versuch 2 - Styropor aus Joghurtbechern
• Erhitzen des Agglomerats führt zur Verdampfung von Pentan (Sdp.: 36 °C) und Aufblähung des Polystyrols
• 1839 von Eduard Simon als unvorhergesehenes
Polymerisationsprodukt von Styrol (aus dem Storax- Baum) entdeckt
• Erst 1931 von I.G. Farben großtechnisch produziert
Polystyrol
•
Radikalische Polymerisation von Styrol
CH
+
C H2
+
C H2
CH CH
H H H H
Polystyrol
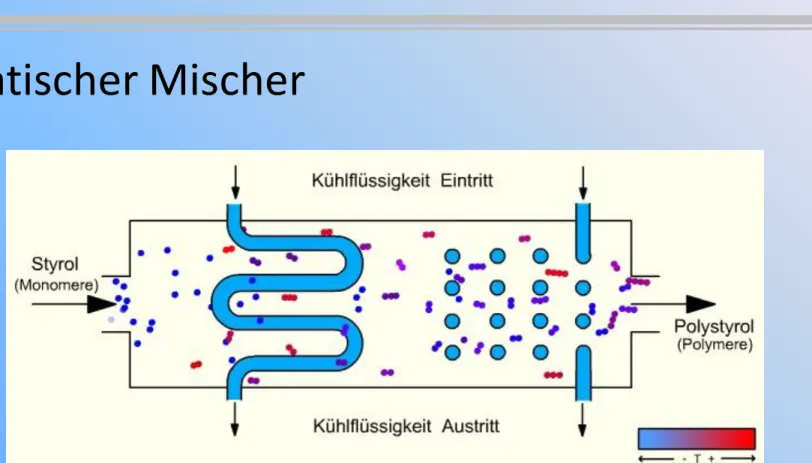
• Statischer Mischer
Abb. 8: Statischer Mischer
Polystyrol
• harter, glasklarer und spröder Kunststoff
• problemlose Verarbeitung (Thermoformen) und günstiger Preis:
– Elektro- und Automobiltechnik, Haushalts- und
Spielzeugartikel, (Lebensmittel-) Verpackungen, etc.
Abb. 9: Polystyrol- granulat
Biopolymere in der Industrie
• z.B. Stärke, DNA, Naturkautschuk
• Stärke: Homoglykan mit zwei Strukturformen
– Amylose (20-30 %), Helix – Amylopektin (70-80 %),
stark verzweigte Struktur
Abb. 10: Amylose (links)
Versuch 3 - Essbares Einweggeschirr
• Stärke und Mehl wirken als Superabsorber und Verdickungsmittel, d.h. sie nehmen
Wasser auf und binden es in ihren Strukturen
Erhöhung der Viskosität
• beim Erhitzen siedet das Wasser und die
Masse quillt auf, wird gelartig und erstarrt
beim Abkühlen
Versuch 3 - Essbares Einweggeschirr
• die Blasen entstehen durch die thermische Zersetzung von Natriumhydrogencarbonat (NaHCO
3):
2 NaHCO
3(s) Na
2CO
3(s)+ CO
2(g) + H
2O
(g)Essbares Einweggeschirr
• Einweggeschirr aus Stärke ist biologisch abbaubar und schont somit die Umwelt mehr als Kunststoff- oder
Pappteller etc.
• Entsorgung durch Verbrennung, Kompostierung, Biovergasung, evtl. Tierfutter
• es kann auch verzehrt
werden, besitzt aber häufig keinen Eigengeschmack
Medizintechnik
• Forschung begann gegen Ende des zweiten Weltkriegs aufgrund geringer Antireaktionen auf Kriegswunden mit Kunststoffsplittern
• biostabile Prothesen/Implantate
– Kunststoffzähne, die mit zahnfleischfarbenem Kunststoff verbunden sind
• chirurgisches Nahtmaterial & Klebstoffe für Wunden
– leicht aufzutragen und versiegelt innerhalb von Sekunden ohne Anästhesie
Versuch 4 - Drug delivery system
• Aspirin wird aus dem Haupt- wirkstoff (Acetylsalicylsäure) und Zusatzstoffen zu
Tabletten gepresst
• polare Verbindung wasserlöslich durch
Ausbildung von Wasserstoffbrückenbindungen
O CH3 O
OH O
Drug delivery system
• Acetylsalicylsäure kann Magengeschwüre und schwere Magenblutungen verursachen, die im schlimmsten Fall den Tode herbeiführen
• Trägermaterialien für Pharmaka gesucht, die den Wirkstoff nur an bestimmten Zielorten freisetzen magensaftresistente Überzüge
• Hydrogele als pH-responsive Aktuatoren, d.h. zur pH- abhängigen Steuerung von Flüssen durch Mikrokanäle
Drug delivery system
• Polymere mit Carboxygruppen pH-abhängiges Löseverhalten
– sie gehen bei pH > 6 in die lösliche Salzform über
• z.B. superabsorbierende Polymere der Acrylsäure
O OH
C H2
Drug delivery system
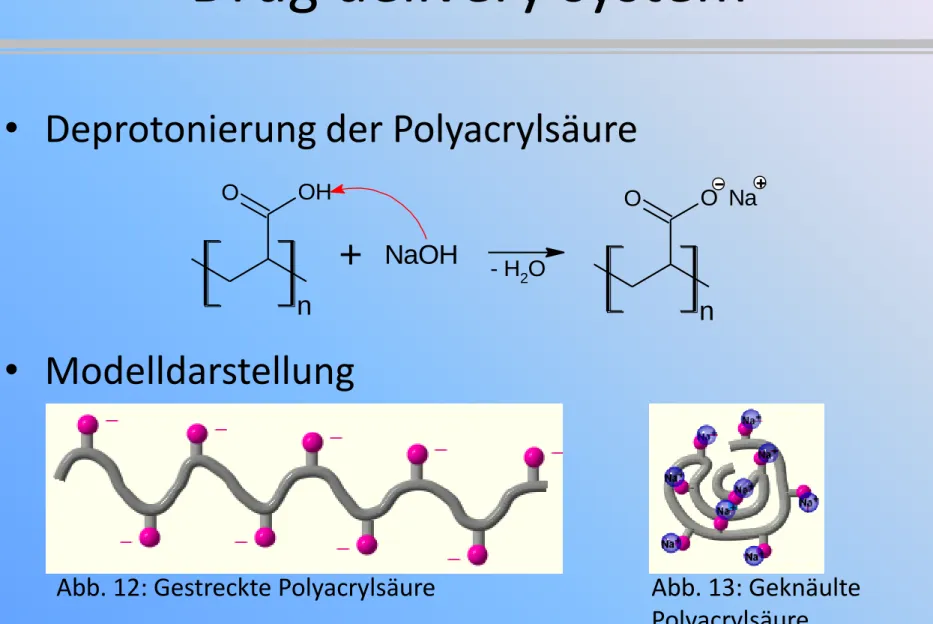
•
Deprotonierung der Polyacrylsäure
•
Modelldarstellung
O OH
n
+ NaOH - H
2O
O- O
n
Na+
Abb. 12: Gestreckte Polyacrylsäure Abb. 13: Geknäulte
Drug delivery system
• vernetzte Polyacrylsäure knäult sich nicht zusammen und kann bis 1000 g Wasser
pro Gramm Polymer aufnehmen
• Aspirin protect kontrahiert im Magen (saures Milieu) und quillt erst im Darm auf (basisches Milieu)
• die Polymerschicht wird dann durchlässig für den Wirkstoff, bleibt aber selbst als Schicht stabil
C H2
O
O O
O
CH2 Ethylenglycoldiacrylat
Elektrotechnik
• Polymere Werkstoffe wurden früher nur als Isolatoren genutzt, z.B. Bakelit
• heute: Einsatz in Batterien/Akkumulatoren, Solarzellen
• Vorteile gegenüber den metallischen Leitern und Halbleitern:
preiswertere Herstellung, geringes Gewicht, bessere Formungsmöglichkeiten, höhere Leistungsfähigkeit
• Nachteile: weder chemisch so stabil noch eine ähnliche Langlebigkeit
Elektrotechnik
Abb. 14: Leitfähigkeiten
cis-Polyacetylen
N H
N H
N H
N H
Undotiertes Polypyrrol
Demonstration 2 -Leitfähige Polymere
Polypyrrol
• Anodische Oxidation zu Pyrrolradikalen
N H
+ e-
N H
N H N
H
N H N
H N
H
N H
+
N H
N H N
H
N H H H
+ 2 H+
Polypyrrol
• bei pH ≥ 7 entsteht durch die Deprotonierung des Stickstoffatoms eine isolierende Polypyrrolfolie
Dotiertes Polypyrrol
Cl O O
O O-
Cl O O-
O O
Cl O O-
O O N
H
+
N H
N H
N H
+
N H
N H
N H
+
N
H n
Leitfähige Polymere
• Polypyrrol
– leitfähige Textilien, z.B. Socken für amerikanische Soldaten die sich bei 10-12 V aufheizen
• Polyanilin
– Überzug auf amerikanischen Stealth-Jets, die die ausgesandten Mikrowellen komplett absorbieren
• Poly(phenylenvinylen) (grün), Polythiopen (rot) und Polyfluoren (blau)
– OLEDs (Organic Light Emmitting Diodes): leuchtkräftige Displays mit geringem Stromverbrauch, hoher Leuchtkraft und
Unabhängigkeit vom Blickwinkel
Zurück zum drug delivery system
Schauen wir mal nach, wie es unserer
Aspirin protect mittlerweile ergangen ist...
Abb. 15: Aspirin protect
Bauindustrie
• Bindemittel/Dispersionpulver für Dichtmassen und Mörtel
• Rohre (PVC)
• Fenster (Plexiglas)
• Abdichtungen/Klebstoffe
• Wärmedämmung
Demonstration 3 - Polyurethanschaum
Demonstration 3 - Polyurethanschaum
•
Polyadditionsreaktion
N N
1,4-Diazabicyclo[2.2.2]octan
+ H O R1 OH
+ - N
N
O C N N C O
Diphenylmethan-diisocyanat
Demonstration 3 - Polyurethanschaum
+
N N
O
H R1 O C O
N R2 N C O H
Urethanbindung N
N
H O+ C
O N- R2 N C O R1
O H
Versuch 5 - Wärmedämmung
• Temperaturmessung in den Suppendosen
• wärmeisolierende Eigenschaft aufgrund der zahlreichen Lufteinschlüsse
• Gase sind generell schlechte Wärmeleiter
• die vielen Poren im PU-Schaum verhindern ein Zirkulieren der Luft und begünstigen die
Wärmeisolierung
Schulrelevanz
• Grund- und Leistungskurse der Qualifikationsphase 4
• Wahlthema Angewandte Chemie
– Unterthema „Werkstoffe“, natürliche und synthetische Makromoleküle
• Inhalte:
– Klassifizierung – Reaktionstypen
– Großtechnische Herstellung
– Polymer mit besonderen Eigenschaften
Abbildungsverzeichnis
Abb. 1-3: https://www.fh-muenster.de/fb3/downloads/werkstofftechnik/Kunststoffanwendungen/KmK_2__
Herstellung-Aufbau-Zusammensetzung-Einteilung.pdf
Abb. 4: http://www.kunststoff-schweiz.ch/assets/images/Bakelizer.jpg Abb. 5: http://www.replicata.de/bilder/produkte/431000000B.jpg
Abb. 6: http://images.manufactum.de/manufactum/grossbild/82985_1.jpg
Abb. 7: http://www.chemgapedia.de/vsengine/media/vsc/de/ch/9/mac/andere/pmma/transparent2schu.jpg Abb. 8: http://www.chemgapedia.de/vsengine/vlu/vsc/de/ch/10/styrol_polymerisation/polystyrol/polystyrol.
vlu/Page/vsc/de/ch/10/styrol_polymerisation/polystyrol/herstellung_von_standard_ps/herstellung _von_standard_ps.vscml.html
Abb. 9: http://www.chemgapedia.de/vsengine/media/vsc/de/ch/10/styrol_polymerisation/polystyrol/
aufarbeitung_standard_ps/medien/granulat.jpg
Abb. 10: http://academic.brooklyn.cuny.edu/biology/bio4fv/page/amylose.jpg Abb. 11: http://www.hermsen.de/shop/media/81010037.jpg
Abb. 12: http://www.chemgapedia.de/vsengine/media/vsc/de/ch/9/mac/andere/acrylsaeure/
polyelektrolyt.png
Abb. 13: http://www.chemgapedia.de/vsengine/media/vsc/de/ch/9/mac/andere/acrylsaeure/polysalz.png Abb. 14: http://www.chemgapedia.de/vsengine/media/vsc/de/ch/9/mac/andere/acetylen/leitfaehig.gif
Literaturverzeichnis
• Brandl, H.; Kabuß, S.:Herstellung eines Fluoreszenz-Solarkollektors. In: Praxis der Naturwissenschaften, 6/37, S. 24ff. 1988.
• Brückner, R.: Reaktionsmechanismen. 3. Auflage. Spektrum Verlag. 2004.
• Bruice, P: Organische Chemie. 5. aktualisierte Auflage. Pearson. 2009.
• Burgemeister, S.: Kunststoffe. Zu finden unter URL:
http://www.chids.de/dachs/expvortr/671Kunststoffe_Burgemeister.doc. Letzter Zugriff am 09.06.2010.
• Büttner, M.; Wagner, G.: Herstellung von essbarem Einweggeschirr. Zu finden als Downloadmaterial unter URL: http://www.friedrich-
verlag.de/go/?action=ShowProd&prod_uuid=ADF0893F5DF74A3FB484CBFBB28C22F4.
Letzter Zugriff am 09.06.2010.
• Flintjer, B.; Jansen, W.: Polypyrrol und Polypyrrol-Batterien. In: Praxis der Naturwissenschaften - Chemie. 3/38, S. 7-11. 1989
• Hessisches Kultusministerium. Lehrplan Chemie für die Jahrgangsstufen G7 bis G12. 2005. Zu finden unter URL:
http://www.kultusministerium.hessen.de/irj/HKM_Internet?uid=3b43019a-8cc6-1811-f3ef- ef91921321b2. Letzter Zugriff am 13.06.2010.
Literaturverzeichnis
• Köhler-Krützfeldt, A.: Fortschritt durch Polymere. In: Praxis der Naturwissenschaften - Chemie. 5/51, S. 2-5. 2002.
• Kühn, I.: Herstellung von essbarem Einweggeschirr. In: Naturwissenschaften im Unterricht Chemie. 9, Heft 45, S. 55-56. 1998.
• Lechner, M.D.: Makromolekulare Chemie. 4. überarbeitete Auflage. Birkhäuser. 2009.
• Rickelt, E.: Lehrerfortbildung - Kunststoffmüll. S. 21f. Philipps-Universität Marburg, Fachbereich Chemie. 1998.
• Rickelt, E.: Polymerisation von Methacrylsäureester (Plexiglas). Philipps-Universität Marburg, Fachbereich Chemie.
• Rickelt, E.: Polyurethan auf Lignin-Basis. Philipps-Universität Marburg, Fachbereich Chemie.
• Kunststoff-Schweiz: Kunststoff - Geschichte. Zu finden unter URL: http://www.kunststoff- schweiz.ch/html/2__seite.html. Letzter zugriff am 14.06.2010.